
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
(Иэ)ЦӘК¶НшВз
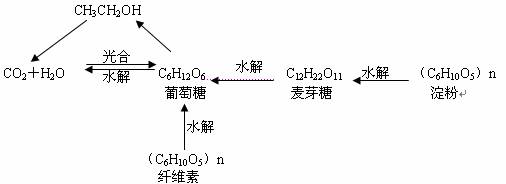

(¶ю)УНЦ¬Улө°°ЧЦКЎў°ұ»щЛбөДұИҪП
|
Ааұр |
Ҫб№№МШөг |
ЦчТӘРФЦК |
јмСй·Ҫ·Ё |
УГНҫ |
|
УНЦ¬ |
ёЯј¶Ц¬·ҫЛбәНёКУНРОіЙөДхҘ |
1І»ұҘәНУНЦ¬Зв»Ҝ 2хҘөДЛбРФЎўјоРФЛ®Ҫв |
ЁDЁDЁDЁD |
ЦЖ·КФнЎўИЛөД»о¶ҜјдҪУДЬФҙ |
|
ө°°ЧЦК |
УЙІ»Н¬°ұ»щЛбЛхЛ®РФөДҪб№№ёҙФУөДёЯ·ЦЧУ»ҜәПОп |
1СООц 2ұдРФ 3СХЙ«·ҙУҰ 4ЧЖЙХҪ№УрГ«ЖшО¶ 5Л®ҪвіЙ°ұ»щЛб 6БҪРФ |
1СХЙ«·ҙУҰ 2ЧЖЙХ |
УӘСшОпЦК |
|
°ұ»щЛб |
·ЦЧУЦРјИУР°ұ»щЈ¬УЦУРфИ»щ |
1ҫЯУРБҪРФ 2·ЦЧУјдЛхЛ®ЙъіЙёЯ·ЦЧУ»ҜәПОп |
ЎЎ ЁDЁDЁDЁDЁD |
ЎЎ УӘСшОпЦК |
(Т»)МЗАа
|
Ааұр |
ЖПМСМЗ |
ХбМЗ |
ВуСҝМЗ |
өн·Ы |
ПЛО¬ЛШ |
|
·ЦЧУКҪ |
C6H12O6 |
C12H22O11 |
C12H22O11 |
(C6H10O5)n |
(C6H10O5)n |
|
·ЦЧУҪб№№МШөг |
ә¬УРфЗ»щ ЎўИ©»щ |
ОЮИ©»щ |
УРИ©»щ |
ОЮИ©»щ |
ОЮИ©»щ УРфЗ»щ |
|
ЦчТӘРФЦК |
хҘ»Ҝ·ҙУҰЎў Тшҫө·ҙУҰЎў әНРВЦЖЗвСх»ҜНӯ·ҙУҰ |
Л®ҪвіЙЖПМСМЗәН№ыМЗ |
Л®ҪвіЙЖПМСМЗ |
Л®ҪвіЙЖПМСМЗ |
Л®ҪвіЙЖПМСМЗ |
|
ЦчТӘУГНҫ |
ЦЖТ©ЎўЦЖҫө |
МрО¶јБ |
МрО¶јБ |
КіУГЎўЦЖЖПМСМЗЎўҫЖҫ« |
·ДЦҜЎўФмЦҪЎўЦЖПхЛбПЛО¬ЎўҙЧЛбПЛО¬ЎўХіҪәПЛО¬ |
ұҫЧЁМв°ІЕЕФЪМюөДСЬЙъОпЦ®әуЈ¬С§ЙъТСХЖОХБЛ№ЩДЬНЕҫц¶ЁУР»ъОпөДРФЦКөДС§П°·Ҫ·ЁЈ¬ФЛУГХвТ»·Ҫ·ЁҝЙНЁ№эЧФС§ХЖОХ¶а№ЩНЕ»ҜәПОпөДУР№ШРФЦКЈ¬ІўДЬФЛУГУР»ъОп·ЦЧУҪб№№ЦР¶а№ЩДЬНЕ¶ФЖд»ҜС§РФЦКөДЦШТӘУ°ПмЎЈ
ёҙП°ұҫЧЁМвКұТӘГЬЗРБӘПөЙъ»оЎўЙъІъКөјКјУЙо¶ФС§ҝЖЦӘК¶өДАнҪвЎЈ
МЗАаУНЦ¬ө°°ЧЦКРЎҪб
НЁ№эұҫЧЁМвөДёҙП°ХЖОХМЗАаЎўУНЦ¬әНө°°ЧЦКФЪҪб№№ЙПөДМШөгЈә¶а№ЩДЬНЕЎЈАэИзНЁ№эЖПМСМЗөДёҙП°ТӘАнҪвЖПМСМЗ·ЦЧУҪб№№јИә¬ҙјфЗ»щ--ҫЯУРҙјөДРФЦКДЬ·ўЙъхҘ»Ҝ·ҙУҰЈ»ә¬УРИ©»щ--ҫЯУР»№ФӯРФДЬ·ўЙъТшҫө·ҙУҰЈ¬НЁ№эУНЦ¬·ЦЧУҪб№№өДёҙП°БЛҪвУНЦ¬·ЦЧУҪб№№ЦРјИә¬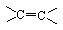 јь--ДЬК№деЛ®НКЙ«Ј»УЦә¬хҘ»щДЬ·ўЙъЛ®Ҫв·ҙУҰЎЈНЁ№э¶Ф°ұ»щЛбө°°ЧЦКөДёҙП°БЛҪвЈ¬-COOHҫЯЛбРФЈ¬-NH2ҫЯјоРФЎЈ
јь--ДЬК№деЛ®НКЙ«Ј»УЦә¬хҘ»щДЬ·ўЙъЛ®Ҫв·ҙУҰЎЈНЁ№э¶Ф°ұ»щЛбө°°ЧЦКөДёҙП°БЛҪвЈ¬-COOHҫЯЛбРФЈ¬-NH2ҫЯјоРФЎЈ
27Ј®(12·Ц)ПЦУРFeЎўCuЧйіЙөДәПҪрЈ¬ЖдЦРFeЎўCuөДЧЬОпЦКөДБҝОӘa molЈ¬CuөДОпЦКөДБҝ·ЦКэОӘxЈ¬СРіЙ·ЫД©әуЈ¬И«ІҝН¶Илә¬b mol HNO3өДПЎИЬТәЦРЈ¬ОўИИК№Ждід·Ц·ҙУҰЈ¬ЗТПхЛбөД»№ФӯІъОпЦ»УРNOЈ¬КФ»ШҙрПВБРОКМвЈә
(1)ИфКЈУаөДІРФьЦ»УРCuЈ¬ФтИЬТәЦРә¬УРөДҪрКфАлЧУОӘЎЎЎЎЎЎЎЎЎЎЎЎ ЎЈ(РҙіцЛщУРҝЙДЬөДЗйҝц)
(2)өұИЬТәЦРҪрКфАлЧУЦ»УРFe2+ЎўCu2+КұЈ¬ФтbөДИЎЦө·¶О§КЗ(УГaЎўxұнКҫ)ЎЎЎЎЎЎЎЎЎЎ ЎЈ
(3)өұxЈҪ50%Ј¬ИЬТәЦРFe3+УлFe2+өДОпЦКөДБҝПаөИКұЈ¬ФЪұкЧјЧҙҝцПВ№ІІъЙъ0.672 LЖшМеЈ¬ЗуaЎўbөДЦөЎЈ
2006ДкЙШ№ШКРЖХНЁёЯөИѧУХРЙъҝјКФДЈДвІвКФ
26Ј®(8·Ц)ПВНјОӘДіКРКЫСОЛбКФјБЖҝұкЗ©ЙПөДІҝ·ЦКэҫЭЈ¬ОКЈә
(1)ёГСОЛбөДОпЦКөДБҝЕЁ¶ИОӘ¶аЙЩЈҝ
 ЎЎ
ЎЎ
(2)ИЎёГСОЛб25.4 mLУл2.00 molЎӨL-1өДЗвСх»ҜДЖ
ИЬТә100 mL»мәПЈ¬ФЩҪ«»мәПТәПЎКНөҪ1.00 LЈ¬
ҙЛКұИЬТәөДpHФјОӘ¶аЙЩЈҝ
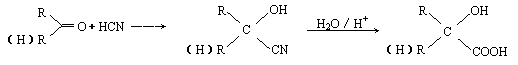
25Ј®(10·Ц)ТСЦӘЈәЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
 ЎЎЎЎ
ЎЎЎЎ
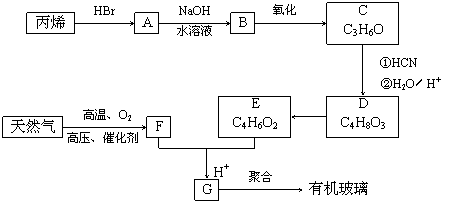
УР»ъІЈБ§ҝЙ°ҙПВБРВ·ПЯәПіЙЈә
 ЎЎ
ЎЎ
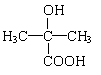 ЎЎ
ЎЎ
ЖдЦРDөДҪб№№јтКҪОӘЈә ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ¬GөД»ҜС§КҪОӘC5H8O2 Ј¬FТаҝЙУЙЛ®ГәЖшФЪёЯОВЎўёЯС№ЎўҙЯ»ҜјБПВәПіЙЎЈ
КФРҙіцЈә
(1)МмИ»ЖшЦчТӘіЙ·ЦөДөзЧУКҪОӘ______________Ј¬BөДҪб№№јтКҪОӘ____________________ЎЈ
(2)E+F Ўъ GөД·ҙУҰ·ҪіМКҪОӘ___________________________________________________ЎЈ
(3)Ў°ұыПЎ Ўъ AЎұәНЎ°D Ўъ EЎұөД·ҙУҰАаРН·ЦұрКфУЪ________________Ўў________________ЎЈ
(4)Рҙіц·ЦЧУЦРН¬Кұә¬УР-OHәН-COOHөДDөДН¬·ЦТм№№МеөДҪб№№јтКҪ
_____________________________________________________________
24Ј®(8·Ц)ЦКЧУәЛҙЕ№ІХс(PMR)КЗСРҫҝУР»ъОпҪб№№өДУРБҰКЦ¶ОЦ®Т»Ј¬ФЪЛщСРҫҝөД»ҜәПОп·ЦЧУЦРЈ¬ГҝТ»ёцҪб№№ЦРөДөИРФЗвФӯЧУөДPMRЖЧЦР¶јёшіцБЛПаУҰөД·е(РЕәЕ)Ј¬ЖЧЦР·еөДЗҝ¶ИУлҪб№№ЦРөДөИРФЗвФӯЧУКэіЙХэұИЎЈПЦУРДіЦЦУР»ъОпЈ¬НЁ№эФӘЛШ·ЦОцөГөҪөДКэҫЭОӘCЈә85.71%Ј¬HЈә14.29%(ЦКБҝ·ЦКэ)Ј¬ЦКЖЧКэҫЭұнГчЛьөДПа¶Ф·ЦЧУЦКБҝОӘ84ЎЈ
(1)ёГ»ҜәПОпөД»ҜС§КҪОӘ_____________ЎЈ
ТСЦӘёГОпЦКҝЙДЬҙжФЪ¶аЦЦҪб№№Ј¬AЎўBЎўCКЗЖдЦРөДИэЦЦЈ¬ЗлёщҫЭПВБРТӘЗуМоҝХЈә
(2)AУлЗвЖшјУіЙЙъіЙ2-јЧ»щОмНйЈ¬ФтAөДҝЙДЬҪб№№УР___________ЦЦЎЈ
(3)BДЬК№деЛ®әНЛбРФёЯГМЛбјШНКЙ«Ј¬PMRЖЧЦРЦ»УРТ»ёцРЕәЕЈ¬ФтBөДҪб№№јтКҪОӘЈә
________________________
(4)CІ»ДЬК№ЛбРФёЯГМЛбјШИЬТәНКЙ«Ј¬І»ДЬУлдеЛ®јУіЙНКЙ«Ј¬ҝЙЭНИЎдеЛ®ЦРөДдеЈ»PMRЖЧЦРТІЦ»УРТ»ёцРЕәЕЈ¬ФтCөДҪб№№јтКҪОӘЈә____________________________
23Ј®( 10·Ц)Ҫ«1 mol I2(g)әН2 mol H2ЦГУЪДі2 LГЬұХИЭЖчЦРЈ¬ФЪТ»¶ЁОВ¶ИПВ·ўЙъ·ҙУҰЈә
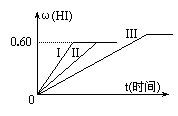 ЎЎI2(g)+H2(g)
ЎЎI2(g)+H2(g)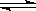 2HI(g)Ј»ЎчHЈј0Ј¬
2HI(g)Ј»ЎчHЈј0Ј¬
ІўҙпөҪЖҪәвЈ¬HIөДМе»э·ЦКэҰШ(HI)ЛжКұјдұд»ҜИзНј
ЗъПЯ(II)ЛщКҫЈә
(1)ҙпЖҪәвКұЈ¬I2(g)өДОпЦКөДБҝЕЁ¶ИОӘ______________ЎЈ
(2)ИфёДұд·ҙУҰМхјюЈ¬ФЪјЧМхјюПВҰШ(HI)өДұд»ҜИзНјЗъПЯ(I)ЛщКҫЈ¬ФЪТТМхјюПВҰШ(HI)өДұд»ҜИзНјЗъПЯ(III)ЛщКҫЎЈФтјЧМхјюҝЙДЬКЗ__________(МоИлПВБРМхјюөДРтәЕЎЈПВН¬)Ј¬ТТМхјюҝЙДЬКЗ___________ЎЈ
ўЩ әгИЭМхјюПВЈ¬ЙэёЯОВ¶И
ўЪ әгИЭМхјюПВЈ¬ҪөөНОВ¶И
ўЫ әгОВМхјюПВЈ¬ЛхРЎ·ҙУҰИЭЖчМе»э
ўЬ әгОВМхјюПВЈ¬А©ҙу·ҙУҰИЭЖчМе»э
ўЭ әгОВәгИЭМхјюПВЈ¬јУИлККөұҙЯ»ҜјБ
(3)ИфұЈіЦОВ¶ИІ»ұдЈ¬ФЪБнТ»ПаН¬өД2 LГЬұХИЭЖчЦРјУИлa mol I2(g)Ўўb mol H2әНc mol HI(aЎўbЎўcҫщҙуУЪ0)Ј¬·ўЙъ·ҙУҰЈ¬ҙпЖҪәвКұЈ¬HIөДМе»э·ЦКэИФОӘ0.60Ј¬ФтaЎўbЎўcөД№ШПөКЗ___________ЎЈ
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com