
题目列表(包括答案和解析)
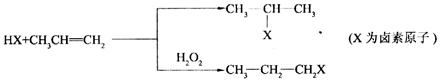
23.(8分)[化学一有机化学基础]有机化学反应因反应条件不同,可生成不同的有机产物。例如:
工业上按下列路线合成结构简式为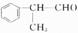 的物质,该物质是一种香料。
的物质,该物质是一种香料。
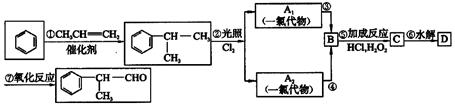
请回答下列问题:
(1)写出A1、A2可能的结构简式:A1_______;A2______________。
(2)反应⑤的化学方程式为__________________。
(3)工业生产中,中间产物经反应③④⑤⑥得D,而不是由A1或A2直接转化为D。其优越性主要是__________。
(4)这种香料有多种同分异构体,写出2种符合下列条件的有机物的结构简式:
a.其水溶液遇FeCl3溶液变紫色;
b.分子中有苯环,且苯环上的一溴代物只有2种。
_____________________,___________________________。
22.(12分)将2molSO2和1molO2混合置于容积为2L的密闭容器中,在800 K时,发生如下反应:
 2SO2(g)+O2(g) 2SO3(g) △H=-196056kJ·mol-1
2SO2(g)+O2(g) 2SO3(g) △H=-196056kJ·mol-1
当反应从开始进行到5min时,反应达到平衡状态,测得混合气体总物质的量为2.1 mol。
请回答下列问题:
(1)800K时,该反应的平衡常数为_____,在0-5min时间间隔内SO2的反应速率为___。
(2)若在5min时降低温度,在某一时刻重新达到平衡状态,则新平衡混合物中气体的总物质的量________2.1 mol(填“>”、“<”或“=”),简述你的判断理由:__________。
(3)若相同条件下,向该容器内分别充人xmolSO2、ymolO2和zmolSO3,反应达到平衡时,容器内混合气体总物质的量仍为2.1 mol。则:x、y、z必须满足的关系是__________。(一个用含x、z的式子表示,一个用含y、z的式子表示)
(4)相同条件下,若在上述容器中,充入0.2 mol SO2、0.4 mol O2和4.0molSO3三种气体,下列对该反应状态的描述中,正确的是________(填字母序号)。
A.处于平衡状态
B.不是平衡状态,反应正向进行
C.不是平衡状态,反应逆向进行
[选做部分]
21.(14分)下表是A、B、C、D四种有机物的有关信息;
|
A |
B |
C |
D |
|
①由C、H、O三种元素组成 ②球棍模型为: 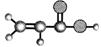 ⑧能与NH3在一定条件下反应生成丙烯酰胺 (CH2-CH-CONH2) |
①由C、H、O三种元素组成 ②能与Na反应,但不能与NaOH溶液反应 ③能与A反应生成相对分子质量为100的酯 |
①相对分子质量与B相同 ②能被弱氧化剂氢氧化铜氧化 ③能与NaHCO3溶液反应放出CO2气体 |
①能使溴的四氧化碳溶液退色 ②能与水在一定条件下反应生成B |
请回答下列问题:
(1)与D在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通武CnH2n。当n=__________时,开始出现该类有机物的同分异构体。
(2)在一定条件下,D分子之间能生成一种具有广泛用途的高分子化合物,写出该高分子化合物的名称是________。
(3)写出A与NH3在一定条件下反应生成丙烯酰胺的化学方程式,并指出反应类型:______,反应类型:________。
(4)丙烯酰胺有多种同分异构体,试写出3种分子中同时含有醛基(-CHO)和碳碳双
键(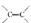 )的同分异构体的结构简式:____________、________________、_____________。
)的同分异构体的结构简式:____________、________________、_____________。
(5)写出B与C反应的化学方程式:
20.(10分)甲、乙、丙为三种常见短周期元素,它们的原子序数依次增大,已知甲元素原于最外层电子数比乙元素原子的多一个,乙元素原于最外层电子数与其电子层数相等,丙元素原子最外层电子数是乙元素原子最外层电子数的2倍。物质A、B属于钠盐,物质C是一种强酸;又知:A中含乙元素,B中含甲元素,C中含丙元素。各种物质之间的相互转化关系如下图所示(部分产物未给出):
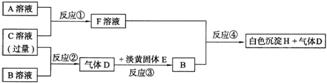
请回答下列问题:
(1)丙元素的原子结构示意图为____________,白色沉淀H的化学式为_______________。
(2)反应①的离子方程式为_________________。
(3)用离子方程式解释B溶液pH>7的原因:__________________。
(4)写出反应③的化学方程式:_________________________。
19.(9分)某研性学习小组用下图装置验证二氧化锰对氯酸钾分解的催化作用,实验时均以生成25mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
|
实验序号 |
KClO3的质量 |
加入的物质及其质量 |
生成25 mL气体所用时间 |
|
Ⅰ |
1.2 g |
无 |
t1(min) |
|
Ⅱ |
1.2 g |
MnO2 0.5 g |
t2(min) |
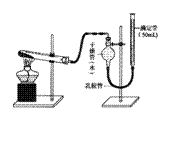 (1)实验装置中滴定管是_____(填“酸式”或“碱式”)
(1)实验装置中滴定管是_____(填“酸式”或“碱式”)
滴定管(50 mL);若要测得实验所需气体体积,滴
定管中起始液面读数(初读数)应控制的刻度范围
是_____。
(2)仪器组装完成后,检验该套装置气密性的操作是
__________________________。
(3)若实验中测得t2<t1,实验小组经过讨论,认为上述
实验还不能完全证明MnO2一定起了催化作用,需
再补做实验。请利用实验n反应后的剩余物和下面提供的合适用品补做实验(简要说明实验步骤,可不填满,也可以补充)。提供的用品有:H2O2溶液、浓盐酸、硝酸、MnO2、NaOH溶液、AgNO3溶液、KClO3、木条、淀粉-KI试纸、蒸馏水及必要的实验仪器。
①__________________________________________:
②___________________________________________;
③__________________________________________。
18.(6分)为测定某种硫酸铜晶体(CuSO4·xH2O)中x的值,某化学实验小组进行了如下实验:
①称取23.2gCuSO4·xH2O晶体,研细后转移入烧杯中,加蒸馏水使其完全溶解;
②向上述所得溶液中滴人过量NaOH溶液;
③将步骤②所得混合物过滤、洗涤后,再将固体转移至坩埚中,灼烧,直至质量不再变化冷却后,称得固体质量为8.0g
请回答下列问题;
(1)步骤①中研磨固体所用仪器的名称是__________。
(2)步骤③中洗涤沉淀的操作要点是:______________________。
(3)x=______________。
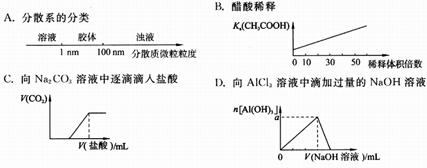
17.将某些化学知识用图像表示,可以收到直观、简明的效果。下列图象所表示的化学知识
中,不正确的是 ( )
[必做部分]
16.X、Y、Z、W为四种短周期元素,已知x、Z同主族,Y、W同周期;X的气态氢化物比Z的稳定;Y的阳离子比W的阳离子氧化性强;Y的阳离子比2的阴离子少一个电子层。下列表示中,正确的是 ( )
A.原子序数,X的>Y的>Z的>W的 B.简单离子半径:W的>Y的>Z的>X的
C.原子半径:W的>Y的>Z的>X的 D.原子的得电子能力:X的<Z的
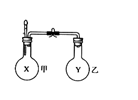
14.某同学仿照“喷泉”实验的原理,在实验室中做了一个“喷烟”实验,如图所示。他在甲,乙两个烧瓶中分别充人X、Y两种无色气体,在胶头滴管中盛有含酚酞的NaOH溶液,实验时将胶头滴管内的液体挤入甲烧瓶内,然后打开止水夹,便可看到甲烧瓶中的导管口喷出白色的烟,同时甲烧瓶中的溶液颜色逐渐变浅。若已知X、Y是HCl、NH3、Cl2、O2、CH4、SO2、NO七种气体中的两种,则下列判断中,正确的是( )
|
C.X是SO2,Y是O2 D.X是NO,Y是O2
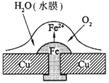 15.铜板上铁铆钉处的吸氧腐蚀原理如右图所示,下列有关说法中,不正确的是 ( )
15.铜板上铁铆钉处的吸氧腐蚀原理如右图所示,下列有关说法中,不正确的是 ( )
A.正极电极反应式为:2H++2e-→H2↑
B.此过程中还涉及到反应:4Fe(OH)2+2H2O+O2=4Fe(OH)3
C.此过程中铜并不被腐蚀
D.此过程中电子从Fe移向Cu
13.在298K、1.01×105Pa下,12g石墨在24g氧气中燃烧至反应物完全消耗,测得放出
xkJ的热量。已知在该条件下,1mol石墨完全燃烧放出ykJ的热量。则石墨与氧气反
应生成CO的热化学方程式表达正确的是 ( )
A.C(石墨,s)+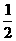 O2(g)=CO(g) △H(298K)=-ykJ·mol-1
O2(g)=CO(g) △H(298K)=-ykJ·mol-1
B.C(石墨,s)+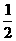 O2(g)=CO(g) △H(298K)=-xkJ·mol-1
O2(g)=CO(g) △H(298K)=-xkJ·mol-1
C. C(石墨,s)+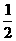 O2(g)=CO(g)
△H(298K)=-(2x-y)kJ·mol-1
O2(g)=CO(g)
△H(298K)=-(2x-y)kJ·mol-1
 D.2 C(石墨,s)+
D.2 C(石墨,s)+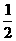 O2(g)=CO(g) △H(298K)=-(2x-y)kJ·mol-1
O2(g)=CO(g) △H(298K)=-(2x-y)kJ·mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com