
题目列表(包括答案和解析)
26.(16分)某无色溶液A中含有K+、Cl-、OH-、SO32-、SO42-,为检验确认其中所含的各阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞试液。检验其中OH- 的实验方法从略,检验其他阴离子的过程如下图所示。

(1)图中试剂①-⑤溶质的化学式分别是:
① ,② ,③ ,④ ,⑤ 。
(2)图中现象a、b、c表明检验出的离子分别是:a 、b 、c 。
(3)白色沉淀B加试剂②反应的离子方程式是:
。
(4)无色溶液B加试剂③的主要目的是 。
(5)白色沉淀B若加试剂③而不加试剂②对实验的影响是
。
(6)无色溶液B加过量试剂③发生反应的离子方程式是:
。
13.已知可逆反应:2X(g) + Y(g)  m Z(g);ΔH=- a kJ·mo1-l (a>0)。现有甲、乙两个容积相等的容器,向甲容器中充入2 mol X和l molY,达到平衡时放出热量b kJ;向乙容器中充入1 mol X和0.5 molY,达到平衡时放出热量c kJ,且b >2c。则a、b的大小关系及m的值域正确的是
m Z(g);ΔH=- a kJ·mo1-l (a>0)。现有甲、乙两个容积相等的容器,向甲容器中充入2 mol X和l molY,达到平衡时放出热量b kJ;向乙容器中充入1 mol X和0.5 molY,达到平衡时放出热量c kJ,且b >2c。则a、b的大小关系及m的值域正确的是
A.a = b m = 3 B.a > b m≤2
C.a < b m≤2 D.a > b m = 2
12.常温下,已知a mol·L-1的某一元强酸HA的稀溶液和b mol·L-1的某一元弱碱BOH的稀溶液等体积混合后溶液pH = 7,则下列叙述不正确的是
A.a < b
B.酸溶液中c (H+ )大于碱溶液c (OH-)
C.反应后溶液中c (B+ ) > c (A-)
D.反应后溶液中c (BOH) + c (B+ ) = b /2 mol·L-1
11.在体积为V L的密闭容器中通入a mol NH3和b mol HCl,充分反应后容器内阳离子和阴离子的个数比为
A.1∶1 B.小于1∶1 C.a∶b D.(a+b)∶ b
10.下列有关电解精炼铜的说法不正确的是
A.粗铜作阳极
B.用CuSO4溶液作电解液
C.阴极的电极反应式为:Cu2+ + 2e- = Cu
D.当阳极质量减少a g时,阴极质量一定增加a g
9.A、B、C三种短周期元素,原子序数按A、B、C依次增大,A元素原子最外层电子数是次外层电子数的2倍,B元素原子的次外层电子数是最外层电子数的2倍,C元素原子的最外层电子数是内层电子总数的一半。则下列说法中正确的是
A.B元素在自然界的含量最多
B.C元素可以组成不同的单质,它们均易溶于CS2
C.A、B、C元素的常见单质的熔点:A>B>C
D.A、B、C的氧化物都能溶于水形成酸
8.表示下列变化的化学用语正确的是
A.NaHCO3的水解:HCO3- + H2O H3O+
+ CO32-
H3O+
+ CO32-
B.NaOH的结构式:Na-O-H
C.钢铁吸氧腐蚀的正极反应式:4OH--4e- = O2↑+ 2H2O
D.1 L 0.5 mo1·L-1 稀硫酸与1 L 1 mol·L-1氢氧化钠溶液反应放出57.3 kJ的热量:
H2SO4 (aq) + 2NaOH (aq) = Na2SO4 (aq) + 2H2O (1);ΔH=-114.6 kJ·mo1-l
7.用NA表示阿伏加德罗常数的值,下列说法正确的是
A.呈中性的稀溶液1 L里含有10-7 NA个H+
B.每升硫酸溶液里含有10-2 NA个H+,该硫酸溶液的pH为2
C.NA个NH4+ 有10 mol质子
D.常温下2.24 L庚烷中有1.6 NA个极性键
6.下列各选项中,两个反应所遵循的化学原理最相似的是
A.葡萄糖和甲醛分别与新制的氢氧化铜悬浊液共热,都产生红色沉淀
B.苯酚和乙烯都能使溴水褪色
C.二氧化硫和过氧化氢都能使品红溶液褪色
D.氯气用于水的杀菌消毒和明矾用于净水
24.(8分)[化学-物质结构与性质]
有A、B、C、D四种元素,其中A元素和U元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A+与D2-离子数之比为2:1。
请回答下列问题:
(1)A元素形成的晶体属于A2密堆积型式,则其晶体内晶胞类型应属于____(填写“六方”、“面心立方”或“体心立方”)。
(2)B-的电子排布式为____,在CB3分子中C元素原子的原子轨道发生的是________杂化。
 (3)C的氢化物的空间构型为_________,其氢化物在同族元素所形成的氢化物中沸点最高的原田是__________。
(3)C的氢化物的空间构型为_________,其氢化物在同族元素所形成的氢化物中沸点最高的原田是__________。
(4)B元素的电负性_______D元素的电负性(填“>”,“<”
或“=”);用一个化学方程式说明B、D两元素形成的
单质的氧化性强弱:____________。
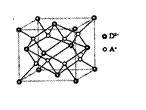
(5)如图所示是R形成的晶体的晶胞,设晶胞的边长为acm。试计算R晶体的密度。(阿伏加德罗常数用NA表示)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com