
题目列表(包括答案和解析)
7.有一种名叫L-多巴的药物可用于治疗帕金森综合症,其结构简式为:
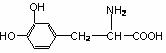
下列关于L-多巴的说法不正确的是( )
A.该有机物中所有碳原子可能处于同一个平面
B.该机物既可以与盐酸反应,又可以与氢氧化钠溶液反应
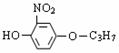
C.该有机物与 互为同分异构体
D.该有机物属于芳香烃类
6.A、B混合气体在密闭容器中发生如下反应:xA(g)+yB(g)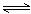 zC(g),
△H<0;达到化学平衡后测得A气体的浓度为0.5mol/L;当恒温下将密闭器的容积扩大一倍并再次达到平衡时,测得A气体的浓度为0.3mol。则下列叙述正确的是( )
zC(g),
△H<0;达到化学平衡后测得A气体的浓度为0.5mol/L;当恒温下将密闭器的容积扩大一倍并再次达到平衡时,测得A气体的浓度为0.3mol。则下列叙述正确的是( )
A. 平衡向右移动 B. x+y>z
C. B的转化率提高 D. C的体积分数增加
5. 某溶液的PH=a,向其中插入两惰性电极,通电一段时间后为测知溶液的PH=b,且b=a.则该电解质是(设电解液的温度没有变化)
A.稀H2SO4 B.饱和CuSO4溶液 C.NaCl溶液 D.饱和Na2CO3溶液
4.对危险化学品要在包装标签上印有警示性标志。氢氧化钠溶液应选用的标志是( )




A.爆炸品 B 氧化剂 C 剧毒品 D腐蚀品
3.下列反应的离子方程式正确的是( )
A.碳酸氢钠溶液显碱性:HCO3-+H2O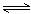 H2CO3+OH-
H2CO3+OH-
B.向沸水中滴加三氯化铁溶液制备氢氧化铁胶体:Fe3++3H2O Fe(OH)3+3H+
Fe(OH)3+3H+
C.向次氯酸钙溶液中通入二氧化硫:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
D.向氢氧化钡溶液中滴加硫酸铜溶液:Ba2++SO42-=BaSO4↓
2.将下列每组内的四种物质同时加入到水中,充分搅拌后,既有氧化还原反应发生,又有沉淀产生的一组是(酸均过量)( )
A. Na2O2、NH4Cl、NaCl、Na2SO4
B. Na2CO3、BaCl2、K2S、盐酸
C. KHCO3、Ca(OH)2、MgCl2、硫酸
D. FeO、AlCl3、Na2SiO3、硝酸
1.设NA为阿伏加德罗常数,下列说法正确的是( )
A.1mol甲基所含有的电子数为10NA
B.标准状况下,22.4LCO2与CO的混合气体含有的碳原子数约为NA
C.1L 1mol/L的盐酸中,所含有的氯化氢分子数为NA
D.标准状况下,11.2L三氧化硫所含有的分子数为0.5NA
29.(16分)瑞典皇家科学院将2004年诺贝尔化学奖授予以色列科学家阿龙·切哈诺沃、阿夫拉姆·赫什科和美国科学家欧文·罗斯,三人共享1000万瑞典克朗(约合136万美元)的奖金,以表彰他们发现了泛素调节的蛋白质降解。
用泛素标记的某天然蛋白质降解产物中含有甘氨酸、丙氨酸、A和M四种α-氨基酸,其中A由C、H、N、O四种元素组成,A能与NaOH反应,也能与盐酸反应。在一定条件下,两分子A发生缩合反应生成B和1个水分子,B的相对分子质量为312,当该蛋白质与浓硝酸反应时显黄色。M中各元素的质量分数为C 54.8%,H 5.58%,N 7.11%,其余为O。M的相对分子质量不超过300,分子中不存在甲基,能与FeCl3溶液发生显色反应,l mol M最多能与3 mol NaOH完全反应。
(1)据此推断A的结构简式为 。
(2)有机物M的相对分子质量为 ,其分子式为 ,符合上述条件的有机物M的可能结构有 (填数字)种,写出其中任意一种与NaOH溶液完全反应的化学方程式:
。
(3)已知α-氨基酸能与亚硝酸反应得到α-羟基酸,例如:



 O
O
O
O

 R―CH―C―OH + HNO2 → R―CH―C―OH + N2↑+H2O
R―CH―C―OH + HNO2 → R―CH―C―OH + N2↑+H2O
NH2 OH
现有某α-氨基酸盐A,其分子中原子数之比为C∶H∶O∶N = 3∶10∶2∶2,由它开始有如下图所示的反应关系,其中无机产物均已略去,括号中的数字为其相对分子质量。
|
 |
|||
|
|||
|
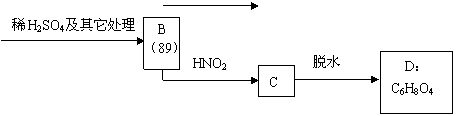
①写出下列有机物的结构简式:
D E
②写出A → B的化学方程式:
28.(13分)已知A-F是中学化学中常见物质,其中A、C、E、F为气体,B、D为液体,D的消费量常作为一个国家工业发达水平的一种标志。F的浓溶液与X共热通常用于实验室制备单质C,X是一种黑色粉末,B是含氧质量分数最高的化合物。反应中部分生成物已略去。试回答下列问题:
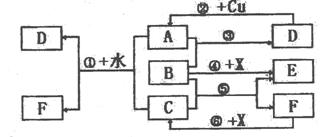
(1)A、C、D三种物质中属于非电解质的是 (填化学式)。
(2)根据图中信息:B、C、D、X氧化性从强到弱的顺序是
。
(3)物质D中含有一种元素Y,Y单质的熔点是112.8℃,则Y单质的晶体类型属于 晶体。Y与碳单质在一定条件下可以生成CY2的化合物,则CY2属于(填“极性”或“非极性”) 分子。
(4)写出反应②的化学方程式: 。
(3)写出反应①、⑥的离子方程式:
① ;
⑥ 。
27.(15分)下图是乙醇脱氢反应的实验装置。
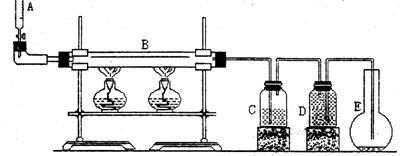
从装置A滴加纯乙醇,通过红热的铜催化剂(在装置B中),生成的气体通过装置C(内盛少量水),一部分气体凝结并溶解于水,剩余气体收集在装置D中(水被排到装置E)。
通过实验证明:
(1)装置D中的气体是纯氢 (2)装置C中溶有沸点为21℃的无色液体X
(3)X不能使溴水褪色 (4)X能生成三氯取代物,不能生成四氯取代物
实验测得1.0 g乙醇经反应后所得氢气的体积为482 mL(标准状况)。
ⅰ.根据上述实验数据,可算出每个乙醇分子脱去的氢原子个数,从而得出液体X的分子式是 。
这一计算的主要计算式为 。
ⅱ.根据有机物的分子结构理论,把乙醇分子在上述反应中几种可能的脱氢方式和脱氢生成物的结构式以及物质名称填入下表空格中(可填满也可不填满)。
|
可能的脱氢方式 |
脱氢生成物的结构式 |
物质名称 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ⅲ.由上述实验证明,只有 (写结构简式)是液体X。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com