
题目列表(包括答案和解析)
19.(10分)某化学兴趣小组利用废铁屑制取FeCl3·6H2O晶体。主要步骤如下:
①洗净后的废铁屑放在烧杯内,用过量的工业盐酸浸泡至不再产生气泡,过滤。
② 按下图组装仪器,并检查装置的气密性,将①得到的滤液放入试剂瓶B中。
③ 在石墨电极X、Y上连接直流电源,通电,待FeCl2全部被氧化后,断开电源。
 ④ 试剂瓶B中的溶液经过一系列操作,可得FeCl3•6H2O晶体。
④ 试剂瓶B中的溶液经过一系列操作,可得FeCl3•6H2O晶体。
请回答下列问题:
(1)A中的X极应连接电源的 极,
A中发生化学反应的方程式 ;
B中溶液颜色的变化 ,
(2)C烧杯中应该盛放的是 ,其作用是 。
(3)试剂瓶B中的溶液由步骤④制得FeCl3•6H2O晶体,④需要进行的操作依次是(填序号) 。
A.加热浓缩 B.洗涤 、干燥 C.过滤 D.冷却结晶
(4)在整个实验过程中,盐酸必须保持过量,主要原因是 。
18.今有一混合物的水溶液,可能含有以下离子中的若干种:K+、NH 、Cl-、Mg2+、Ba2+、CO
、Cl-、Mg2+、Ba2+、CO 、SO
、SO ,现取三份各100mL溶液进行如下实验:
,现取三份各100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液无沉淀产生,加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量变为2.33g。根据上述实验,下列推测正确的是 ( )
A.一定存在K+和NH B.100mL溶液中含0.01molCO
B.100mL溶液中含0.01molCO
C.Cl-可能存在 D.Ba2+一定不存在,Mg2+可能存在
|
17.将某些化学知识用数轴表示直观形象、简明易记。下列用数轴表示正确的是 ( )
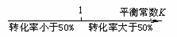
A.平衡常数与转化率关系:
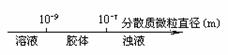
B.分散系的分类与分散质粒直径大小关系:


 C.AlCl3和NaOH反应后铝元素的存在形式与反应物中n(OH-)/n(Al3+)
C.AlCl3和NaOH反应后铝元素的存在形式与反应物中n(OH-)/n(Al3+)

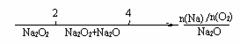 D.Na与O2反应的产物与反应物n(Na)/n(O2)的关系:
D.Na与O2反应的产物与反应物n(Na)/n(O2)的关系:
16.熔融盐燃料电池具有高的发电效率,因而受到重视。用Li2CO3和Na2CO3的熔融盐混合物作电解质,一极通CO气体,另一极通O2和CO2混合气体,可制得在650℃下工作的燃料电池。已知该电池总反应为:2CO+O2 2CO2。则下列说法中正确的是 ( )
A.通CO的一极是电池的正极
B.正极反应式为:2CO+2CO →4CO2+4e-
→4CO2+4e-
C.负极反应式为:O2+2CO2+4e-→2CO
D.该电池工作过程中需不断补充CO和O2,CO2可循环利用
15.常温下,有甲、乙两份体积为1L、浓度均为0.1 mol·L-1的氨水,其pH为11。①甲用蒸馏水稀释100倍后,溶液的pH将为a;②乙与等体积、浓度为0.2 mol·L-1的盐酸混合,在混合溶液中:n(NH )+n(H+)-n(OH-)=bmol。a、b正确的答案组合是 ( )
)+n(H+)-n(OH-)=bmol。a、b正确的答案组合是 ( )
A.9<a<11;0.1 B.9<a<11;0.2 C.12<a<13;0.2 D.13;0.1
14.在一密闭容器中加入A、B、C三种气体,保持一定温度,在t1~t4时刻测得各物质的浓度如右下表。据此判断下列结论正确的是 ( )
|
B.A的转化率比B的转化率低
C.在容器中发生的反应为:
 2A+B 2C
2A+B 2C
D.在t2~t3内A的平均反应速率为:
[1/(t3-t2)]mol·L-1·s-1
13.下列各组物质,前者加入后者时,无论前者是否过量,都能用同一离子方程式表示的是
( )
A.稀盐酸,Na2CO3溶液 B.氯化铝溶液,氨水
C.碳酸氢钠溶液,澄清石灰水 D.溴化亚铁溶液,氯水
12.已知:为使Fe3+、Fe2+、Zn2+较完全的形成氢氧化物沉淀,溶液的pH应分别为3.7、9.6、4.4左右。某硫酸锌酸性溶液中含有少量Fe3+、Fe2+,为除去这些离子制得纯净的硫酸锌,应加入的试剂是 ( )
A.NaOH溶液 B.氨水 C.KMnO4、ZnCO3 D.H2O2、ZnO
11.某探究小组在某温度下测定溶液的pH时发现:0.01mol·L-1的NaOH溶液中,由水电离出的c(H+)·c(OH-)=10-22(mol·L-1)2,则该小组在该温度下测得0.1mol·L-1NaOH溶液的pH应为 ( )
A.13 B.12 C.11 D.10
9.下列离子在溶液中能大量共存,加入(NH4)2Fe(SO4)2·6H2O晶体后,仍能大量共存的是
( )
A.Na+ H+ Cl- NO B.K+ Ba2+ OH- I-
B.K+ Ba2+ OH- I-
C.Na+ Mg2+ Cl- SO D.Cu2+ S2- Br- ClO-
D.Cu2+ S2- Br- ClO-
|
A.四种元素位于同一周期 B.氢化物的稳定性H2Y>HZ
C.离子的氧化性aW3+>bX+ D.a+3=c-2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com