
题目列表(包括答案和解析)
16.下列各组中,两种气体的分子一定相等的
A.温度相同,体积相同的O2和N2 B.压强相同,体积相同的O2和N2
C.体积相等,密度相等的CO和C2H4 D.质量相等,密度不等的C2H4和N2
15.在100 mL某混合溶液中,C(HNO3)=0.4mol/L,C(H2SO4)=0.1mol/L。向其中加入1.92g铜粉,微热,充分反应后溶液中C(Cu2+)为(假设溶液体积不变)
A、0.15 mol/L B、0.3 mol/L C、0.225 mol/L D、无法计算
14. 最近意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构与P4相似,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ热量。根据以上信息和数据,下列说法正确的是
最近意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构与P4相似,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ热量。根据以上信息和数据,下列说法正确的是
A.N4属于一种新型的化合物 B.N4沸点比P4(白磷)高
C.N4与N2互为同素异形体 D.1mol N4气体转变为N2将吸收882kJ热量
13.已知M2O7x-+3S2-+14H+=2M3++3S↓+7H2O,则M2O7x-中的M的化合价为
A.+2 B.+3 C.+4 D.+6
12.下列各溶液中,各离子组一定能大量共存的有
A.含有大量Ba2+的溶液中:HCO3-、Fe3+、Ag+、SO42-、SCN-
B.滴加无色酚酞试液后变红色的溶液中:Na+、CO32-、K+、ClO-、AlO2-
C.由水电离的c(OH-)=10-14mol·L-1 的溶液中:CH3COO-、C6H5O-、Na+、K+
D.加入铝粉后产生氢气的溶液中:NH4+、Na+、NO3-、Cl-、HS-
11、Na2FeO4是一种高效多功能水处理剂,应用前景广阔。一种制备Na2FeO4的方法可用化
学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
对此反应下列说法中不正确的是
A.Na2O2在反应中只作氧化剂
B.O2是氧化产物
C.Na2FeO4既是氧化产物又是还原产物
D.2mol FeSO4发生反应时,共有10mol电子转移
10.从海水中提取镁,可按如下步骤进行:
①把贝壳制成石灰乳; ②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物; ③将沉淀物与盐酸反应,结晶过滤、在HCl气体氛围中干燥产物; ④将得到的产物熔融电解得到镁。下列说法不正确的是
A.第④步电解时阴极产生氯气
B.①②③步骤的目的是从海水中提取MgCl2
C.以上提取镁的过程中涉及化合、分解和复分解反应
D.此法的优点之一是原料来源丰富
9.一定条件下,体积为10L的密闭容器中,1mol X和1mol Y进行反应:
2X(g)+Y(g)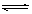 Z(g),经60s达到平衡,生成0.3mol Z。下列说法正确的是
Z(g),经60s达到平衡,生成0.3mol Z。下列说法正确的是
A.若升高温度,X的体积分数增大,则该反应的△H>0
B.将容器体积变为20 L,Z的平衡浓度变为原来的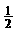
C.以X浓度变化表示的反应速率为0.001mol/(L·S)
D.若增大压强,则物质Y的转化率减小
8.某一密闭容器中盛有饱和Ca(OH)2溶液,当加入少量CaO粉末,反应后恢复到原来温度,下列说法正确的是
①有晶体析出 ②c[Ca(OH)2]增大 ③pH不变 ④c(H+)c(OH-)的积不变 ⑤c(H+)一定增大
A. ①② B. ①③④ C. ①②④ D. ①③⑤
7.将溶质的质量分数为a%、物质的量浓度为C1 mol·L-1的H2SO4溶液蒸发掉一定量的水,使其溶质的质量分数变为2a%,此时物质的量浓度为C2 mol·L-1,则C1和C2的关系是
A. C2>2C1 B. C2=2C1
C. C2<2C1 D. C1=2C2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com