
题目列表(包括答案和解析)
1、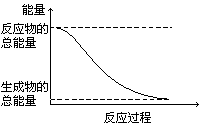 下列变化为放热反应的是
下列变化为放热反应的是
A.H2O(g)=H2O(l) △H=-44.0 kJ/mol
B.2HI(g)=H2(g)+I2(g) △H=+14.9 kJ/mol
C.形成化学键时共放出能量862 kJ的化学反应
D.能量变化如右图所示的化学反应
22.含氮废水进入水体而对环境造成的污染越来越严重,某课外兴趣小组先测定某废水中含NO3-为3×10-4mol/L,而后用金属铝将NO3-还原为N2,从而消除污染。
(1)配平下列有关反应的离子方程式:
NO3-+Al+H2O→N2↑+Al(OH)3↓+OH-
(2)上述反应中,还原剂是________,被还原的元素是___________,每生成2molN2,将有_______mol电子发生转移。
(3)有上述废水100m3,若要完全消除污染,则所耗金属铝的质量为________kg。(需要有过程)
21.(12分)(I)(6分)已知某有机物A的分子式是C2H4,能发生下列转化关系(部分反应物或生成物及反应条件已略去):
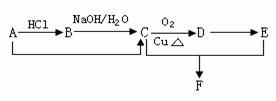
请回答下列问题:
(1)写出下列物质的结构简式:B ,D ;
(2)写出下列反应类型:A→B ,C+E→F ;
(3)写出下列反应的化学方程式:C+E→F
(II)(6分)近年来,乳酸CH3CH(OH)COOH成为人们的研究热点之一。乳酸可以用化学方法合成,也可以由淀粉通过生物发酵法制备。乳酸有许多用途,其中利用乳酸的聚合而合成的高分子材料,具有很好的生物兼容性,它无论在哺乳动物体内或自然环境中,最终都能够降解成为二氧化碳和水。请回答下列有关问题:
(1)乳酸在发生下列变化时所用的试剂是a
,b
;CH3CH(OH)COOH CH3CH(OH)COONa
CH3CH(OH)COONa 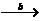 CH3CH(ONa)COONa
CH3CH(ONa)COONa
(2)乳酸的某种同分异构体具有下列性质:能发生银镜反应;1mol该物质能跟金属钠反应产生1molH2。它的结构简式为 。(已知同一个碳原子上不能连接2个羟基)
19.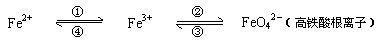 (12分)铁及其化合物的应用十分广泛,亚铁盐、铁盐、高铁酸盐(高铁酸盐只能在强碱性介质中稳定存在)等铁的化合物也在不同的领域中各扮演着重要角色,可用下式表示它们之间的相互转化:
(12分)铁及其化合物的应用十分广泛,亚铁盐、铁盐、高铁酸盐(高铁酸盐只能在强碱性介质中稳定存在)等铁的化合物也在不同的领域中各扮演着重要角色,可用下式表示它们之间的相互转化:
回答下列有关问题:
⑴ Fe与稀硫酸反应可以制取FeSO4,
写出此反应的化学方程式 ,在此反应中,氧化产物是 ;
⑵ 用上述⑴反应所得的酸性溶液,实现上述①、④的转化,要求产物纯净:
要实现①转化可选用的试剂是 ,
A、Cl2 B、H2O2 C、O3 D、KMnO4
要实现④转化,写出反应的离子方程式 ;
⑶ 在强碱性溶液中,用NaClO可实现②转化,若生成1mol FeO42-,则需NaClO mol;
高铁酸盐是一种“绿色环保高效”消毒剂,比含氯消毒剂的性能更为优良。使用高铁酸盐消毒剂,不仅可以消毒杀菌,还能净水,消毒杀菌时发生的转化是③,净水时发生反应的离子方程式为
。20.(6分)已知下列两个热化学方程式:H2(g)+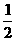 O2(g)=H2O(1); △H=-285.5kJ/mol;C3H8(g)+5O2(g)=3CO2(g)+4H2O(1);△H=-2220.0kJ/mol
O2(g)=H2O(1); △H=-285.5kJ/mol;C3H8(g)+5O2(g)=3CO2(g)+4H2O(1);△H=-2220.0kJ/mol
(1)实验测得H2和C3H8的混合气体共5mol,完全燃烧生成液态水时放热6262.5kJ,则混合气体中H2和C3H8的体积比是 。
(2)已知:H2O(1)=H2O(g);△H=+44.0kJ/mol。写出丙烷燃烧生成CO2和气态水的热化学方程式
18. (8分)某课外研究小组,用含有较多杂质的铜粉,通过不同的化学反应制取胆矾。其设计的实验过程为:

(1)铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧时将瓷坩埚置于
上(用以下所给仪器的编号填入,下同),取用坩埚应使用 ,灼烧后的坩埚应放在石棉网上,不能直接放在桌面上。
实验所用仪器:a 蒸发皿 b 石棉网 c 泥三角d 表面皿 e 坩埚钳 f 试管夹
(2)由粗制氧化铜通过两种途径制取胆矾,与途径Ⅰ相比,途径Ⅱ有明显的两个优点是: 、 ;
(3)在测定所得胆矾(CuSO4·xH2O)中结晶水x值的实验过程中:连续称量的质量相差不超过 为止。
(4)若测定结果x值偏高,可能的原因是
a 加热温度过高 b 胆矾晶体的颗粒较大
c 加热中胆矾晶体溅出 d 胆矾晶体部分风化
17.(6分)今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,确定一定存在的离子是 ;可能存在的离子是 ;一定不存在的离子是 。
16.下列有关实验事故的处理或实验操作的叙述中,正确的是( )
A.浓硫酸不小心沾到皮肤上,立即用稀NaOH溶液洗涤
B.用分液漏斗将甘油和水的混合液体分离
C.若皮肤不慎沾到苯酚,应立即用酒精清洗
D.为了测定某溶液的pH,将未经湿润的pH试纸浸入到待测溶液,过一会取出,与标准比色卡进行对比
15.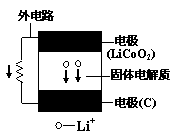 某新型二次锂离子电池结构如右图,电池内部是固体电解质,充电、放电时允许Li+在其间通过(图中电池内部“→”表示放电时Li+的迁移方向)。充电、放电时总反应可表示为:
某新型二次锂离子电池结构如右图,电池内部是固体电解质,充电、放电时允许Li+在其间通过(图中电池内部“→”表示放电时Li+的迁移方向)。充电、放电时总反应可表示为:
LiCoO2+6C  Li1-xCoO2+LixC6
Li1-xCoO2+LixC6
下列说法正确的是( )
A.外电路上的“→”,表示放电时的电流方向
B.充电时阴极反应是:LixC6-xe-=6C+xLi+
C.放电时负极反应是:LiCoO2-xe-=Li1-xCoO2+xLi+
D.外电路有0.1mole-通过,生成锂的质量为0.7g
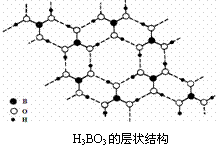
14.正硼酸(H3BO3)是一种类似于石墨的片层状结构的白色晶体,层内的H3BO3分子间通过氢键相连(如右图所示)。下列有关说法正确的是( )
A.正硼酸晶体属于原子晶体
 B.H3BO3分子熔沸点较高
B.H3BO3分子熔沸点较高
C.分子中硼原子最外层为8电子稳定结构
D.含1molH3BO3的晶体中有3mol氢键
13. 以惰性电极电解CuSO4溶液。一段时间后取出电极,加入9.8gCu(OH)2后溶液与电解前相同,则电解时电路中流过的电子为( )
A.0.1mol B.0.2mol C.0.3mol D.0.4mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com