
题目列表(包括答案和解析)
3.关于金属锂的叙述中,错误的是
A.跟水的反应比钠还剧烈
B.它的原子半径比钠的原子半径小
C.它的阳离子的氧化性比钠离子的氧化性强
D.它可作还原剂
2.下列变化需要加入氧化剂才能实现的是
A.S2-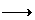 HS- B.HCO
HS- B.HCO
 CO2
CO2
C.I- I2 D.Cu2+
I2 D.Cu2+ Cu
Cu
1.下列物质属于弱电解质的是
A.氯化铝 B.铜 C.酒精 D.水
20.(10分)
今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH4+、Cl-、Mg2+、Fe3+、CO32-、SO42-,现在每次取100.00ml进行实验。
(1)第一份加入AgNO3溶液有沉淀产生。
(2)第二份加足量NaOH后加热,收集到气体0.896L(标准状态下)。
(3)第三份加足量BaCl2后,得干燥沉淀6.27g,沉淀经足量盐酸洗涤干燥后,剩2.33g。试回答有关问题:
①判断Na+、Cl-是否存在?Na+ Cl- (填下列序号)
A.一定存在 B.可能存在 C.一定不存在
②肯定存在的离子在原溶液中的物质的量浓度分别为:
, ,
, 。
19、(9分)(1)2mol/LNaHSO4与1mol/LBa(OH)2溶液等体积混合,反应的离子方程式为 ;若在反应后的溶液中继续滴加Ba(OH)2溶液,写出发生反应的离子方程式 ;
(2)、充分燃烧13 g乙炔气体时生成二氧化碳气体和液态水,并放出热量b kJ,写出乙炔燃烧的热化学方程式:
;
又已知:H2O(g)=H2O(l);△H2=-44.0kJ/mol,则1 mol乙炔燃烧生成二氧化碳气体和气态水放出热量为 。
18、(8分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e→NO+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:
(2)反应中硝酸体现了 、 性质。
(3)反应中若产生2mol气体,则转移电子的物质的量是 mol。
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原
因是 。
17、(1)、(10分)在某工厂在生产维尼纶过程中,先以乙炔和醋酸为原料,通过以下反应制得中间体。

CH≡CH+CH3COOH CH3COOCH=CH2
(i)以上反应类型是 ,中间体名称是 。
(ii)写出中间体通过碳碳双键由小分子变成大分子的反应方程式
。
(iii)将中间体和稀碱溶液共热,可蒸馏出一种有机物甲的水溶液,含2.2g甲的溶液进行银镜反应可得10.8g银,则甲的结构简式为 。请写出该反应的化学方程式
。
(2)(15分)已知:

下列有机化合物A~H有如图的转化关系:

化合物D的分子式为C10H10O,其苯环上的一氯代物只有两种;F的分子式为C10H9OBr。请回答下列问题:
(i)写出下列化合物的结构简式:
A : I:
(ii)反应①的反应类型为 ,反应②的条件为 。
(iii)反应③的化学方程式为:
(iv)化合物D有多种同分异构体,其中属于酚类,结构中除苯环外无其他环且苯环上只有两种互为对位的取代基的同分异构体有 种(不考虑两双键直接相连)。请写出其中两种的结构简式
、 。
16.用类推的方法可能会得出错误结论,因此类推出的结论要经过实践的检验才能确定其正确与否。下列类推结论中正确的是:( )
A.Mg失火不能用CO2灭火,Na失火也不能用CO2灭火
B.工业上电解熔融MgCl2制取金属镁,工业上也用电解熔融AlCl3的方法制取金属铝
C.Al与S直接化合可以得到A12S3,Fe与S直接化合也可以得到Fe2S3
D.Fe3O4可以写成FeO·Fe2O3,Pb3O4也可写成PbO·Pb2O3
草 稿 纸
II卷
15.向2mL0.5mol/L的FeCl3溶液中加入3 mL5mol/L的KF溶液,发现FeCl3溶液渐渐褪至无色,再加入KI溶液和CCl4振荡后,静置,不见CCl4层有紫红色,则下列说法正确的是( )
A.Fe3+不与I-发生反应 B.Fe3+与F-结合成不与I-反应的物质
C.F-使I-的还原性减弱
D.Fe3+被F-还原为Fe2+ ,使溶液中不再存在Fe3+
14.下列叙述中正确的是( )
A.相同条件下,N2和O3混合气与等体积的N2所含原子数相等
B.等物质的量的甲基(-CH3)和羟基(-OH)所含电子数相等
C.常温常压下28 g CO与22.4 L O2所含分子数相等
D.16g CH4与18 g NH4+ 所含质子数相等
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com