
题目列表(包括答案和解析)
6.在一定条件下,将钠与氧气反应的生成物1.5 g溶于水,所得溶液恰好能被 80 mL浓度为0.50 mol/L的HCl溶液中和,则该生成物的成分是( )
(A)Na2O (B)Na2O2 (C)Na2O和Na2O2 (D)Na2O2和NaO2
|
Al2O3 + N2 + 3 C === 2 AlN + 3 CO 下列叙述正确的是( )
A.在氮化铝合成反应中,N2是还原剂,Al2O3是氧化剂
B.氮化铝晶体属于分子晶体 C.氮化铝中氮元素化合价为-3
D.上述反应中每生成2 mol AlN,N2得到3 mol电子
5.某溶液中含有的溶质是FeBr2、FeI2,若向该溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的KSCN溶液,结果溶液变为血红色,则下列叙述正确的是: ( )
① 原溶液中的Br-一定被氧化②通入氯气后原溶液中的Fe2+一定被氧化
③不能确定通入氯气后的溶液中是否存在Fe2+
④若取少量所得溶液,加入CCl4,静置,向上层溶液中加入足量的AgNO3溶液,只产生白色沉淀,说明原溶液中的I-、Fe2+、Br-均被完全氧化
A.①②③ B.②③④ C.①③④ D.①②③④
4.许多国家十分重视海水资源的综合利用。不需要化学变化就能够从海水中获得的物质是 ( )
(A)氯、溴、碘 (B)钠、镁、铝 (C)烧碱、氢气 (D)食盐、淡水
3.下列说法正确的是 ( )
A.含有离子键的化合物一定是离子化合物 B.共价化合物中只含有极性键
C.含有共价键的化合物一定是共价化合物 D.非极性键只存在于单质分子中
2.通过分析周期表结构和各元素性质的变化趋势,判断砹(原子序数为85)及其化合物的叙述正确的是 ( )
A.由KAt的水溶液制备At的化学方程式为2KAt + Cl2 == 2KCl +At2
B.相同条件下,HAt比HI难分解
C.AgAt是一种易溶于水的固体
D.At在第五周期VIIA族
1、若发现位于元素周期表第七横行. 第十七纵行列的元素的一种原子,该原子的质量数为280,则该原子核内的中子数为 ( )
A,163 B,164 C,165 D,166
27.(8分)在NaOH、Na2CO3混合液中加入盐酸,若NaOH、Na2CO3、HCl物质的量分别是x、y、z。
(1)计算反应后溶液中NaCl物质的量(A)。
(2)已知Na2CO3跟HCl按下式反应:
Na2CO3+HCl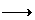 NaHCO3+NaCl
NaHCO3+NaCl
NaHCO3+HCl NaCl+H2CO3
NaCl+H2CO3
计算反应后溶液中CO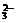 的物质的量?(B)?。
的物质的量?(B)?。
26.(8分)化工厂经常用浓氨水检验管道是否漏氯气,其反应为3Cl2+8NH3====6NH4Cl+N2。当有160.5 g NH4Cl产生时,求被氧化的氨气是多少克?
25.(10分)无水氯化铝是白色晶体,易吸收水分,在178℃升华,装有无水氯化铝露置于潮湿空气中会爆炸并产生大量白雾,工业上由金属与氯气作用或由无水氯化氢气体与熔融Al作用而制得,某课外活动小组在实验室内通过下列装置(如下图)制取少量纯净的无水氯化铝。 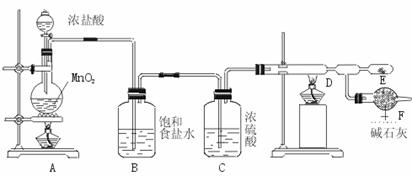
(1)开始实验时,不能先点燃A装置的酒精灯后打开分液漏斗的活塞,将浓盐酸注入烧瓶内,其理由是 。
(2)A装置发生反应的化学方程式: 。
(3)在E处可收集到纯净的氯化铝,原因是 。
(4)若无B、C装置,使A产生的气体直接进入D,实验产生的不良后果是 。
(5)F装置的作用是 。
24.(6分)用37%,密度为1.19 g·cm-3的浓盐酸配制0.1 mol·L-1的稀盐酸500 mL,请回答:
(1)所需浓盐酸的体积为 mL;
(2)此实验配制稀盐酸,除玻璃棒、胶头滴管、试剂瓶外,还需的仪器有 、__________和 。
(3)如果在配制时,第一次加水量太少,搅拌时间较长,对配制溶液的浓度有什么影响?
(“偏高”“偏低”或“无影响“)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com