
题目列表(包括答案和解析)
21.(16分)(1)(4分)
①________________ ;②_______________;
③________________ ;④_______________________________;
(2)(12分)
①______ ____ ,____________。②_____________。
③____________________________________________ 。
④_____ , 。
20.(8分) ⑴ 。 ⑵ 。
⑶ 。
19.(18分)
⑴.氯化铜 醋酸
⑵.① ②
③ . .
⑶. ,
⑷. , ; ; 。
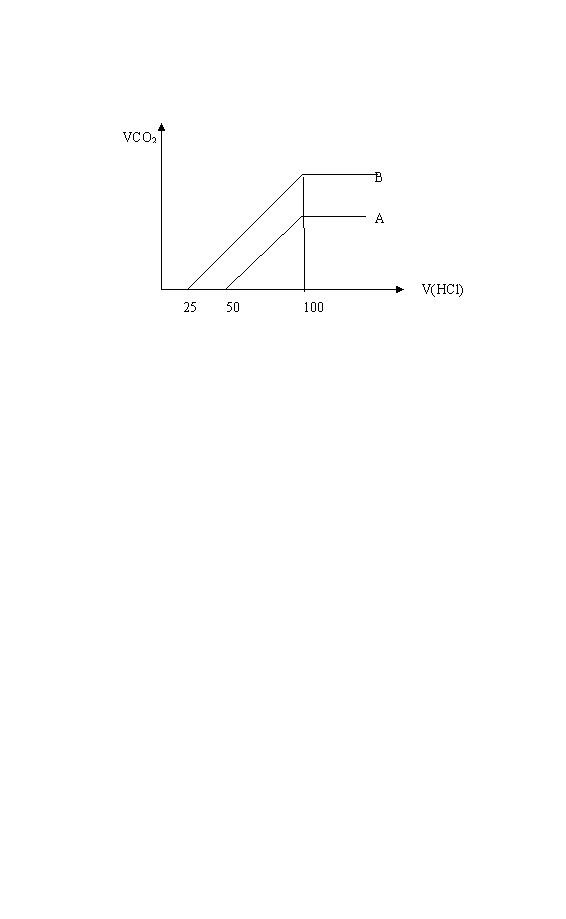
22.(16分)取等物质的浓度NaOH溶液两份A和B,每份20ml,向其中各通入一定量的CO2,然后分别将其稀释为100ml ,分别向稀释后的溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生CO2气体体积与所加盐酸的关系如下图所示
(1)曲线A表明,原溶液中通入CO2后,所得溶液中的溶质为(写化学式) ,加入盐酸后产生CO2体积的最大值 ml,滴入盐酸的过程中发生反应的离子方程式 、
。
(2)曲线B 表明,原溶液中通入CO2后,所得溶液中的溶质为(写化学式) ,两溶质物质的量之比为 ;加入盐酸后产生CO2体积的最大值为 ml。
(3)求原NaOH溶液物质的量的浓度 mol· L-1

 徐水一中高三月考 化学答卷纸
徐水一中高三月考 化学答卷纸
Ⅱ卷(共56分)
21.(16分)(1)(4分) 进行下面的实验,必须用到下述何种仪器,将正确的仪器名称填入空白处
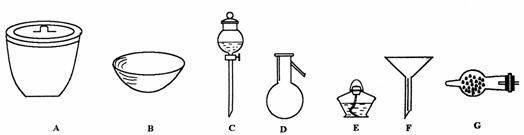
①欲干燥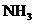 需使用仪器________________;
需使用仪器________________;
②欲分离互不相溶的两种液态物质,须使用________________;
③欲分离液态混合物中沸点不同的组分,须使用________________;
④欲分离浮于液体中的固体物质,须使用________________________________;
(2)(12分)实验室用固体烧碱配制500mL 0.1mol·L-1的NaOH溶液。
①需称量______ ____ g的烧碱固体,固体应放在____________中称量。
②配制过程中,不需要使用的仪器是(填符号)_____________。
A烧杯 B量筒 C玻璃棒 D1000mL容量瓶 E漏斗
③根据实验的实际需要和②中列出的仪器判断,完成实验还缺少的仪器
是____________________________________________ (填仪器名称)。
④ⅰ如果没有用蒸馏水洗涤烧杯、玻璃棒,配成的溶液的物质的量浓度比要求的_____ (填“偏高”或“偏低” );ⅱ有位同学在定容时不小心多加了水使液面高于刻度线,于是他用胶头滴管吸出过多的上层溶液。这样将会使配得的溶液的物质的量浓度 (填“偏高”、“偏低”或“无影响” )。
20.(6分)某无色溶液,由Na+、Ag+、Ba2+、Al3+、、、、中的若干种组成。取该溶液进行如下实验:
(A)取适量试液,加入过量盐酸,有气体生成,并得到溶液;
(B)在(A)所得溶液中再加入过量碳酸氢铵溶液,有气体生成,同时析出白色沉淀甲;
(C)在(B)所得溶液中加入过量Ba(OH)2溶液,也有气体生成,并有白色沉淀乙析出。
根据上述实验回答下列问题:
⑴ 溶液中一定不存在的离子是 。
⑵ 一定存在的离子是 。
⑶ 判断沉淀乙成份的方法是 。
19.(18分)按要求写出下列方程式
⑴.(2分)写出下列物质在水溶液中的电离方程式
氯化铜
醋酸
⑵.(8分)写出下列反应的离子方程式
①硫酸铜溶液与氢氧化钠溶液混合
②碳酸钠溶液与稀盐酸混合
③边微热边向铵明矾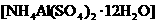 溶液中逐滴加入
溶液中逐滴加入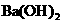 溶液至中性.此时发生反应的离子方程式为______________ .
溶液至中性.此时发生反应的离子方程式为______________ .
向以上所得中性溶液中继续滴加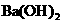 溶液,这一步离子反应的离子方程式是______________.
溶液,这一步离子反应的离子方程式是______________.
⑶.(4分)写出符合离子方程式Ba2++SO42- =BaSO4↓的两个化学方程式
,
⑷.(4分)在反应KClO3+6HCl==3Cl2+KCl+3H2O中,KClO3被 ,是 剂;Cl2是 产物 ,被氧化和被还原的氯元素的物质的量之比为 。
18.两种金属粉末的混合物2g,与足量稀硫酸反应,生成0.1gH2,则这种混合物的可能组成是
A.Fe、Mg B.Mg、Al C.Fe、Zn D.Fe、Cu
Ⅱ卷(共56分)
17.同温同压下,某容器充满氧气时质量为116 g,若充满二氧化碳时质量为122g ,充满某气体时质量为114 g,则该气体的相对分子质量为
A、28 B、34 C、32 D、44
16.在MgCl2、KCl、K2SO4三种盐的混合溶液中,若K+、Cl-各为1.5mol,Mg2+为0.5mol,则SO42-的物质的量为
A.0.1mol B.0.5mol C.0.15mol D.0.25mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com