
题目列表(包括答案和解析)
6.科学研究发现,用10B合成的10B20有较好的抗癌作用,下列说法中正确的是
A.10B和10B20互为同位素
B.10B20和10B互为同素异形体
C.10B和10B20互为同分异构体
D.10B的中子数与核外电子数相等
29.有机物A1和A2含有碳、氢、氧三种元素,且互为同分异构体。巳知6gA1在足量的氧气中完全燃烧生成13.2g二氧化碳和7.2g水。有关物质之间的转化关系如下:
已知:X为六元环状化合物

(1)A1的分子式为
(2)写出下列物质的结构简式:
A2 X
(3)书写化学方程式:反应④ ;
反应①属于 反应,反应②属于 反应
(4)与G具有相同官能团的G的同分异构体M在酸性条件下,加热失水生成N,N的甲酯可以发生加聚反应生成聚合物P,写出M→N的化学方程式:
聚合物P的结构简式为:
 (1)C3H8O(2分)
(1)C3H8O(2分)
(2)A2:CH3CHOHCH3(2分) X: (2分)
(3)④:CH3CH2CHO + 2 Ag(NH3)2OH  2Ag↓+ CH3CH2COONH4
+3NH3 + H2O (3分)
2Ag↓+ CH3CH2COONH4
+3NH3 + H2O (3分)
①:消去(1分) ②:加成 (1分)
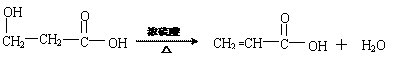 (4)
(4)

|
(2分)
28.回答下列问题:
⑴ 常温下将体积为v1、浓度为c1的一元弱酸与体积为v2、浓度为c2的一元弱碱混合。若v1·c1=v2·c2,混合后的溶液pH<7,则一元弱酸的电离程度 (选填“大于”、“小于”或“等于”)一元弱碱的电离程度;
 ⑵ 对于一定条件下体积可变的密闭容器中已达平衡的可逆反应:
⑵ 对于一定条件下体积可变的密闭容器中已达平衡的可逆反应:
A(g)+3B(g)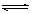 2C(g);ΔH<0
2C(g);ΔH<0
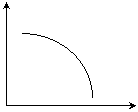
若其他条件不变,只改变右图中横坐标所表示的物理量,纵坐标所表示的
物理量变化如右图所示:
① 若横坐标表示温度,则纵坐标可以表示 、 、
(至少填两个含义不同的物理量);
② 若横坐标表示压强,则纵坐标 (填“能”或“不能”)表示平衡混合物的密度,理由是:
。
⑴ 大于 (3分)
⑵ ① C的物质的量或百分含量、A或B的转化率、平衡混合物的平均相对分子质量(4分,每空2分)
② 不能 (2分) P增大,则容器体积减小,但混合气体的质量不变,故平衡混合物的密度增大(每空3分)
27.已知:A、B、E为固体化合物;D、G为固体单质;F、X、Z为可燃性气体,F、X燃烧的火焰呈蓝色或淡蓝色。在一定条件下它们能实现如图所示的变化。

(1)写出A、B、Z、的名称。A_________,B________,E____________。
(2)G跟氢氧化钠溶液反应生成气体X和溶液,写出Y跟这种溶液所发生反应的类型______________________。
(3)写出G和氢氧化钠溶液反应的化学方程式:___________________________________________________。
(4)写出1molZ跟1molHCl反应的化学方程式:____________________________________________________。
(1)二氧化硅、氧化钙、碳化钙。(2)复分解反应。
(3)Si+2NaOH+2H2O=Na2SiO3+2H2+H2O。
(4)HC≡CH+HCl CH2=CHCl。
CH2=CHCl。
26.A、B、C、D四种短周期元素的原子半径依次减小,在周期表中B与A、C相邻,C的最外层电子数是其电子总数的3/4,D能分别与A、B、C形成电子总数相符的化合物X、Y、Z。试回答:
(1)在X、Y、Z三种化合物中稳定性由强到弱的顺序是(用化学式表示,下同) ,Z的电子式是 。
(2)常温下8gX完全燃烧生成液态水和CO2,放出热量akJ,写出表示X燃烧热的热化学方程式:
。
(3)将Y溶于水所得溶液与适量AlCl3溶液反应,其离子方程式是 。
(4)若由A、B、C、D四种元素组成一种离子化合物,1mol该化合物中含有10mol原子,则该化合物受热分解的化学方程式为 。
(5)Y跟HCl反应生成固体。该固体跟有毒的工业盐NaNO2的水溶液混合加热,NaNO2被完全破坏,当有1molNaNO2发生反应时,共有3mol电子转移,该反应的化学方程式 。
(1)H2O、NH3、CH4(2分) Z的电子式略H:C:H (2分)
(2)CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-2aKJ/mol(3分)
|
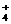 (3分)
(3分)
|
(5)NaNO2+NH4Cl NaCl+N2↑+2H2O(3分
13.在一定的条件下,当64gSO2气体被氧化成SO3气体时,共放出热量98.3KJ。已知SO2在此条件下转化率为80%,据此,下列热化学方程式正确的是( )
A.SO2(g)+1/202(g) 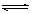 SO3(g );△H=-98.3KJ·mol-1
SO3(g );△H=-98.3KJ·mol-1
B.2SO2(g)+02(g) 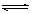 SO3(1 );△H=-196.6KJ·mol-1
SO3(1 );△H=-196.6KJ·mol-1
C.SO2(g)+1/202(g) 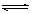 SO3(g );△H=-78.64KJ·mol-1
SO3(g );△H=-78.64KJ·mol-1
D.2SO2(g)+02(g) 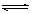 SO3(g );△H=+196.6KJ·mol-1
SO3(g );△H=+196.6KJ·mol-1
12.用已知物质的量浓度的NaOH溶液滴定未知物质的量浓度的盐酸溶液时,用甲基橙做指示剂,下列实验操作会引起测量结果偏高的是( )
①酸式滴定管使用前,水洗后未用待测盐酸润洗;
②锥形瓶水洗后未干燥
③碱式滴定管用蒸馏水洗后,未用标准液洗
④读取滴定管终点读数时,俯视刻度线
⑤配制好的NaOH溶液保存不当,部分与空气中的CO2反应生成了Na2CO3
A.③ B.②⑤ C.③⑤ D.③④⑤
11.常温下,下列各组离子在指定的环境中不能大量共存,且一定会放出无色气体的是( )
A.遇pH试纸变红色的溶液中:K+、Cl-、NO-3、NH+4
B.在c(H+)/c(OH-)=1×1012的溶液中:I-、Cl-、HCO-3、Na+
C.在c(H+)=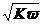 的溶液中:Na+、S2-、NO-3、CO2-3
的溶液中:Na+、S2-、NO-3、CO2-3
D.由水电离出的c(H+)=1×10-12mol·L-1的溶液中:NH+4、Fe2+、SO42-、Cl-
10.下列各溶液中,微粒的物质的量浓度关系正确的是( )
A.0.1mol/L的(NH4)2SO4溶液中,c(SO42-)>c(NH4+)>c(H+)>c(OH-)
B.25℃时,pH=7的氨水和硫酸铵的混和溶液中,c(NH4+)=c(SO42-)
C.0.1mol/L的Na2CO3溶液与0.05mol/L的盐酸等体积混合后的溶液中,
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
D.c(NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4Cl溶液c[(NH4)2CO3]<[(NH4)2SO4]<c(NH4Cl)
9.X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6。下列说法正确的是( )
A.Y、Z两元素形成的简单阴离子的还原性Z>Y
B.原子半径大小的顺序为W>X>Y>Z
C.X与W形成的化合物W2X2中含有离子键和共价键
D.Y、Z两种元素最高价氧化物的水化物的酸性Z>Y
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com