
题目列表(包括答案和解析)
31.Na2S2O3·5H2O(俗称海波)是照相业常用的一种定影剂。工业上制得的Na2S2O3·5H2O晶体中可能含有少量的Na2SO3和Na2SO4杂质。为了测定某海波样品的成分,称取三份质量不同的该样品,分别加入相同浓度的硫酸溶液30mL,充分反应后滤出硫,微热滤液使生成的SO2全部逸出。(Na2S2O3+H2SO4→Na2SO4+SO2↑+S↓+H2O)
(1)测得有关实验数据如下(标准状况):
|
|
第一份 |
第二份 |
第三份 |
|
样品的质量/g |
7.54 |
15.08 |
35.00 |
|
二氧化硫的体积/L |
0.672 |
1.344 |
2.688 |
|
硫的质量/g |
0.8 |
1.6 |
3.2 |
(摩尔质量:Na2S2O3·5H2O 248g/mol ;Na2SO3 126g/mol;Na2SO4 142 g/mol)
计算所用硫酸溶液的物质的量浓度。
(2)分析以上实验数据,该样品中(填写选项字母) 。
A 仅含有Na2S2O3·5H2O
B 含有和Na2S2O3·5H2O和Na2SO3,无Na2SO4
C 含有Na2S2O3·5H2O、Na2SO3和Na2SO4
(3)若将30.16g该样品和一定量的上述硫酸溶液混合微热。试讨论:当加入硫酸的体积(aL)在不同取值范围时,生成的SO2体积(bL)的值(可用含a的关系式表示)。
30.取3.40g只含羟基,不含其他官能团的液态饱和多元醇,置于5.00L氧气中,经点燃,醇完全燃烧。反应后气体体积减少0.56L,将气体经CaO吸收,体积又减少2.80L(所有体积均在标准状况下测定)。
(1) 3.40g醇中,C 、H、 O物质的量分别为:
C mol,H _____mol,O mol;该醇中C、H、O的原子数之比为 。
(2)由以上比值能否确定该醇的分子式,其原因是 。
(3) 如果将该多元醇的任意一个羟基换成卤素原子,所得到的卤代物都只有一种,试写出
该饱和多元醇的结构简式: 。
29、 生产工程塑料PBT( )的重要原料G(1,4-丁二醇),可以通过下图三种不同的合成路线制备。又知B的所有原子处于同一平面。
生产工程塑料PBT( )的重要原料G(1,4-丁二醇),可以通过下图三种不同的合成路线制备。又知B的所有原子处于同一平面。
请你结合下列所给有关信息,回答问题。
Ⅰ.CH2=CH-CH=CH2与Br2的CCl4溶液发生1∶1加成可得到BrCH2-CH=CH-CH2Br和BrCH2-CHBr-CH=CH2二种产物。
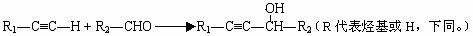
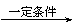 Ⅱ.2R-Cl+2Na
R-R+2NaCl
Ⅱ.2R-Cl+2Na
R-R+2NaCl
Ⅲ.
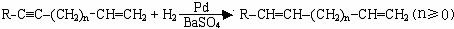 Ⅳ.
Ⅳ.
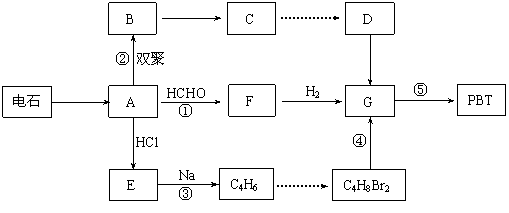
⑴写出E和F的结构简式: 、 。
⑵写出反应⑤的化学反应方程式: 。
⑶请你设计出由B→C…→D的反应流程图(有机物用结构简式表示,必须注明反应条件)。
 提示:①合成过程中无机试剂任选 ②反应流程图表示方法示例如下:
提示:①合成过程中无机试剂任选 ②反应流程图表示方法示例如下:

 B C
…… G
B C
…… G
28.(1)烷烃分子中的基团可能有四种:一CH3、一CH2、一CH、一C一,其数目分别用a、b、c、d表示,对烷烃(除甲烷外)中存在的关系作讨论:
①下列说法正确的是:
A. a的数目与b的数目没有因果联系。 B. c增加1,a就会增加3
C. d增加1,a就会增加2 D. b增加1, a就会增加2
②若某烷烃分子中, b=c=d=1,则满足此条件的该分子的结构可能有 种,写出其中一种的名称 _________________________________ 。
 (2) 某烃的组成为C15H24,分子结构非常对称。有关实验证实该烃中仅存在三种基团:乙烯基(-CH=CH2)、亚甲基(-CH2-)、次甲基(-CH-),并且乙烯基和次甲基之间必须通过亚甲基相连,相同基团之间不相连。
(2) 某烃的组成为C15H24,分子结构非常对称。有关实验证实该烃中仅存在三种基团:乙烯基(-CH=CH2)、亚甲基(-CH2-)、次甲基(-CH-),并且乙烯基和次甲基之间必须通过亚甲基相连,相同基团之间不相连。
试填写:
① 该烃分子中无环,则含乙烯基__________个,
该烃的结构简式为__________ 。
②若该烃分子中有一个环,则其结构简式为___________。
27.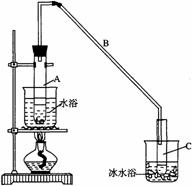 某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
已知: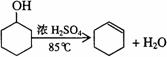
|
|
密度
(g/cm3) |
熔点
(℃) |
沸点
(℃) |
溶解性 |
|
环己醇 |
0.96 |
25 |
161 |
能溶于水 |
|
环己烯 |
0.81 |
-103 |
83 |
难溶于水 |
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是__________,导管B除了导气外还具有的作用是__________。
②试管C置于冰水浴中的目的是___________________________________________。
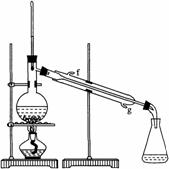 (2)制备精品
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_________层(填上或下),分液后用_________(填入编号)洗涤。
A KMnO4溶液 B 稀H2SO4 C Na2CO3溶液
②再将环己烯按右图装置蒸馏,冷却水从________口进入。蒸馏时要加入生石灰,目的是__________________。
③收集产品时,控制的温度应在_________左右,实验制得的环己烯精品质量低于理论产量,可能的原因是( )
A 蒸馏时从70℃开始收集产品 B 环己醇实际用量多了
C 制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是_________。
A 用酸性高锰酸钾溶液 B 用金属钠 C 测定沸点
25.下表是元素周期表的一部分,表中所列字母分别代表一种元素。
|
a |
|
|
|||||||||||||||
|
|
|
|
|
b |
c |
d |
e |
|
|||||||||
|
f |
|
g |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
h |
i |
回答下列问题:
(1)以上指定元素形成的单质中,熔点最低的是________(填化学式);
(2)由a、c、d三种元素形成的化合物中,能促进水电离的是________(填其中一种物质的化学式),能抑制水电离的是_________(填其中一种物质的化学式)。
(3)e元素位于周期表中第____周期____族。b、c、d、e、h元素的氢化物中,热稳定性最大的是_____(填氢化物的化学式)。
(4)f、g元素的单质共5.0 g在100 mL水中完全反应,生成的溶液中只含有一种溶质分步写出发生反应的化学方程式:
① ____ ___ ②
所得溶液的物质的最大浓度为 mol/L。(液体的体积变化忽略不汁)
24.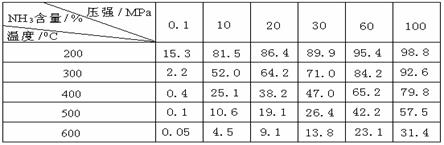 工业合成氨时将N2和H2按体积比为1 :3通入合成塔中,在不同条件下达到平衡时,混合物中NH3的含量(体积分数)如下表:
工业合成氨时将N2和H2按体积比为1 :3通入合成塔中,在不同条件下达到平衡时,混合物中NH3的含量(体积分数)如下表:
(1)根据表中数据并应用化学平衡移动原理,分析为提高平衡混合物中NH3的含量,可采取的措施是 (多选或选错均不给分)
A.增大压强 B.减小压强 C.提高温度 D.降低温度
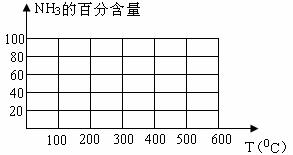 (2)根据表中数据,画出在30MPa下,
(2)根据表中数据,画出在30MPa下,
NH3的百分含量随温度的变化曲线图。
在实际生产中,控制温度在500℃左右,其原因是
。
(3)在500℃、30 MPa条件下反应达到平衡时H2的转化率为 ;若在某条件下平衡混合物中NH3的百分含量为a%,原混合气体与平衡混合气体的总物质的量之比__________(用含a的代数式表示)。
23.在氯酸钾的分解反应里,二氧化锰的催化问题到目前还没有肯定的解释。鉴于制得的氧气中有氯气的气味,生成的氯化钾又略显紫红色,认为反应过程如下:
Ⅰ:2KClO3+2MnO2→2A+B↑+C↑ Ⅱ:2A→D+MnO2+C↑
Ⅲ:B+D→2KCl+MnO2+O2↑
根据催化剂定义,反应前后化学性质和质量不变。回答下列问题:
(1) B气体化学式为___________,A固体化学式为________________。
(2) I式反应被氧化的元素为___________________。
(3) 反应Ⅲ的化学方程式为 。
(4) 按照上述反应过程,若生成1.5molO2,总共有 mol电子发生转移。
22.环己醇、丙酮(CH3COCH3)和戊醛(CH3CH2CH2CH2CHO)的混合物2.000g完全燃烧后,所得气体通过P2O5吸收瓶,吸收瓶增重1.998g,则混合物的平均分子量为
A.74.75 B.86.00 C.71.75 D.81.33
第II卷(共66分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com