
题目列表(包括答案和解析)
18.(12分)测定含I-浓度很小的碘化物溶液时,利用振荡反应进行化学放大,可以准确求出原溶液中I-的浓度。主要步骤如是:
①取100mL样品溶液,用单质溴将样品中的I-氧化成IO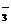 ,将过量的溴除去。
,将过量的溴除去。
②再加入过量的KI,并用硫酸酸化,使IO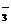 完全转化成I2。
完全转化成I2。
③将②中生成的碘完全萃取后,用肼将其还原成I-。
④将生成的I-萃取到水层后,用步骤①的方法再处理转化为IO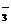 。
。
⑤将④得到的溶液加入适量的KI溶液,并用硫酸酸化,使IO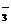 完全转化成I2。
完全转化成I2。
⑥将⑤得到的溶液完全转入250mL容量瓶,并加水稀释至刻度。
⑦分别取⑥得到的溶液25.00mL于锥形瓶中,加入指示剂,用0.1010mol/L 的Na2S2O3标准溶液滴定(2Na2S2O3+I2=Na2S4O6+2NaI)。
⑧重复操作⑦两次。
根据上述步骤回答下列问题:
⑴在操作①中,除去过量溴单质的方法是 。
⑵请写出操作②中发生的反应的离子方程式 。
⑶在萃取操作中,使用的玻璃仪器有 。步骤⑦使用的指示剂是 ;判断滴定达到终点的现象为 。
⑷下表是该实验的记录结果:
|
滴定 次数 |
待测溶液的体积 |
标准溶液的体积 |
|
|
滴定前刻度/mL |
滴定后刻度/mL |
||
|
1 |
25.00 |
1.02 |
21.05 |
|
2 |
25.00 |
2.00 |
21.99 |
|
3 |
25.00 |
0.11 |
20.09 |
原溶液中I-的物质的量浓度为 。
17.(10分)某化学兴趣小组在做实验时,将AgNO3溶液和KI溶液混合,发现有黄色沉淀生成,振荡后迅速消失。大家经查阅资料后,发现可能的原因是发生了下列反应:AgI+I- [AgI2]-。
[AgI2]-。
⑴甲同学设计了两个简单的实验方案来进行验证,请你协助他完成实验。
实验1:向浓KI溶液中滴加AgNO3溶液,现象为 。
实验2:向AgNO3溶液中滴加稀KI溶液,有黄色沉淀生成;再
。
⑵乙同学在实验所得的溶液中滴加硝酸溶液,结果又出现了沉淀。请解释出现沉淀的原因 。
⑶丙同学在实验所得的溶液中滴加氯水也可以看到沉淀,但由于溶液为黄色,分不清沉淀的颜色。大家通过查阅数据,分析认为产生的沉淀不可能是AgCl,所查阅的数据是 ;请设计简单的实验说明不会产生AgCl沉淀: 。
16.世界上60%的镁是从海水中提取的,其主要步骤如下:
①把贝壳制成石灰乳;②在海水中加入石灰乳,过滤,洗涤沉淀物;③将沉淀物与盐酸反应,结晶、过滤;④在氯化氢热气流中干燥晶体;⑤电解上述晶体的熔融物。
下列说法正确的是
A.镁元素在元素周期表中位于第三周期、ⅡA族
B.向洗涤液中滴加碳酸钠溶液可检验沉淀是否洗涤干净
C.在氯化氢热气流中干燥晶体的目的是加快干燥速度
D.步骤⑤也可以采用电解该晶体水溶液的方法
第二卷(非选择题 共72分)
15.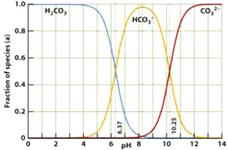 下图是一水溶液在pH从0至14的范围内,H2CO3、HCO
下图是一水溶液在pH从0至14的范围内,H2CO3、HCO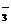 、CO
、CO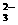 三种成分平衡时的组成百分率,下列叙述正确的是
三种成分平衡时的组成百分率,下列叙述正确的是
A.此图是1.0mol/L碳酸钠溶液滴定1.0 mol/L
HCl溶液的滴定曲线
B.在pH为6.37及10.25时,溶液中
c(H2CO3)= c(HCO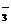 )= c(CO
)= c(CO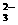 )
)
C.人体血液的pH约为7.4,则CO2在血液中多以HCO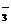 的形式存在
的形式存在
D.若用CO2和NaOH反应制取Na2CO3,溶液的pH必须控制在12以上
14.下列溶液中各微粒的浓度关系正确的是
A.物质的量浓度相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中c(NH4+):
c[(NH4)2SO4] > c(NH4HSO4) > c(NH4Cl)
B.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:
c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C.某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-)
D.1.0mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3)
13.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,其与水的离子反应是:
4FeO42-+10H2O=4Fe(OH)3(胶体)+3O2↑+8OH-。工业上先制得Na2FeO4,然后在低温下,向Na2FeO4溶液中加入一定量KOH,可制得K2FeO4。下列说法中不正确的是
A.K2FeO4溶液有丁达尔效应 B.K2FeO4溶液具有吸附性
C.K2FeO4溶液能除去氧化性杂质 D.上述制得K2FeO4的反应为复分解反应
12.下列有关化学事实或现象的解释正确的是
A.合金在潮湿的空气中形成原电池,故其耐腐蚀性都较差
B.氯化钠溶于水也有化学过程,是因为离子键发生了断裂
C.升高温度反应速率加快,原因是活化分子百分数增加
D.铝的金属性较强,所以铝制容器在空气中容易被腐蚀
11.下列离子方程式书写正确的是
A.用氨水溶解氯化银沉淀:Ag++2 NH3·H2O=[Ag(NH3)2]++2 H2O
B.向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全:
Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3·H2O+ H2O
C.硫酸亚铁溶液与稀硫酸、双氧水混合:2Fe2++H2O2 +2H+=2Fe3++2H2O
D.向次氯酸钠溶液中通入足量SO2气体:ClO-+ SO2+ H2O = HClO+ HSO3-
10.下列各组离子可能大量共存的是
A.pH=1的溶液中:Fe2+、Al3+、HCO3-、MnO4-
B.能与金属铝反应放出氢气的溶液:K+、NO3-、Cl-、NH4+
C.含有大量OH-的无色溶液中:Na+、Cu2+、AlO2-、SiO32-
D.常温下水电离出的c(H+)·c(OH-)=10-20的溶液中:Na+、C1-、S2-、SO32-
9.阿伏加德罗常数约为6.02×1023mol-1。下列叙述中正确的是
A.32g含有少量臭氧的氧气中,共含有氧原子1.204×1024
B.在标准状况下,2.24L己烷中所分子数约为6.02×1023
C.12.5 mL 16 mol/L浓硫酸与足量铜反应,生成SO2的分子数约为6.02×1022
D.2.7g铝与足量氢氧化钠溶液反应转移的电子数约为1.806×1023
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com