
题目列表(包括答案和解析)
2、设NA代表阿伏加德罗常数,下列说法不正确的是 ( )
A.5.6 g铁与足量硝酸反应转移的电子数为0.3NA
B.100 mL 2.0 mol/L的盐酸与醋酸溶液中氢离子数均为0.2NA
C.标准状况下,22.4 L氦气与22.4 L氟气所含分子数均为NA
D.18 g水中含有的电子数为10NA
1、水的沸点是100℃,硫化氢的分子结构跟水相似,但它的沸点却很低,是-60.7℃,引起这种差异的主要原因是 ( )
A.范德华力 B.共价键 C.氢键 D.相对分子质量
1.某研究性学习小组为了证明在同温同压下,相同浓度相同体积的酸性强弱不同的一元酸与足量镁带反应的速率不同,但是产生的氢气的体积相同,在下图装置的锥形瓶中分别装入1mol•L-1的盐酸和醋酸各10mL,进行实验。
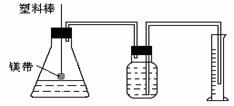
⑴分别称取除去表面氧化膜的镁带ag,并系于塑料棒的末端。则a的数值至少为 g。
⑵除了上图装置中出现的实验仪器和用品外,本实验还需用到的仪器和用品有:天平、100mL量筒、剪刀、胶头滴管、 和 。
⑶在广口瓶中装足量水,按图连好装置后,要 (填操作名称)。
⑷将塑料棒向下移动,使镁条全部浸入酸中,至酸反应完成。
为了比较反应速率和产生氢气的体积,应记录的实验数据为 。
实验结果表明:镁带和盐酸的反应速率比镁带和醋酸的反应速率 (填“快”或“慢”),理由是 。
⑸下列情况中可能导致反应速率变快的是 (填序号,多填扣除分,下同);可能导致产生氢气的体积减少的是 。A.镁带中含有少量跟酸不反应的杂质
B.没有除去镁带表面的氧化膜 C.镁带中含有少量的杂质铁
(12分)⑴0.12(2分)⑵砂纸、计时器(2分)⑶检查装置的气密性(1分)
⑷反应开始至气泡停止冒出的时间(1分),排入量筒水的体积(1分),快(1分),同浓度的盐酸比醋酸溶液中的H+浓度大(1分)⑸AC(2分,漏选得1分,多选0分),B(1分)
2.某研究性学习小组为了证明在同温同压下,相同浓度相同体积的酸性强弱不同的一元酸与足量镁带反应的速率不同,但是产生的氢气的体积相同,在下图装置的锥形瓶中分别装入1mol•L-1的盐酸和醋酸各10mL,进行实验。
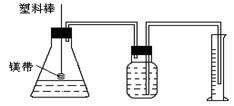
⑴分别称取除去表面氧化膜的镁带ag,并系于塑料棒的末端。则a的数值至少为 g。
⑵除了上图装置中出现的实验仪器和用品外,本实验还需用到的仪器和用品有:天平、100mL量筒、剪刀、胶头滴管、 和 。
⑶在广口瓶中装足量水,按图连好装置后,要 (填操作名称)。
⑷将塑料棒向下移动,使镁条全部浸入酸中,至酸反应完成。
为了比较反应速率和产生氢气的体积,应记录的实验数据为 。
实验结果表明:镁带和盐酸的反应速率比镁带和醋酸的反应速率 (填“快”或“慢”),理由是 。
⑸下列情况中可能导致反应速率变快的是 (填序号,多填扣除分,下同);可能导致产生氢气的体积减少的是 。A.镁带中含有少量跟酸不反应的杂质
B.没有除去镁带表面的氧化膜 C.镁带中含有少量的杂质铁
(12分)⑴0.12(2分)⑵砂纸、计时器(2分)⑶检查装置的气密性(1分)
⑷反应开始至气泡停止冒出的时间(1分),排入量筒水的体积(1分),快(1分),同浓度的盐酸比醋酸溶液中的H+浓度大(1分)⑸AC(2分,漏选得1分,多选0分),B(1分)
1.(5分)下列实验设计或操作合理的是(多选倒扣分)_____________。
a.中和热测定实验时,如果没有环形玻璃棒,可用环形铜质搅拌棒代替。
b.实验室制取乙烯时必须将温度计的水银球插入反应液中,测定反应液的温度。
c.在250mL烧杯中,加入216mL水和24g NaOH固体,配制10% NaOH溶液
d.向Na2CO3与NaOH的混合溶液中加入足量的CaCl2溶液,再滴加几滴酚酞试液,可检验NaOH的存在。
e.使用水银温度计测量烧杯中水浴温度时,不慎打破水银球,用滴管将水银吸出放入水封的小瓶中,残破的温度计插入装有硫粉的广口瓶中
f.用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物;
bde(多选、少选一个扣2分,扣完为止)
25、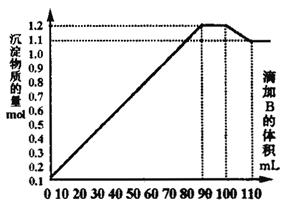 (10分)向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH
(10分)向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH
的混合溶液B,产生的沉淀总物质的量和加入溶液B的体积关系如右图所示:
(1)当加入B溶液110 mL时,溶液中的沉淀是__________________(填化学式)。
(2)溶液B中Na2SO4与NaOH的物质的量浓度之比____________;从90 mL至100 mL之间加入10 mL B溶液时所发生的离子反应方程式是_________ 。
(3)将A、B溶液中各溶质的物质的量浓度填入下表:
|
溶质 |
Na2SO4 |
NaOH |
BaCl2 |
AlCl3 |
FeCl3 |
浓度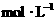 |
|
|
|
|
|
24、(5分)一定质量的氧化镁和氧化钙的混合物刚好与10倍质量的盐酸完全反应,试求盐酸中溶质的质量分数。
23、(10分)已知单质铁溶于-定浓度的硝酸溶液中反应的离子方程式为:aFe+bNO3-+cH+
=dFe2++fFe3++gNO↑+hN2O↑+kH2O(化学计量数a-k均为正整数)。回答下列问题:
(1)根据反应中氮、氢、氧三种元素的原子个数守恒,可得c、g、h的关系式是(用-个代数式表示。下同) 。
(2)根据反应中离子的电荷守恒,可得b、c、d、f的关系式是 。
(3)根据反应中电子转移的总数相等,可得d、f、g、h的关系式是 。
(4)若a=12,且铁和稀硝酸恰好完全反应,则b的取值范围是 ;
c的取值范围是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com