
题目列表(包括答案和解析)
6.对可逆反应4NH3(g)+5O2(g)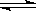 4NO(g)+6H2O(g),下列叙述正确的是 (
)
4NO(g)+6H2O(g),下列叙述正确的是 (
)
A.达到化学平衡时,5v正(O2)=4v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,平衡混合物中各物质的浓度相等
D.若容器的总压强不随时间而变化,则反应达到平衡状态
5.在2A+B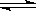 3C+4D反应中,表示该反应速率最快的是 ( )
3C+4D反应中,表示该反应速率最快的是 ( )
A.vA=0.5mol/(L·min) B.vB=0.01mol/(L·s)
C.vC=0.8mol/(L·min) D.vD=1mol/(L·min)
4.R、W、X、Y、Z为原子序数依次递增的同一短周期元素,下列说法一定正确的是
(m、n均为正整数) ( )
A.若R(OH)m为强碱,则W(OH)n也为强碱 B.若HXOm为强酸,则Y是活泼非金属元素 C.若Y的最低化合价为-2,则Z的最高正化合价为+6 D.若X的最高正化合价为+5,则五种元素都是非金属元素
3.有两种短周期元素X和Y可组成化合物XY3,当Y的原子序数为m时,X的原子序数可能为:①m-4;②m+4;③m+8;④m-2;⑤m+6 ( )
A.①②③④⑤ B.①②④⑤ C.①②⑤ D.①③④
2.已知1-18号元素的离子aW3+、bX+、cY2-、dZ- 都具有相同的电子层结构,下列关系正确的是 ( )
A.质子数c>b B.离子的还原性Y2-> Z-、
C.氢化物的稳定性H2Y>HZ D.原子半径X<W
1.居室装修用石材的放射性常用 作为标准,居里夫人(Marie Curie)因对Ra元素的研究两度获得诺贝尔奖。下列叙述中正确的是
( )
作为标准,居里夫人(Marie Curie)因对Ra元素的研究两度获得诺贝尔奖。下列叙述中正确的是
( )
A.RaCl2的熔点比CaCl2高
B.Ra元素位于元素周期表中第六周期ⅡA族
C.一个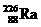 原子中含有138个中子
原子中含有138个中子
D.Ra(OH)2是一种两性氢氧化物
14. (16分)苏丹红一号(sudanⅠ)是一种偶氮染料,不能作为食品添加剂使用。它是由苯胺和2-萘酚为主要原料制备的,它们的结构简式如下所示:

(1)苏丹红-号的化学式(分子式)为
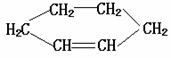
 (2)在下面化合物(A)-(D)中,与2-萘酚互为同分异构体的有(填字母代号)
(2)在下面化合物(A)-(D)中,与2-萘酚互为同分异构体的有(填字母代号)
 (提示:
可表示为 )
(提示:
可表示为 )
A B C D
(3)上述化合物(C)含有的官能团是
(4)在适当的条件下,2-萘酚经反应可得到芳香化合物E(C8H6O4),1mol E与适量的碳酸氢钠溶液反应可放出二氧化碳44.8L(标准状况),E与溴在有催化剂存在时反应只能生成两种-溴取代物,两种一溴取代物的结构简式分别是
E与碳酸氢钠反应的化学方程式是
(5)若将E与足量乙醇在浓硫酸作用下加热,可以生成一个化学式(分子式)为C12H14O4的新化合物,该反应的化学方程式是
反应类型是 。
13.(20分)用如图装置进行实验,将A逐滴加入B中:
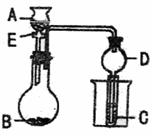
(1)若A为浓硫酸,B为第三周期金属元素的片状单质,其在常温下难与水反应,但在加热时可与水反应,C为品红溶液,实验中观察到溶液褪色,则B是 (写化学式),根据题意写出B与浓H2SO4的化学方程式: ;反应后往烧杯中加入沸水,又可观察到试管C中的现象为 。
(2)若B为Na2CO3,C为C6H5ONa溶液,实验中观察到小试管内溶液变浑浊,则酸A
应具有的性质是 ,25℃时等物质的量浓度的B、C两溶液pH大的是 (填化学式);然后往烧杯中加入沸水,可观察到试管C中的现象是 。
(3)若B是生石灰,实验中观察到C溶液先形成沉淀,然后沉淀溶解,当溶液恰好澄清时,关闭E,然后往烧杯中加入热水,静置片刻,观察到试管壁出现光亮的银镜,
则A是 (写名称),C是 (写化学式)与乙醛的混合液,写出银镜反应的离子方程式 ,仪器D在此实验中的作用是 。
12.(12分)为防止碘缺乏病,,通常在食盐中加入KIO3。
⑴用淀粉碘化钾溶液和稀硫酸可定性检验出食盐中的IO3-,其原理是食盐中的IO3- 与KI溶液发生反应生成的碘单质使淀粉变蓝。表示该反应的离子方程式是:_______________________________ ______ ;
若要确认食盐中还含有K+,具体的方法是________________________________________。
⑵工业上以石墨和铁为电极电解KI溶液制取KIO3。电解时,石墨作_________(填“阳极”或“阴极”),石墨电极上的电极反应式是_________________ __________ _,电解过程中铁电极附近溶液pH__________(填“变大”、“变小”或“不变”)。
11、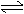 (10分)在10℃和200KPa的条件下,反应aA(g) dD(g)+ eE(g)建立平衡后,再逐步增大体系的压强(温度维持不变),下表列出不同压强下反应建立平衡时物质D的浓度:
(10分)在10℃和200KPa的条件下,反应aA(g) dD(g)+ eE(g)建立平衡后,再逐步增大体系的压强(温度维持不变),下表列出不同压强下反应建立平衡时物质D的浓度:
|
压强/ Pa |
200KPa |
500KPa |
1000KPa |
|
D的浓度/mol·L-1 |
0.085 |
0.20 |
0.44 |
根据表中数据,回答下列问题:
(1)压强从200KPa增大到500KPa时,平衡向 反应方向移动(填“正”或“逆”),其理由是 。
(2)压强从500KPa增加到1000KPa,平衡向 反应方向移动(填“正”或“逆”),其理由是 。平衡之所以向该方向移动,这是由于 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com