
题目列表(包括答案和解析)
7. 在氯化钠晶体晶胞中,与每个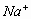 距离最近且等距的几个
距离最近且等距的几个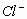 所围成的空间构型为
所围成的空间构型为
A. 正四面体形 B. 正八面体形
C. 正六面体形 D. 三角锥形
6. 一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是
一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是
A.NaCl是非电解质
B.NaCl溶液是电解质
C.NaCl在水溶液中电离出了可以自由移动的离子
D.NaCl溶液中水电离出大量的离子
5.常温下单质硫主要以S8形式存在。加热时,S8会转化为S6、S4、S2等。当温度达到
750℃时,硫蒸气主要以S2形式存在(占92%)。下列说法中正确的是
A.S8转化为S6、S4、S2属于物理变化
B.不论哪种硫分子,完全燃烧时都生成SO2
C.常温条件下单质硫为原子晶体
D.把硫单质在空气中加热到750℃即得S2
4.下列叙述正确的是
A.稀有气体原子序数越大,熔点越低
B.同周期元素的原子半径越小,气态氢化物还原性越弱
C.晶体中分子间作用力越强,分子越稳定 D.同主族金属的原子半径越大,熔点越高
3.科学家最近发现两种粒子:第1种是只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”;第2种是由四个氧原子构成的分子。下列有关这两种粒子的说法不正确的是
A.“四中子”不显电性 B.“四中子”的质量数为4
C.第2种粒子是氧元素的另一种同位素 D.第2种粒子的化学式为O4
2.含11.2gKOH的稀溶液与1L0.12mol/L的H2SO4 溶液反应放出11.46kJ的热量。该反应的热化学方程式是
A.KOH(aq)+1/2H2SO4 (aq)=1/2K2SO4(aq)+H2O (1) △H= -11.46kJ/mol
B.2KOH(aq)+H2SO4 (aq)=K2SO4(aq)+2H2O (g) △H= 一114.6kJ/mol
C.2KOH(aq)+H2SO4 (aq) =K2SO4(aq)+2H2O (1) △H= +114.6kJ/mol
D.KOH(aq)+1/2H2SO4 (aq)=1/2K2SO4(aq)+H2O (1) △H= 一57.3kJ/mol
1.用右图表示的一些物质或概念间的从属关系中不正确的是
|
|
X |
Y |
Z |
|
例 |
苯的同系物 |
芳香烃 |
芳香族化合物 |
|
A |
氧化物 |
化合物 |
 纯净物 纯净物 |
|
B |
胶体 |
分散系 |
混合物 |
|
C |
电解质 |
离子化合物 |
化合物 |
|
D |
碱性氧化物 |
金属氧化物 |
氧化物 |
26、某工厂排出的废水中含有金属Ba2+,为了测定其浓度,作如下实验:
①称取K2Cr2O7固体0.1323g溶于适量的稀硫酸中,再向其中加入过量KI,反应后用Na2S2O3 溶液与之反应,当用去27.00mL时恰好完全反应。
②另取废水50.00mL,控制适当的酸度加入足量的K2Cr2O7溶液,得BaCrO4沉淀,沉淀经洗涤、过滤后,用适量的稀盐酸溶解,此时 CrO42- 转化为 Cr2O72-,再加过量KI反应,反应液再同上述Na2S2O3 溶液反应,反应完全时,消耗Na2S2O3 溶液24.00mL,已知有关的离子方程式为:
_____Cr2O72-+____I-+______H+=______Cr3++_____I2+____ ______
I2+2S2O32-=2I-+S4O62-
(1)配平上述方程式。
(2)Na2S2O3 溶液的浓度为__________。
(3)求废水中Ba2+的物质的量浓度是多少?
25、 已知:有机物A是一种镇痛解热药品,其结构简式为:

(1)B、D的关系是 (填序号)。
a.互为同位素 b.互为同系物 c.互为同分异构体 d.同类物质
(2)写出②③反应的化学方程式,注明反应类型
反应② ; 。
反应③ ; 。
(3)能与FeCl3溶液发生显色反应的属于酯类的C的同分异构体有 种。
24、A为日常调味品之一,K胶体经过处理可用作干燥剂,F为白色腊状固体,B为无色无
味液体。请回答下列问题:
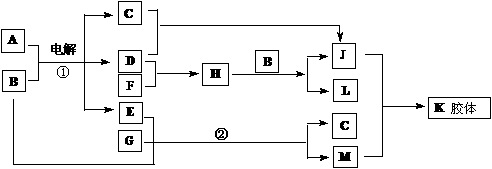
(1)写出下列物质化学式:
A:________; D:________;E:________;
(2)判断晶体A、F、G的熔点高低(用化学式表示)________>_________>______
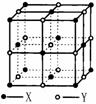 (3)晶体A由两种微粒构成,其晶体结构如图所示,
(3)晶体A由两种微粒构成,其晶体结构如图所示,
相邻最近异种微粒间距为a cm,晶体A的密度为
ρ g/cm3,则用相关数据表达阿伏加德罗常数
NA=__________________。
(4)写出反应②的离子方程式________________。
(5)铁锅与A的溶液接触时容易生锈,可以用方程式表示其原因:
①负极反应:______________正极反应:_______________
② Fe2++2OH-=Fe(OH)2
③__________________________________________________
④ 2Fe(OH)3 + (x-3)H2O==Fe2O3·xH2O(铁锈)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com