
题目列表(包括答案和解析)
3. 同温同压下,当反应物分解了8%时,总体积也增加8%的是( )

 A.2NH3(g) ? N2(g)+3H2(g)
B.2NO(g) ? N2(g)+O2(g)
A.2NH3(g) ? N2(g)+3H2(g)
B.2NO(g) ? N2(g)+O2(g)

 C.2NO3(g)? 4NO2(g)+O2(g) D.2NO2(g)
? 2NO(g)+O2(g)
C.2NO3(g)? 4NO2(g)+O2(g) D.2NO2(g)
? 2NO(g)+O2(g)
2.下列混合物的分离和提纯方法中,主要不是从物质的溶解性角度考虑的是( )
A.过滤 B.蒸馏 C.结晶 D.萃取
1、对危险化学品要在包装标签上印有警示性标志。氢氧化钠溶液应选用的
标志是( )




A.爆炸品 B 氧化剂 C 剧毒品 D腐蚀品
28.(18分)U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性,U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
(1)V的单质分子的结构式为 ;XW的电子式为 ;Z元素在周期表中的位置是 。
(2)U元素形成的同素异形体的晶体类型可能是(填序号) 。
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
(3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式) ;U、W的氢化物分子结合H+能力较强的是(写化学式) ,用一个离子方程式加以证
明 。
(4)YW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW有关反应的离子方程式为 。
由此可知VW和YW2还原性较强的是(写化学式) 。
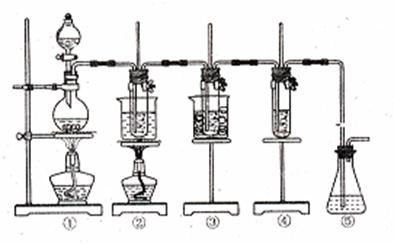 29.(12)在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
29.(12)在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
图中:①为氯气发生装置;②的试管里盛有15mL30%KOH溶液,并置于水浴中;③的试管里盛有15mL8%NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。 请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过 (填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有 (填写下列编号字母)的净化装置。
A.碱石灰 B.饱和食盐水
C.浓硫酸 D.饱和碳酸氢钠溶液
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是
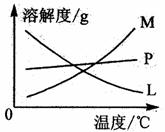
反应完毕生经冷却后,②的试管中有大量晶体析出。下图中符合该晶体溶解曲线的是 (填写编号字母);从②的试管中分离出该晶体的方法是
(填写实验操作名称)
(3)本实验中制取次氯酸钠的离子方程式是 。
(4)实验中可观察到④的试管里的溶液的颜色发生了如下变化,请填写下表中的空白:
|
实验现象 |
原因 |
|
溶液最初从紫色逐渐变为 色 |
氯气与水反应生成的H+使石蕊变色 |
|
随后溶液逐渐变为无色 |
|
|
然后溶液从无色逐渐变为
色 |
|
27.(12)在一定条件下,下列各物质可发生如图所示的变化(反应中生成的水没有写出)
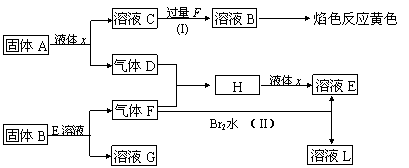
请回答:(1)固体A是(写化学式) 。
(2)反应(I)的化学方程式 。
(3)反应(II)的化学方程式 。
26.(18分)请填写下列空白:
(1)现用物质的量的浓度为amol/L的标准盐酸去测定VmLNaOH溶液的物质的量浓度;
①酸式滴定管用蒸馏水洗净后,还应该进行的操作是______________。
②下图2是酸式滴定管中液面在滴定前后的读数:
 |
|||||
 |
|||||
|
|||||
c (NaOH) = _______________________________________。
③若在滴定前滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失,则测定的NaOH物质的量浓度会偏_______ ____。
(2)图3是中学化学实验中的一种常用装置,若要在仅盛有少量水的水槽的条件下
检查其气密性(不得使用任何导管、橡皮管,且不得拔下橡皮塞等),其操作方
法和现象是 。
(3)①用已准确称量的1.06gNa2CO3固体配制0.100mol·L-1 Na2CO3溶液100mL,所需要的仪器为 。
②除去KCl溶液中的SO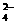 ,依次加入的试剂为(填溶质的化学式) 。
,依次加入的试剂为(填溶质的化学式) 。
13.已知:2H2(g)+O2(g)=2H2O(l):△H=-571.6kJ/mol
H2(g)+ O2(g)=H2O(g);△H=-241.8kJ/mol
O2(g)=H2O(g);△H=-241.8kJ/mol
则氢气的燃烧热为( )
A.241.8kJ/mol B.-241.8kJ/mol
C.285.8kJ/mol D.571.6kJ/mol
12.使用容量瓶配制溶液时,由于操作不当,会引起误差,下列情况会使所配溶液浓度偏低的是 ( )
①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了
②用滴定管量取液体时,开始时平视读数,结束时俯视读数
③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
④转移溶液前容量瓶内有少量蒸馏水 ⑤定容时,仰视容量瓶的刻度线
⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
A.①③⑤⑥ B.①②⑤⑥ C.②③④⑥ D.③④⑤⑥
11.在下列比较中,正确的是 ( )
A.受热稳定性:HI>HBr>HCl>HF B.碱性:NaOH>Al(OH3)>Mg(OH)2
C.微粒半径:F-<Na+<Mg2+ D.单质的熔点:Li >Na>K>Rb
10.用相同质量的金属钠进行下列实验,产生氢气最多的是( )
A.将钠投入到足量的盐酸中 B.将钠投入到足量的乙醇中
C.将钠用铝箔包好,并刺有小孔,投入足量的水中
D.将钠投入足量硫酸铜溶液中
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com