
题目列表(包括答案和解析)
25.(8分) a单质及其化合物在一定条件下可发生如右图所示的
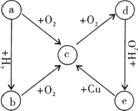 变化,五种物质中都含有同一种元素。
变化,五种物质中都含有同一种元素。
(1)若a常温下是一种固体,则a是 ,c是 。
e→c的化学方程式为 。
(2)若a常温下是一种气体,则a是 ,d是 。
e→c的离子方程式为 。
24.(11分)有A、B、C、D、E、F六种元素,原子序数依次增大,位于不同的三个短周期,其中B与D可形成DB2、DB3化合物,在同周期元素中,C的金属性最强,E的非金属性最强;请回答:
(1)写出A、C、E三种元素的名称
A. C. E.
(2)A、B形成的化合物与DB2反应生成一种强酸的化学方程式为:
(3)已知DB2在一定条件下可转化为DB3,1mol DB2充分反应,放出98.3kJ的热量。该反应的热化学方程式是
(4)用铂作电极电解由C、E形成化合物的饱和溶液时,一段时间后,将阳极产物和阴极溶液混合,反应的离子方程式是 。若改用铁棒做阳极材料,则阳极的电极反应式为: 。
23.某合金(仅含铜、铁)中铜和铁的物质的量之和为ymol,其中Cu的物质的量分数为a ,将其全部投入50mLbmol·L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物)。下列说法正确的是
A.若金属有剩余,在溶液中再滴入硫酸后,金属不会溶解
B.若金属全部溶解,则溶液中一定含有Fe3+
C.若金属全部溶解,且产生336mL气体(标准状况),则b=0.3
D.当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b≥80y(1-a/3)
22.有BaCl2和NaCl的混合溶液aL,将它均分成两份。一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴加AgNO3溶液,使Cl-离子完全沉淀。反应中消耗xmol H2SO4、ymol AgNO3。据此得知原混合溶液中的c(Na+)/ mol·L-1为
A.(y-2x)/a B.(y-x)/a C.(2y-2x)/a D.(2y-4x)/a
21.将5.4g Al投入200.0mL 1.0mol∙L-1 的某溶液中放出氢气,充分反应后无固体物质剩余。该溶液可能为
A.HNO3溶液 B.Ba(OH)2溶液 C.H2SO4溶液 D.HCl溶液
20.医疗上颇为流行的“理疗特效垫”,就是利用铁缓慢氧化放出的热均匀、稳定,使患处保持温热状态。56g铁粉被完全氧化,需消耗氧气的质量为
A.16g B.21g C.24g D.32g
19.20℃时,KCl的溶解度为34g,若忽略固体溶解引起的溶液体积变化,则在该温度下,所配KCl溶液的物质的量浓度不可能是
A.5mol/L B.4mol/L C.3mol/L D.2mol/L
18、在某澄清、透明的浅黄色溶液中,可能含有下列八种离子:H+、NH4+、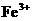 、Ba2+、Al3+、SO42-、HCO3-、I-,在检验方案设计时初步分析其溶液中最多可含离子(不包括K+和OH-)有
、Ba2+、Al3+、SO42-、HCO3-、I-,在检验方案设计时初步分析其溶液中最多可含离子(不包括K+和OH-)有
A、4种 B、5种 C、6种 D、7种
17.常温下,测得某氨水溶液的pH 约为12,将其与0.01 mol/L的盐酸等体积混合后,所得溶液中物质的量浓度最大的离子是
A. Cl- B. NH4+ C. H+ D. OH-
16. 已知NaHSO3溶液呈酸性、NaHCO3溶液呈碱性。现有浓度均为0.1 mol/L的NaHSO3溶液和NaHCO3溶液,溶液中各粒子的物质的量浓度存在下列关系(R表示S或C),其中一定正确的是
A.c(Na+)>c(HRO3-)>c(H+)>c(RO32-)>c(OH-)
B.c(Na+)+c(H+)=c(HRO3-)+c(RO32-)+c(OH-)
C.c(H+)+c(H2RO3)=c(RO32-)+c(OH-)
D.两溶液中c(Na+)、c(HRO3-)、c(RO32-)分别相等
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com