
题目列表(包括答案和解析)
18.碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌锰碱性电池以KOH为电解质,电池总反应式为: Zn+2MnO2+2H2O= 2MnOOH+Zn(OH)2。下列说法错误的是
A.电池工作时,锌失去电子
B.电池正极的电极反应式为:MnO2+H2O+e-= MnOOH+OH-
C.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g
D.锌锰碱性电池是二次电池,所以性能比普通锌锰电池好
17.天津是我国研发和生产锂离子电池的重要基地。锂离子电池正极材料是含锂的二氧化钴(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。电池反应为LiCoO2+C6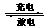 CoO2+LiC6,下列说法正确的是
CoO2+LiC6,下列说法正确的是
A.充电时,电池的负极反应为LiC6-e- = Li++C6
B.放电时,电池的正极反应为CoO2+Li++e- = LiCoO2
C.羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质
D.锂离子电池的比能量(单位质量释放的能量)低
16.已知:(1)Zn(s)+1/2O2(g)= ZnO(s) ΔH= -348.3kJ/mol
(2)2Ag(s)+1/2 O2(g)= Ag2O(s) ΔH= -31.0kJ/mol,则Zn(s)+ Ag2O(s)= ZnO(s)+ 2Ag(s)的ΔH等于
A.-317.3kJ/mol B.-379.3kJ/mol C.-332.8 kJ/mol D.317.3 kJ/mol
15.下列反应的离子方程式正确的是
A.次氯酸钙溶液中通入少量CO2:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO
B.硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2H2O2+4H+=Fe3++4H2O
C.碳酸氢钠溶液与足量的氢氧化钡溶液混合:Ba2++2OH-+2HCO3-=BaCO3↓+CO32-+2H2O
D.硝酸铁溶液中加过量氨水:Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+
14.500 mL KNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是
A.原混合溶液中c(K+)为2 mol·L-1
B.上述电解过程中共转移4 mol电子
C.电解得到的Cu的物质的量为0.5 mol
D.电解后溶液中c(H+)为2 mol·L-1
13.向1.00 L 0.3 mol/L的NaOH溶液中缓慢通入CO2气体至溶液增重8.8g,所得溶液中,下列说法正确的是
A.溶质为Na2CO3
B.溶质为Na2CO3、NaHCO3
C. c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
D.c(Na+)=c(HCO3-)+2c(CO32-)+c(OH-)-c(H +)
12.事实上,许多非金属氧化物在一定条件下能与Na2O2反应,且反应极有规律。如:Na2O2+SO2 = Na2SO4、Na2O2+SO3 = Na2SO4+ O2,据此,你认为下列方程式中不正确的是
A.2Na2O2+2Mn2O7=4NaMnO4+O2↑ B.2Na2O2+P2O3=Na4P2O7
C.2Na2O2+2 N2O3=4NaNO2+O2↑ D.2 Na2O2+2 N2O5 =4NaNO3+O2↑
11.“拟晶”(quasicrystal)是一种具有凸多面体规则外形但不同于晶体的固态物质。A165Cu23Fel2是二十世纪发现的几百种拟晶之一,具有合金的某些优良物理性能。有关这种拟晶的说法错误的是
A.A165Cu23Fel2的硬度比金属A1、Cu、Fe都大
B.A165Cu23Fel2中三种金属的化合价均可视作零;
C.A165Cu23Fel2不可用作长期浸泡在海水中的材料
D.1mol A165Cu23Fel2溶于过量的稀硝酸时共失去265 mol电子
10.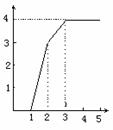 某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度(纵坐标/mol·L-1)和加入铁粉的物质的量(横坐标/mol)之间的关系如图所示。则溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为:
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度(纵坐标/mol·L-1)和加入铁粉的物质的量(横坐标/mol)之间的关系如图所示。则溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为:
 A.1∶1∶1
A.1∶1∶1
B.1∶3∶1
C.3∶3∶8
D.1∶1∶4
9.下列各组物质的溶液,前一种溶液逐滴滴入后一种溶液中,与后一种溶液逐滴滴入前一种溶液中产生的现象相同的是
①Ba(OH)2和稀H3PO4 ②HNO3和NaAlO2 ③NaOH和AlCl3 ④Ca(HCO3)2和Ba(OH)2 ⑤Na2CO3和HCl ⑥AgNO3和NH3·H2O ⑦NaHCO3和HCl
A.①⑤ B.②④ C.⑤⑦ D.④⑦
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com