
题目列表(包括答案和解析)
3.把分别盛有熔融的氯化钾、氯化镁、氯化铝的三个电解槽串联,在一定条件下通电一段时间后,析出钾、镁、铝的物质的量之比为( )
A.1:2:3 B.3:2:1 C.6:3:1 D.6:3:2
2.(2007年高考全国理综卷I)已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4 = 2CuI↓+13I2+12K2SO4+12H2O
其中1 mol氧化剂在反应中得到的电子为( )
(A)10 mol (B)11 mol (C)12 mol (D)13 mol
1.(2007年高考全国理综卷II)下列氧化还原反应中,水作为氧化剂的是( )
(A)CO+H2O CO2+H2
(B)3NO2+H2O = 2HNO3+NO
CO2+H2
(B)3NO2+H2O = 2HNO3+NO
(C)2Na2O2+2H2O = 4NaOH+O2↑ (D)2F2+2H2O = 4HF+O2
化合物KxFe(C2O4)y· zH2O是一种重要的光化学试剂,其中铁为+3价。分别称取该样品0.49lg两份,其中一份在110℃干燥脱水,至质量恒定为0.437g。另一份置于锥形瓶中,加入足量的3 mol·L-1 H2SO4和适量的蒸馏水,加热至75℃,趁热加入0.0500mol·L-1KMnO4溶液24.0mL,恰好完全反应;再向溶液中加入适量的某种还原剂,将Fe3-完全转化为Fe2+,该溶液中Fe2+刚好与4.0 mL0.0500mol·L-1KMnO4溶液完全反应。
通过计算,分别求:(1)0.49lg样品中结晶水的物质的量。
(2)化合物中草酸根的质量分数。
(3)化合物的化学式。
己知:2 KMnO4 + 5 H2C2O4 + 3H2SO4 = 2MnSO4 + K2SO4 + 10CO2↑+ 8H2O
MnO4- +5Fe2++8H+=Mn2+ + 5Fe3+ + 4H2O
6.(8分实验室为监测空气中汞蒸气的含量;往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为:4CuI+Hg→Cu2HgI4+2Cu
(1)上述反应产物Cu2HgI4中,Cu元素显 价。
(2)以上反应中的氧化剂为 ,当有1molCuI参与反应时,转移电子 mol。
(3)CuI可由Cu2+与I-直接反应制得,请配平下列反应的离子方程式。
Cu2++ I-→ CuI+ I3-
5.(8分)(1)1985年,化学上第一次用非电解法制得氟气,试配平该反应的化学方程式:
[ ]K2MnF6+[ ]SbF5 →[ ]KSbF6+[ ]MnF3+[ ]F2↑
反应中_______元素被还原。
(2)氰(CN)2、硫氰(SCN)2的化学性质和卤素(X2)很相似,化学称为拟卤素如:
(SCN)2+H2O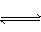 HSCN+HSCNO
它们阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-。
试写出:
①(CN)2与KOH溶液反应的化学方程式:_______
②NaBr和KSCN混合溶液中加入(CN)2,反应的离子方程式:_______
HSCN+HSCNO
它们阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-。
试写出:
①(CN)2与KOH溶液反应的化学方程式:_______
②NaBr和KSCN混合溶液中加入(CN)2,反应的离子方程式:_______
4.(6分)下列物质: ⑴Na⑵ Br2 ⑶Na2O ⑷NO2 ⑸CO2 ⑹ SO3 ⑺NH3 ⑻H2S ⑼HCl ⑽ H2SO4 ⑾Ba(OH)2 ⑿NaCl ⒀蔗糖 ⒁NaCl溶液。其中属于电解质的是 , 属于非电解质的是 ,能导电的是 。
3.(8分)过氧化氢H2O2,(氧的化合价为-1价),俗名双氧水,医疗上
利用它有杀菌消毒作用来清洗伤口。对于下列A~D涉及H2O2的反应,填写空白:
A.Na2O2 +2HCl= 2NaCl+H2O2 B.Ag2O+ H2O2=2Ag+O2+ H2O
C.2 H2O2=2 H2O+O2 D.3 H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8 H2O
(1)H2O2仅体现氧化性的反应是(填代号) 。
(2)H2O2既体现氧化性又体现还原性的反应是(填代号) 。
(3)H2O2体现酸性的反应是(填代号) 。
(4)上述反应说明H2O2、Ag2O、K2CrO4氧化性由强到弱的顺序是: 。
2. (6分) 已知H+(aq)+OH-(aq)=H2O(l) △ H=-57.3kJ/mol ,回答下列问题。
(1)用20gNaOH配稀溶液跟足量稀盐酸反应放出____________ kJ的热量。
(2)用2molH2SO4配稀溶液跟足量稀NaOH反应,此反应的中和热为
(3)如果将(1)中和反应中稀盐酸换成稀醋酸时,反应放出的热量 (1)放出的热量(填大于、小于、等于)
1. (8分) 煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳。然后是使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的化学方程式为:
a.C(s)+ O2(g) = CO2(g) △H=E1 ①
b.C(s) + H2O(g) = CO(g)+ H2(g) △H=E2 ②
H2(g)+ 1/2 O2(g) = H2O(g) △H=E3 ③
CO(g)+ 1/2 O2(g) = CO2(g) △H=E4 ④
回答:
⑴与途径a相比途径b有较多的优点,即______ _____ _______________________________________________________________________。
⑵上述四个热化学方程式中哪个反应△H >0?________________
⑶等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是( )
A、a比b多 B、a比b少 C、a与b在理论上相同
⑷根据能量守恒定律,E1、E2、E3、E4之间的关系为____________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com