
题目列表(包括答案和解析)
23.下表列出了元素周期表中的部分元素(用元素符号或名称表示):
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
B |
C |
N |
O |
F |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Si |
P |
S |
Cl |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
锗 |
As |
Se |
Br |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
锑 |
Te |
I |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
铋 |
At |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
117 |
|
(1)表中用元素符号所列出的元素除H外,其余非金属元素原子 (填序号)。
a.最外层电子数都大于4
b.主族序数等于周期数
c.最外层电子数都大于电子层数
(2)以下关于元素的性质或用途的叙述正确的是 (填序号)。
a.P、S、Cl等元素的化合物常用来制取农药
b.硅(Si)、锗(Ge)可用于制半导体材料
c.F是最活泼非金属元素,其最高价氧化物的水化物的酸性最强
(3)以下方法可以比较S、Cl非金属性强弱的是 (填序号)。
a.分别测定Na2S溶液和NaCl溶液的pH
b.将Fe分别与S、Cl2反应,分析产物中Fe的化合价
c.将H2S通入氯水中,观察到有淡黄色固体析出:H2S + Cl2 → 2HCl + S↓
(4)美俄科学家2006年10月5日宣布他们已制得了118号元素。试分析,若制得117号元素(位置见表),按元素周期表中金属与非金属的分区,它应是一种 (选填“金属”、“非金属”)元素,写出117号元素最外层电子排布式 。
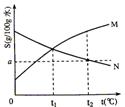
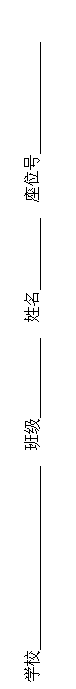
22.下图是M、N两种物质的溶解度曲线,在t2℃时往盛有100g水的烧杯中先后加入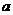 gM和
gM和 gN(两种物质溶解时互不影响,且溶质仍是M、N),充分搅拌,将混合物的温度降低到t1℃,下列说法正确的是
gN(两种物质溶解时互不影响,且溶质仍是M、N),充分搅拌,将混合物的温度降低到t1℃,下列说法正确的是
 A.t1℃时,M、N的溶解度相等,得到M、N的饱和溶液
A.t1℃时,M、N的溶解度相等,得到M、N的饱和溶液
B.t2℃时,得到M的不饱和溶液、N的饱和溶液
C.t2℃时,M、N的物质的量浓度一定相等
D.t1℃时,M、N的溶质质量分数一定相等
高三教学调研
 化学试卷
化学试卷
 第II卷(共84分)
第II卷(共84分)
21.2005年是勒夏特列(1850-1936)诞生155周年,他发现的平衡移动原理在工农业生产和日常生活中有许多重要应用。下列事实中,能用勒夏特列原理解释的是
A.实验室常用排饱和食盐水的方法收集氯气
B.由H2(g)、I2(g)、HI(g)组成的平衡体系,体积缩小后颜色加深
C.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
D.在合成氨工业中选择适当的催化剂可提高生产效率
20.下列有关实验的做法或说法正确的是
A.在制备乙烯实验中,为防止反应过于剧烈,加热时应使温度缓慢上升至170℃
B.向苯酚钠稀溶液中,不断通入足量二氧化碳气体,溶液最终不会出现浑浊现象
C.将溴乙烷滴入NaOH溶液后加热,待充分反应后,再加入AgNO3溶液后有浅黄色沉淀生成。
D.分别向三支盛有乙酸乙酯的试管中加入氢氧化钠溶液、稀硫酸、水,同时在水浴中加热,三支试管中香味持续时间按加入氢氧化钠、稀硫酸、水的顺序依次增长
19.实验室中,下列除去括号内杂质的有关操作正确的是
A.苯(硝基苯):加少量蒸馏水振荡,待分层后分液
B.乙醇(水):加新制的生石灰,蒸馏
C.CO2(HCl、水蒸气):通过盛有碱石灰的干燥管
D.乙烷(乙烯):通入氢气发生加成反应
18.两种微粒的质子数和电子数都相等,它们不可能是
A.一种阳离子和一种阴离子 B.一种分子和一种离子
C.一种原子和一种分子 D.一种单质分子和一种化合物分子
17.有一酸性溶液可能含有SO42-、Br-、H2SO3、NH4+ 等微粒,对该溶液进行实验:
(1)取少量溶液加热,放出的气体可以使品红溶液褪色;
(2)取原溶液加碱液使溶液呈碱性,加热,放出的气体能使湿润的红色石蕊试纸变蓝;
(3)取原溶液加氯水,溶液略显黄色,再加入BaCl2溶液,产生的白色沉淀不溶于稀硝酸。
对于下列微粒,不能确定其在原溶液中一定存在的是
A.SO42- B.Br- C.H2SO3 D.NH4+
16.在一定温度下,向饱和的烧碱溶液中加入一定量的Na2O2,充分反应后恢复到原来温度,下列说法中正确的是
A.溶液中c(Na+ )增大,有O2放出 B.溶液中Na+ 数目减小,有O2放出
C.溶液的pH增大,有O2放出 D.溶液的pH不变,有H2放出
15.氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有H2生成,下列叙述正确的是
A.NH4H是共价化合物 B.NH4H与水反应时,水作还原剂
C.NH4H溶于水,所形成的溶液显碱性 D.NH4H中的H元素只有一种化合价
14.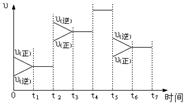 下图表示反应
下图表示反应 在某一时间段中反应速率与反应过程的关系。由图判断,SO3的百分含量最高的一段时间是
在某一时间段中反应速率与反应过程的关系。由图判断,SO3的百分含量最高的一段时间是
A.t1-t2 B.t3-t4 C.t4-t5 D.t6-t7
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com