
题目列表(包括答案和解析)
23.(10分) 江苏省东海县矿产丰富,除了水晶制品名扬天下外,蛭石、蛇纹石等矿石储量大,品位高,其相关的耐火、保温隔热材料(主要成分为MgO、Al2O3)工业也较发达。
某中学化学探究小组通过查阅相关资料,对蛭石的组成进行了实验探究。
I、相关资料:
①蛭石的成分可看成是由MgO、Fe2O3、Al2O3、SiO2组成
②氢氧化物开始沉淀及沉淀完全时的pH
|
氢氧化物 |
Fe(OH)3 |
Mg(OH)2 |
Al(OH)3 |
|
沉淀的pH范围 |
1.5~4.1 |
9.4~12.4 |
3.3~5.2 |
 Ⅱ、相关实验:
Ⅱ、相关实验:
Ⅲ、实验数据:
① 矿石样品质量为:8.22g
② 实验过程中得到固体的质量:A-2.40g、 D-2.14g 、 F-1.56g
③ 每次转化所得固体成分只有一种
请你根据以上内容和中学化学知识回答以下问题
(1)过滤操作需要的玻璃仪器有:
(2)写出由D制一种红色颜料的化学方程式:
(3)工业上的耐火材料通常由F及滤液E进一步转化而成,请你分析滤液E中可能含有成分,设计一个从滤液E制取耐火材料的实验方法:
(4)滤液B和NaOH溶液反应时,应控制溶液的pH在7~8之间,这是因为:
(5)通过计算,写出用氧化物的形式表示蛭石组成的化学式
21.(10分)实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:
4NH4++6HCHO=3H++6H2O+(CH2)6N4H+ [滴定时,1 mol(CH2)6N4H+与 l mol H+相当],然后用NaOH标准溶液滴定反应生成的酸,某兴趣小组用甲醛法进行了如下实验:
步骤I 称取样品1.500g。
步骤II 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤Ⅲ 移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛溶液,摇匀、静置
5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。
按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数 (填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积
(填“偏大”、“偏小”或“无影响”)
③滴定时边滴边摇动锥形瓶,眼睛应观察
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由 色变成 色。
(2)滴定结果如下表所示:
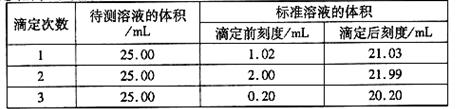
若NaOH标准溶液的浓度为0.1010mol·L-1则该样品中氮的质量分数为
20. (10分)实验室配制500mL0.1molLNa2CO3溶液,回答下列问题:
(1)应用托盘天平准确称取十水碳酸钠晶体 g。
(2)若在称量样品时,药品放在天平右盘上,砝码放在左盘上,天平平衡时,则实际称量的碳酸钠晶体是 g(1g以下用游码)。
(3)用托盘天平和小烧杯称出碳酸钠晶体的质量,其正确操作顺序的标号是:
(同一标号有的可用多次)。
A.调整零点 B.将游码移到刻度尺的零刻度处 C.将碳酸钠晶体放入小烧杯中和称量 D.称量空的小烧杯 E.将砝码放回砝码盒内 F.记录称量结果
(4)配制碳酸钠溶液时需要的主要仪器有(选填序号,多选倒扣分) 。
A.500mL容量瓶 B.烧杯 C.玻璃棒 D.分液漏斗 E.250mL容量瓶 F.移液管
(5)在下列实验操作中,溶液的浓度是偏高、偏低还是不变?
① 洗涤容量瓶后容量瓶中还残存有少量蒸馏水 ;②加水时不小心水越过刻度线 ;③定容后摇匀液面低于刻度线 ;④定容时俯视刻度线 。
20. 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列描述正确的是
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列描述正确的是
A.反应开始到10s,用Z表示的反应速率为0.158 mol/(L·s)
B.反应开始到10 s,X的物质的量浓度减少了0.79 mol/L
C.反应的化学方程式为:X(g)+Y(g)=Z(g)
D.反应开始到10 s时,Y的转化率为79.0%
第Ⅱ卷 非选择题(共80分)
19.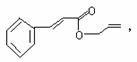 对复杂的有机物结构可用“键线式”表示。如苯丙烯酸1-丙烯酯:
对复杂的有机物结构可用“键线式”表示。如苯丙烯酸1-丙烯酯:
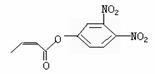
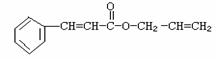 可简化为
可简化为
杀虫剂“阿乐丹”的结构表示为 ,若它在稀酸作用下
能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是( )
A.遇FeCl3溶液均显紫色 B.均能发生银镜反应
C.均能与溴水发生反应 D.均能与NaOH溶液发生反应
18.将2.4 g Fe 、Mg合金投入到一定量的稀硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下的气体V L(硝酸被还原成NO),若向反应后的溶液中加入足量的NaOH溶液,待金属元素全部沉淀后,再将沉淀过滤、洗涤、灼烧后称量,质量为3.6 g。则收集到的气体体积V值可为
A.0.986 B.1.12 C.3.36 D.6.72
17.下列反应中,氧化剂与还原剂物质的量的关系为1∶2的是
A.O3+2KI+H2O==2KOH+I2+O2
B.2CH3COOH+Ca(ClO)2==2HClO+Ca(CH3COO)2
C.I2+2NaClO3==2NaIO3+Cl2
D.4HCl+MnO2==MnCl2+Cl2↑+2H2O
16.下列各种溶液中,一定不能大量共存的离子组是
A.pH=0的溶液中:Fe2+、NO3-、SO42-、I-
B.由水电离的c(H+)=10-14mol·L-1 的溶液中:K+、Na+、Ca2+、HCO3-
C.含有大量Fe3+的溶液中:Mg2+、Al3+、Cu2+、SO42-
D.使紫色石蕊试液变蓝色的溶液中:Na+、AlO2-、S2-、SO42-
15.类推的思维方法在化学学习和研究中常回产生错误的结论,因此类推出的结论要经过实践的检验才能决定其正确与否.下列几种类推结论中不正确的是
A.Mg失火不能用CO2灭火;Na失火也不能用CO2灭火
B.Fe3O4可写成FeO·Fe2O3;Pb3O4可写成PbO·Pb2O3
C.能用电解熔融MgCl2来制取金属镁,也能用电解熔融AlCl3来制取金属铝;
D.Fe与S直接化合生成FeS;Al与S直接化合也可以生成Al2S3
14.下列离子方程式中,正确的是
A. 氢氧化铝与足量盐酸反应 Al(OH)3 + 3H+ = Al3+ + 3H2O
B. NH4HCO3和足量NaOH溶液相混合 HCO3- + OH- = CO32- + H2O
C. 大理石溶解于醋酸 CaCO3 + 2H+ = Ca2+ + CO2↑+ H2O
D. 过量CO2通入氢氧化钠溶液中 CO2 + 2OH- = CO32- + H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com