
题目列表(包括答案和解析)
24.(12分)
(1)K=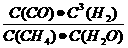 (2分);(2)增大(2分);不变(2分);(3)<(2分);
(2分);(2)增大(2分);不变(2分);(3)<(2分);
 (2分)
(2分)
(4)防止催化剂中毒(2分);
25每空2分)
(1)(3分)硫 铜 Na2SO4
(2)(2分)ⅡB 三
(3)过滤(1分)
(4)(1分)MnO2+MS+2H2SO4==MnSO4+ MSO4+S↓+2H2O
(5) (1分)新工艺不需要高温焙烧,大大节约了能源(燃料)(或旧工艺高温焙烧产生大气污染物SO2,新工艺不产生有害气体;或新工艺许多物质都可以循环利用)
23.(10分)(1)漏斗、烧杯、玻璃棒 ;(2)2Fe(OH)3 Fe2O3+3H2O
Fe2O3+3H2O
(3)将所得的滤液E加热煮沸一定时间(或向滤液中加入足量的NaOH溶液),
再进行过滤、洗涤、干燥,最后进行高温灼烧。
(4)根据表中数据,控制溶液的pH在7~8之间,Mg2+没有变化,Al3+转化为AlO2- ,
只有Fe(OH)3沉淀。(5)8MgO·Al2O3·Fe2O3·4Si
22.(10分)(l)① 偏高② 无影响③ B ④ 无 粉红(或浅红)( 2 ) 18.85 %
21.(共10分)
(1)5.3……1分; (2)4.7……1分 (3)BADFCFEB……2分(只要错1个序号, 2分全扣)(4)ABC……2分(每选错1个倒扣1分,直到扣完为止,但不出现负分)
(5)[每空1分,共4分]①不变;②偏低;③不变;④偏高。
29.(10分)下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
|
a |
|
|
|||||||||||||||
|
b |
|
|
|
c |
d |
e |
f |
|
|||||||||
|
g |
h |
i |
j |
|
k |
l |
m |
||||||||||
|
n |
|
|
|
|
|
|
o |
|
|
|
|
|
|
|
|
|
|
试回答下列问题:
(1)请写出元素O的基态原子电子排布式 。
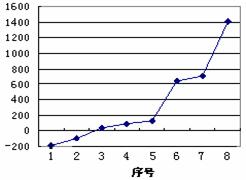 (2)第三周期8种元素按单质熔点高
(2)第三周期8种元素按单质熔点高
低的顺序如右图,其中序号“8”代
表 (填元素符号);其中电负性
最大的是 (填右图中的序号)。
(3)由j原子跟c原子以1 : 1相互
交替结合而形成的晶体,晶型与晶
体j相同。两者相比熔点更高的是 (填化学式),
试从结构角度加以解释: 。
(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
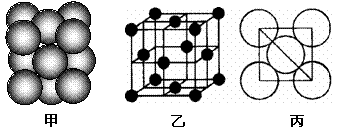
若已知i的原子半径为d,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
①晶胞中i原子的配位数为___ ____ ,一个晶胞中i原子的数目为_ _;
②该晶体的密度为_______(用字母表示)。
第Ⅱ卷 非选择题(共80分)
28.(10分)我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染。PETG的结构简式为:
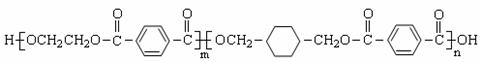
已知:
(1) 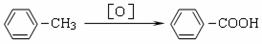
(2) 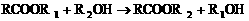 (R、R1、R2表示烃基)
(R、R1、R2表示烃基)
这种材料可采用以下合成路线:
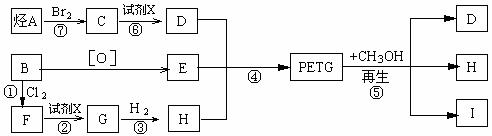
试回答下列问题:
⑴ 反应②⑥加入的试剂X是___________,⑤的反应类型是__ 。
(2)写出结构简式:B ____________________ I ____________________。
(3)合成时应控制的单体的物质的量
n(D)∶n(E)∶n(H)= _____∶______∶______(用m、n表示)。
(4)写出化学方程式:
反应③: ;
反应⑥: 。
27.(10分)
根据下面的反应路线及所给信息填空。
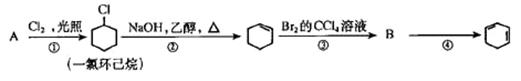
(1)A的结构简式是 _____________,名称是 。
(2)①的反应类型是: 。
③的反应类型是: 。
(3)反应④的化学方程式是 _____________________________。
26、(8分)沉淀物并非绝对不溶,其在水及各种不同的溶液中溶解有所不同,同离子效应、络合物的形成等都会使沉淀物的溶解度有所改变。下图是AgCl在NaCl、AgNO3 溶液中的溶解情况。
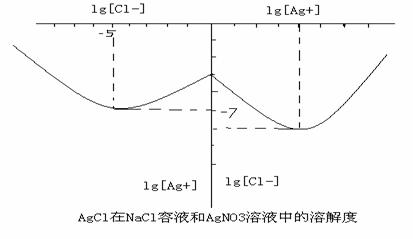
由以上信息可知:
(1)AgCl的溶度积常数的表达式为: ,由图知AgCl的溶度积常数为 。
(2)AgCl在NaCl溶液中的溶解出现如图所示情况(先变小后变大)的原因是:
。
(3)反应AgCl + NaBr == AgBr + NaCl能在水溶液中进行,是因为 。
25. (10分)(某地有软锰矿(主要成份为MnO2,含少量Al2O3、SiO2)和闪锌矿(主要成份ZnS,含少量FeS、CuS、CdS、SiO2),科研人员采用新工艺生产二氧化锰和锌,同时还得副产品镉和X、Y、Z等。工业流程图如下图(框图中水省略):
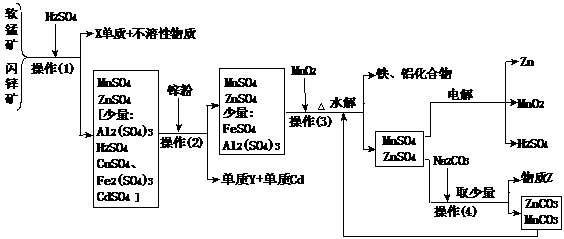
请回答:
(1)副产品X的名称是 ,Y的名称是 、Z的化学式为 。
(2)他们的主要产品中的元素在周期表中,锌(30Zn)属 族,X在 周期。
(3)图中“操作(1)~(4)”都包含的共同一种操作,在实验室中该操作的名称为 。
(4)操作(1)中,在稀H2SO4存在下MnO2把硫化物氧化成硫单质和+2价硫酸盐。如果硫化物用MS表示,请写出MnO2与硫化物反应的化学方程式: 。
(5)旧工艺生产二氧化锰,是将软锰矿与煤混合粉碎后高温焙烧,再用硫酸浸取焙烧料净化后电解。对比旧工艺,新工艺有好多个优点,请你至少说出新工艺的一个优点:
。
24.
甲烷蒸气转化反应为:CH4(g)+H2O(g) CO(g)+3H2(g),工业上可利用此反应生产合成氨原料气H2。
CO(g)+3H2(g),工业上可利用此反应生产合成氨原料气H2。
已知温度、压强和水碳比[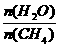 ]对甲烷蒸汽转化反应的影响如下图:
]对甲烷蒸汽转化反应的影响如下图:
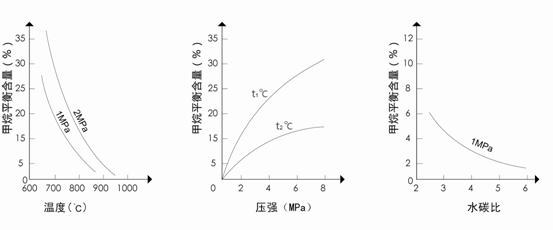
图1(水碳比为3) 图2(水碳比为3) 图3(800℃)
(1)该反应平衡常数K表达式为________________________。
(2)升高温度,平衡常数K__________(选填“增大”、“减小”或“不变”,下同),降低反应的水碳比,平衡常数K__________。
(3)图2中,两条曲线所示温度的关系是:t1_____t2(选填>、=或<);在图3中画出压强为2 MPa时,CH4平衡含量与水碳比之间关系曲线。
(4)工业生产中使用镍作催化剂。但要求原料中含硫量小于5×10-7%,其目的是____________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com