
题目列表(包括答案和解析)
12.金属钛(Ti)性能优越,被称为继铁、铝制后的“第三金属”。工业上以金红石为原料制取Ti的反应为:
aTiO2 + bCl2 + cC 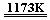 aTiCl4 + cCO ……反应①TiCl4 +2Mg
aTiCl4 + cCO ……反应①TiCl4 +2Mg 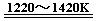 Ti + 2MgCl2 ……反应②
Ti + 2MgCl2 ……反应②
关于反应①、②的分析不正确的是
(1) TiCl4在反应①中是还原产物,在反应②中是氧化剂;(2) C、Mg在反应中均为还原剂,被还原;(3)在反应①、②中Mg的还原性大于C,C的还原性大于TiCl4;(4) a=1,b=c=2;(5) 每生成19.6 g Ti,反应①、②中共转移4.8 mol e-。
A.(1)(2)(4) B.(2)(3)(4) C.(3)(4) D.(2)(5)
16.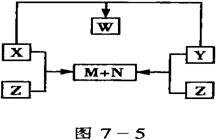 (15分)化合物X、Y、Z是由短周期的三种元素两两结合而成,X、Y、Z之间的转化关系如图7-5所示(无被省略的物质):又知:X、N、W均为液态物质,且X与N的组成元素相同。试回答:
(15分)化合物X、Y、Z是由短周期的三种元素两两结合而成,X、Y、Z之间的转化关系如图7-5所示(无被省略的物质):又知:X、N、W均为液态物质,且X与N的组成元素相同。试回答:
(1)上述转化关系图中生成W涉及到的基本反应类型是__________________。
(2)X、Y、Z、W的化学式依次是:X_________、Y_________、Z____________、W____________。
(3)写出X与Y、X与Z反应的化学方程式:X+Y:_________________________________;
X+Z:_________________________________。
15.(2007年高考全国理综卷I,15分)A、B、C、D、E均为可溶于水的固体,组成它们的离子有
|
阳离子 |
Na+ |
Mg2+ |
Al3+ |
Ba2+ |
|
|
阴离子 |
OH- |
Cl- |
CO32 - |
SO42 - |
HSO4- |
分别取它们的水溶液进行实验,结果如下:
①A溶液与B溶液反应生成白色沉淀,沉淀可溶于E溶液;
②A溶液与C溶液反应生成白色沉淀,沉淀可溶于E溶液;
③A溶液与D溶液反应生成白色沉淀,沉淀可溶于盐酸;
④B溶液与适量D溶液反应生成白色沉淀,加入过量D溶液,沉淀量减小,但不消失。
据此推断它们是A__________;B___________;C__________;D___________;E___________。
14. (12分)有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如下图所示的装置进行实验。通入SO2气体,将带余烬的木条插入试管C中,木条复燃。
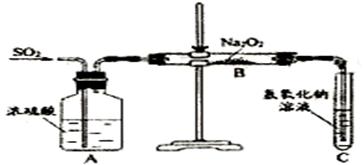
请回答下列问题:
(1) 第1小组同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是: 。
(2) 请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3。
。
(3) 第2小组同学认为Na2O2与SO2反应生成了Na2SO3和O2外,还有Na2SO4生成。为检验是否有Na2SO4生成,他们设计了如下方案:

上述方案是否合理? 。请简要说明理由:
① ;② 。
13.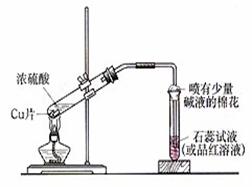 (18分)实验室常用下列装置来进行铜跟浓硫酸反应等一系列实验。(1)根据什么现象可判断铜跟浓硫酸反应有SO2生成 _____________
。
(18分)实验室常用下列装置来进行铜跟浓硫酸反应等一系列实验。(1)根据什么现象可判断铜跟浓硫酸反应有SO2生成 _____________
。
根据什么现象可判断铜跟浓硫酸反应有硫酸铜生成_____________________________________________________。
写出甲装置中发生的主要反应的化学方程式_____________________________________________________。
(2)你在实验室中进行这个实验时,除了(1)小题中指到的实验现象外,还可以观察到许多其它的实验现象,请写出两种: ____________ ,
________________ 。
(3)装置乙的试管口部放有一团浸有碱液的棉花,棉花中通常是浸有饱和碳酸钠溶液,写出棉花中发生反应的化学方程式___________________________________。
12. .下列溶液中,不能区别SO2和CO2气体的是
①石灰水 ②KMnO4溶液 ③溴水 ④酸化的Ba(NO3)2溶液 ⑤品红溶液
A.①②③⑤ B.②③④⑤ C.只有① D.①③
第I卷答题表 班考号 姓名
第Ⅱ卷(非选择题共60分)
11. 下列离子方程式书写正确的是:
A.将Ba(OH)2溶液不断加入KAl(SO4)2溶液中反应至沉淀物质的量最大:
3Ba2+ + 6OH– + 2Al3+ + 3SO42–== 3BaSO4↓+ 2Al(OH)3↓
B.向硝酸银溶液中加入过量氨水:Ag+ + NH3·H2O =AgOH↓ + NH4+
C.CuSO4溶液跟Ba(OH)2溶液混合:Ba2+ + SO42– == BaSO4↓
D.氢氧化铁溶于氢碘酸中:Fe(OH)3 + 3H+ = Fe3+ + 3H2O
10. .欲鉴别物质的量浓度都为0.1 mol·L-1的KCl、(NH4)2SO4、NH3·H2O和H2SO4四瓶无色溶液,下列实验方案最佳的是
A.用pH试纸鉴别 B.分别用闻气味和pH试纸鉴别
C.分别用BaCl2和NaOH溶液鉴别 D.用Ba(OH)2溶液鉴别
9.已知I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性强弱的顺序是SO2>I->H2O2>Fe2+>Cl-,则下列反应不可能发生的是
A.2Fe3++SO2+2H2O====2Fe2++SO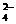 +4H+ B.2Fe2++Cl2====2Fe3++2Cl-
+4H+ B.2Fe2++Cl2====2Fe3++2Cl-
C.I2+SO2+2H2O====H2SO4+2HI D.H2O2+H2SO4====SO2+O2+2H2O
8. 下列关于浓硫酸的叙述正确的是
A.浓硫酸具有吸水性,因而能使蔗糖炭化
B.浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体
C.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
D.浓硫酸在常温下能够使铁、铝等金属钝化
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com