
题目列表(包括答案和解析)
27.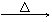 (14分)某种碱式碳酸铜,其组成可表示为:Cu2(OH)2CO3·xH2O。在加热条件下,可以发生分解,化学方程式为:Cu2(OH)2CO3·xH2O
2CuO+CO2↑+(x+1) H2O
(14分)某种碱式碳酸铜,其组成可表示为:Cu2(OH)2CO3·xH2O。在加热条件下,可以发生分解,化学方程式为:Cu2(OH)2CO3·xH2O
2CuO+CO2↑+(x+1) H2O
现取一定量的(不称量其质量)该固体样品,先后完成两个实验:
实验(i):测定该碱式碳酸铜粉末的组成中结晶水x的值;
实验(ii):用实验(i)结束后的残留固体完成乙醇的催化氧化并验证其反应产物。
请回答下列问题:
(1)用下图中的仪器(必要的铁架台、铁夹、酒精灯等均在图中略去)组装完成实验(i)的实验装置,组装时仪器按气流方向从左到右连接的顺序为 → → → C 。
在这套装置中,干燥管C中盛有的物质是 。(填写下列选项的编号)
 A.无水硫酸铜 B.碱石灰 C.氯化钠晶体 D.无水氯化钙
A.无水硫酸铜 B.碱石灰 C.氯化钠晶体 D.无水氯化钙
(2)若要用上图中的各种仪器组装完成实验(ii)的实验装置,组装时仪器也按气流方向从左到右连接的顺序为 → → → 。在这套装置中,干燥管C的作用是 。
(3)在完成两个实验时,首先都必须先 (实验操作步骤),然后在仪器 (填装置对应字母,下同)中加入碱式碳酸铜,乙醇放入仪器 中。
(4)在实验(ii)中,需要加热的仪器是 (填装置对应字母)。
(5)写出D中反应的化学方程式为
(6)若实验(i)测得CO2的质量为a克,水的质量为b克,则x的表达式= 。
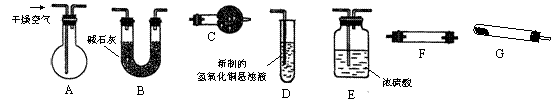
26.(10分)下图是一个制取氯气,并以氯气为原料进行特定反应的装置。
(1)A是氯气发生装置,其反应的化学方程式为 。
(2)实验开始时,先点燃A处的酒精灯,打开旋塞K,将Cl2充满整个装置,再点燃D处的酒精灯,接上E装置,Cl2通过C瓶后再进入D,发生反应后的产物是CO2和HCl,试写出D中的反应化学方程式 。装置C的作用是 。
(3)在E处,可能观察到的实验现象是 。
(4)若将E处烧杯中的溶液改为澄清的石灰水,反应过程中现象为 (填字母编号)
A.有白色沉淀生成 B.无明显现象 C.先有白色沉淀生成后沉淀消失
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有Cl2产生,此时B中的现象是 ,B的作用是
。
25.(8分)A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A、C及B、D分别是同一主族元素,B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的两倍,又知四种元素的单质中有两种气体、两种固体。
(1)D元素在周期表中的位置 ,其原子的核外电子排布式 。
(2)C、D两元素形成的化合物W的电子式为 ,其水溶液呈 性。
(3)A、C、D三种元素共同构成的化合物中含有的化学键为 、 。
(4)写出两种均含A、B、C、D四种元素的化合物相互间发生反应,且生成气体的离子方程式 。
24. (8分)t℃时,将3 mol A和1 mol B气体通入容积为2 L的密闭容器中(容积不变),发生如下反应:3A(g) + B(g) xC(g)+Q(Q>0),2 min时反应达到平衡状态(温度不变),剩余了0.8
mol B,并测得C的浓度为0.2mol/L,请填写下列空白:
(8分)t℃时,将3 mol A和1 mol B气体通入容积为2 L的密闭容器中(容积不变),发生如下反应:3A(g) + B(g) xC(g)+Q(Q>0),2 min时反应达到平衡状态(温度不变),剩余了0.8
mol B,并测得C的浓度为0.2mol/L,请填写下列空白:
(1)从开始反应至达到平衡状态,生成C的平均反应速率为 mol/L·min。
(2)x= ;此反应的平衡常数表达式K= 。
(3)恒温时,若向上述平衡混合物的容器中再充入a mol C后,化学平衡将向 方向移动,B物质的质量分数 ,K值 (填“变大”或“变小”或“不变”,下同)。
(4)若升高反应体系的温度,v (C) ,混合气体的平均相对分子质量 。
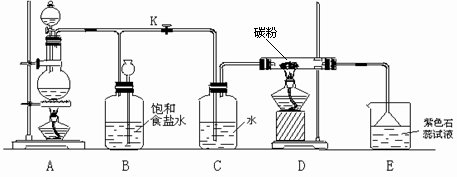
23. (8分)2001年是20世纪伟大的化学家鲍林(Linus Pauling 1901~1994)诞辰100周年。他是一位化学结构大师,曾获得1954年诺贝尔化学奖。后人在他的遗作中发现有一结构式如右图所示。
(8分)2001年是20世纪伟大的化学家鲍林(Linus Pauling 1901~1994)诞辰100周年。他是一位化学结构大师,曾获得1954年诺贝尔化学奖。后人在他的遗作中发现有一结构式如右图所示。
请你对这个结构作一番分析后,回答下列问题。
(1)它的分子式是 。
(2)如果该分子中的氮原子都在一个平面上,则该分子中的所有原子是否可能处于同一平面内 (填“可能”或“不可能”)。
(3)有人预测它可能是炸药,如果它在没有氧气参与的情况下发生爆炸(假设发生分解反应,生成两种单质和两种氧化物,其中一种是CO气体),则反应的化学方程式可能为 ;如果有足量氧气参与的条件下发生爆炸,反应方程式为 ,1mol该化合物爆炸时需消耗 mol氧气。
22. 按右图装置(夹持仪器略)进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是………………………………………………( )
按右图装置(夹持仪器略)进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是………………………………………………( )
A.若A为浓盐酸,B为MnO2,C中盛品红溶液,
则C中溶液褪色
B.若A为醋酸,B为贝壳,C中盛澄清石灰水,
则C中溶液变浑浊
C.若A为浓氨水,B为生石灰,C中盛A1C13溶液,
则C中先产生白色沉淀后沉淀又溶解
D.实验仪器D可以起到防止溶液倒吸的作用
第Ⅱ卷(共84分)
21.向300mLKOH溶液中缓慢通入2.24L(标准状况) CO2气体,充分
反应后,在减压低温下蒸发溶液,得到19.4g白色固体。则下列
说法中正确的是…………………………………………………………………( )
A.此白色固体是KOH和K2CO3的混合物
B.此白色固体是K2CO3和KHCO3的混合物
C.原KOH溶液的物质的量浓度是1 mol/L
D.原KOH溶液的物质的量浓度是0.5 mol/L
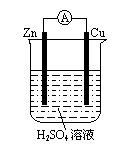
20.关于右图所示装置的下列说法中正确的是…………………( )
A.电流表指针不会偏转
B.Zn是阴极,Cu是阳极
C.外电路中电流方向是Cu→Zn
D.Zn是负极,在反应中失去电子,发生氧化反应
19.在100mL0.10mol/L的AgNO3溶液中加入100mL溶有2.08g BaCl2的溶液,再加入100mL溶有0.010molCuSO4·5H2O的溶液,充分反应。下列说法中正确的是…………( )
A.最终得到白色沉淀和无色溶液
B.最终得到白色沉淀是等物质的量的两种化合物的混合物
 C.在最终的溶液中n(Cl―)=0.01mol
C.在最终的溶液中n(Cl―)=0.01mol
D.在最终的溶液中c(Cu2+)=0.01mol/L
18. 在容积不变的密闭容器中的如下反应:2SO2(g)+O2(g) 2SO3(g)+196.6kJ·mol-1,
在容积不变的密闭容器中的如下反应:2SO2(g)+O2(g) 2SO3(g)+196.6kJ·mol-1,
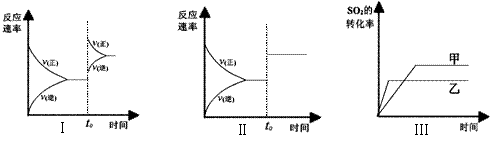 当其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是……( )
当其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是……( )
A.图I研究的是t0时刻增大O2的浓度对反应速率的影响
B.图II研究的是t0时刻加入催化剂后对反应速率的影响
C.图III研究的是催化剂对平衡的影响,且甲的催化效率比乙高
D.图III研究的是温度对化学平衡的影响,且乙的温度较低
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com