
题目列表(包括答案和解析)
28、取一定量的Na2CO3、NaHCO3、Na2SO4混合物与250ml 1.00mol/L过量盐酸反应,生成2.016升CO2 (标准状况),然后加入500ml 0.100mol/LBa(OH)2溶液,得到沉淀的质量为2.33g,溶液中过量的碱用10.0ml 1.00mol/L盐酸恰好中和。计算混合物中各物质的质量。
27、下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体。
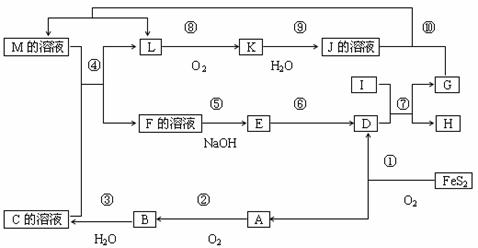
请填写下列空白
(1)在元素周期表中,组成单质G的元素位于第 周期,第 族
(2)在反应⑦中氧化剂与还原剂的物质的量之比为
(3)在反应②③⑥⑨中,既属于化合反应又属于非氧化还原反应的是 (填序号)
(4)反应④的离子方程式是
(5)将化合物D与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是
26、短周期三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5, X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数之和;Y元素原子的最外电子层上的电子数是它的电子层数的2倍;X和Z可以形成XZ3的化合物。请回答
(1)X、Y、Z元素的名称分别是 、 、
(2)Y2Z2分子的电子式
(3)某含有X、Y、Z三种元素的化合物分子A,其分子内所含电子总数为18,写出A的结构简式
(4)用惰性电极电解X的最高价含氧酸的水溶液,阳极的电极反应式为
25、卤素互化物是指不同卤素原子之间以共价键结合形成的化合物,XX′型卤素互化物与卤素单质结构相似,性质相近。试回答下列问题
(1)卤素互化物BrCl 能发生下列反应
H2O + BrCl = HBrO + HCl KBr + BrCl = KCl + Br2
①写出KI与IBr反应的化学方程式
②写出苯与ICl发生取代反应生成一卤代物的化学方程式(不必写条件)
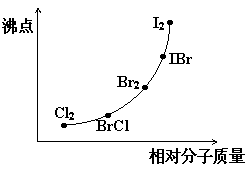
(2)右图是部分卤素单质和XX′型卤素互化物的沸点与其相对分子质量的关系图。它们的沸点随着相对分子质量增大而升高,其原因是
(3)试推测ICl的沸点所处的最小范围
24、在分子的结构式中,由一个原子提供成键电子对形成的共价键用→表示,如
H2SO4: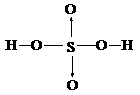
写出硝酸的结构式 、硝酸乙酯的结构式
23、元素周期表前20号元素中,某两种元素的原子序数相差3,周期数相差1,它们形成化合物时原子数之比为1:2
(1)写出符合此条件的常见化合物的化学式 ;
(2)写出其中两种化合物的电子式 ;
(3)写出其中两种化合物分别和水反应的离子方程式
, 。
22、(1)写出表示8个质子、10个中子的原子的化学符号
(2)元素周期表中位于第7纵行的锰元素属于第 族
(3)元素周期表中最活泼非金属位于第 纵行
(4)所含元素超过18种的周期是第 、 周期
21、50ml 0.50mol/L盐酸与50ml/0.55mol/LNaOH溶液在右图所示装置中进行中和反应,通过反应过程中所放出热量可计算中和热。回答下列问题
(1)装置图所示装置的不足之处为 、
,若用此装置测得的中和热数值 (偏大、偏小、无影响)
(2)实验中改用60ml 0.50mol/L盐酸与50ml 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量 (相等、不相等),所测得中和热
(基本相等、不相等),简述理由
(3)若含20.0gNaOH的稀溶液与足量稀盐酸反应放出28.7kJ热量,表示中和热的热化学方程式为
20、用惰性电极电解+n价金属的硝酸盐,当阴极析出m克金属时,阳极上产生气体560ml(标准状况),则金属相对原子质量为
A.4mn B.10mn C.m/2n D.2m/n
19、同温同压下,两个容积相等的储气瓶,一个装有C2H4,另一个装有C2H2和C2H6的混和气,两瓶内的气体一定具有相同的
A.质量 B.原子总数 C.碳原子数 D.密度
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com