
题目列表(包括答案和解析)
19.(2分)完成下列离子方程式(给出物质的计量数不能改变)
(1) +6H+= 2Fe3++3
(2) +Ca2++2 =CaCO3↓+
18.(6分)20世纪80年代,科学家发现的C60分子是由60个碳原子构成的,它的形状像足球(图C),因此又叫足球烯;90年代科学家又发现一种碳的单质--碳纳米管,它是由碳原子构成的六边环形的管状大分子,其六元环结构与足球烯的六元环相似(图D),图A、图B分别是金刚石和石墨的结构示意图。图中小黑点或小黑圈均代表碳原子。
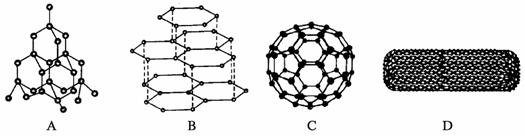
试回答下列问题:
(1)金刚石、石墨、足球烯和碳纳米管的熔点存在较大差异的原因是
_________________________________________________________________。
(2)常温下足球烯和碳纳米管的化学性质是否比金刚石和石墨活泼?_________________(填“活泼”和“不活泼”),理由是______ ___。
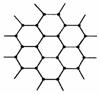 (3)由右边石墨的晶体结构俯视图可推算在石墨晶体中,每个正六边形平均所占有的C 原子数与C-C键数之比为_____________。
(3)由右边石墨的晶体结构俯视图可推算在石墨晶体中,每个正六边形平均所占有的C 原子数与C-C键数之比为_____________。
(4) 燃氢汽车之所以尚未大面积推广除较经济的制氢方法尚未完全解决外,制得H2后还需解决贮存问题。在上述四种碳单质中有可能成为贮氢材料的是__ __。
17.(4分)玻璃棒是化学实验中常用的仪器,其作用是用于搅拌、过滤或转移液体时引流。下列有关实验过程中,肯定不需要使用玻璃棒进行操作的是(填字母代号)______
A.一定溶质质量分数溶液的配制
B.用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验
C.用普通漏斗组成的过滤装置进行过滤实验
D.实验室用FeSO4溶液和NaOH溶液制备Fe(OH)2沉淀
E.用已知浓度的盐酸和未知浓度的氢氧化钠溶液进行中和滴定实验
F.硫酸铜晶体里结晶水含量测定的实验
G.将适量氯化铁饱和溶液滴入沸水中制氢氧化铁胶体
16.四个可加热的密闭容器中,分别装有;①Na2O2和NaHCO3;②Na2O2和NH4HCO3;③Na2O2和Ca(HCO3)2;④Na2CO3和NaHCO3。各容器中每种物质均为0.5mol,现将各容器加热至300℃,完全分解后排出气体,四个容器中残留固体只有Na2CO3的容器是
A.①② B.②④ C.②③ D.①④ b
第Ⅱ卷(非选择题 共36分)
15.将0.2 mol MnO2和50 mL 12mol/L盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为(不考虑盐酸的挥发)
A.等于0.3 mol B.小于0.3 mol
C.大于0.3 mol D.以上结论都不正确
14.已知IBr的性质与卤素相似,CrO5的结构为 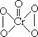 ,次氟酸的结构为H-O-F,下列反应中属于氧化-还原反应的是
,次氟酸的结构为H-O-F,下列反应中属于氧化-还原反应的是
①IBr+H2O=HIO+HBr ②Cr2O72-+4H2O2+2H+=2CrO5+5H2O
③ 2HOF=2HF+O2↑
A.①②③ B.只有② C.只有③ D.无
13.在273℃,404kPa下,一个盛满空气的容器的总质量为95.3g(空气的平均分子量为29),若改盛氢气其总质量为92.6g,则此容器的容积为
A.3.36 L B.2.24 L C.1.12 L D.0.56 L
12.X、Y、Z三种元素,其中有一种金属元素。X、Y原子的电子层数相同。Y、Z原子的最外层电子数相同。又知这三种元素原子的最外层电子数之和为17。原子核中的质子数之和为31。下列说法正确的是
A.X、Y、Z均为主族元素
B.XY3中所有原子均满足最外层8电子稳定结构
C.Y是非金属性最强的元素
D.Z是短周期中原子序数最大的元素
11.向铁和铜的混合物中加入不足量的稀硝酸,反应后剩余了m1g金属,再继续加入一定量的稀硫酸,充分反应后剩余了m2 g金属,则对m1 g金属组成推断正确的是
A.其中只含有铁 B.其中不可能含铁
C.其中肯定含有铜 D.其中铁和铜一定都有
10.当两块铂金属片插入100g 10%CuSO4溶液后,通电一段时间,在阳极析出0.16g物质时,CuSO4溶液的质量分数为
A.8.47% B.8.36% C.8.73% D.9.02%
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com