
题目列表(包括答案和解析)
2.某溶液中大量存在的五种离子:NO3-、SO42-、Fe3+、H+、M,其物质的量之比为:n(NO3-):n(SO42-):n(Fe3+):n(H+):n(M)=2:3:1:3:1,则M可能为 ( )
A.Fe2+ B.Mg2+ C.CO32- D.Ba2+
1.下列说法不正确的是 ( )
A.0.2mol/L的NaHCO3溶液中:[Na+]>[HCO3-]>[OH-]>[H+]
B.叠氮酸(HN3)与醋酸酸性相似,NaN3水溶液中离子浓度大小顺序为:
c(Na+)>c(N3-)>c(OH-)>c(H+)
C.向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中:[NH4+] = [Cl-]
D.pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合后所得溶液的pH>7
11.U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
⑴.V的单质分子的结构式为_______________;XW的电子式为____________;
Z元素在周期表中的位置是_____________。
⑵.U元素形成的同素异形体的晶体类型可能是(填序号)__________。
① 原子晶体 ② 离子晶体 ③ 分子晶体 ④ 金属晶体
⑶.U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)____________;V、W的氢化物分子结合H+能力较强的是(写化学式)______________,用一个离子方程式加以证明_________________。
⑷.YW2气体通人BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为______,由此可知VW和YW2还原性较强的是(写化学式)______。
10. 下图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体。(b)反应①②是化工生产中的重要反应。(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥。(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得。(e)化合物J由两种元素组成,其相对分子质量为32。
下图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体。(b)反应①②是化工生产中的重要反应。(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥。(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得。(e)化合物J由两种元素组成,其相对分子质量为32。
请按要求填空:
⑴反应③的化学方程式______ ________。
⑵C的电子式______________;H的化学式______________。
⑶L的溶液与化合物E反应的离子方程式
__________ ____。
⑷化合物J的化学式_____ _________。
9.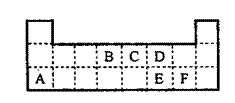 下表是元素周期表的一部分。表中所列的字母分别代表某一元素。(1)1molA与D的氢化物完全反应产生的气体在标准状况下的体积为
。
下表是元素周期表的一部分。表中所列的字母分别代表某一元素。(1)1molA与D的氢化物完全反应产生的气体在标准状况下的体积为
。
(2)写出B的最高价氧化物的电子式 。
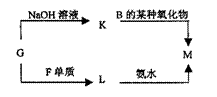 (3)表中的另一种金属元素(未标出)的单质G,可以发生如下图所示转化
(3)表中的另一种金属元素(未标出)的单质G,可以发生如下图所示转化
其中化合物M是一种白色胶状沉淀,则M的化学式为 ;
K的溶液与B的某种氧化物反应的化学方程式为 ;L与氨水反应的离子方程式为 ; 一种新型无机非金属材料由G元素和C元素组成,其化学式为 。
8。有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是
A.若Y的最高正价为+m,则X的最高正价一定为+m
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
D.若X(OH)n为强碱,则Y(OH)n也一定为强碱
7.几种短周期元素的原子半径及主要化合价见下表:
|
元素代号 |
L |
M |
Q |
R |
T |
|
原子半径/nm |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
|
主要化合价 |
+2 |
+3 |
+6、-2 |
+2 |
-2 |
下列叙述正确的是
A、L、M的单质与稀盐酸反应速率L>M B、Q、T两元素的氢化物分子间存在氢键
C、M与T形成的化合物有两性 D、L、Q形成的简单离子核外电子数相等
6.RO3- 酸根所含电子数比硝酸根离子NO3- 的电子数多10,下列关于R和N的说法正确的是 A.R和N元素的最高正化合价相同 B.R在周期表的周期序数和族序数分别比N多1 和2
C.RO3-和NO3-都只能被还原,不能被氧化 D.R和N两种元素的单质都是空气的主要成分
5.下列说法正确的是
A、离子半径:Ca2+<S2-,原子半径:Na>Cl
B、从上到下,卤素的非金属性逐渐减弱,故氢卤酸的酸性依次减弱
C、因为氧化性:HClO>稀H2SO4,所以非金属性:Cl>S
D、钠在反应中失去的电子比铝少,故钠的金属性小于铝的金属性
4.MnO2和Zn是制造干电池的重要原料,工业上用软锰矿和闪锌矿联合生产MnO2和Zn的基本步骤为: ⑴ 软锰矿、闪锌矿与硫酸共热: MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+
S+2H2O。 ⑵ 除去反应混合物中的不溶物
 ⑶ 电解混合液MnSO4+ZnSO4+2H2O M MnO2+Zn+2H2SO4 下列说法不正确的是
⑶ 电解混合液MnSO4+ZnSO4+2H2O M MnO2+Zn+2H2SO4 下列说法不正确的是
A.硫酸在生产中可循环使用 B.步骤⑴中每析出12.8g S沉淀共转移0.8mol电子
C.电解时MnO2在阳极处产生 D.步骤⑴中MnO2和H2SO4都是氧化剂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com