
题目列表(包括答案和解析)
8、某固定容积的密闭容器中,存在下列化学平衡. aA(g) bB(g)+cC(g),
bB(g)+cC(g),
在温度不变的条件下,向容器中再充入一定量的A物质,重新达到平衡时,判
断在下列情况下有关物质量的变化趋势 (在下列空白中填写“增大”“减小”或“不变”) (1)当a=b+c时,B的物质的量分数(2)当a>b+c时,A的物质的量分数 (3)当a<b+c时,A的转化率
A(1)减小(2)不变(3)减小 B(1)不变 (2)减小 (3)增大
C ⑴ 不变 ⑵减小 ⑶减小 D(1)减小(2)不变 (3减小)
7、若要将下面装置改成可随时控制反应和停止的气体发生装置,则需在试管
里增设一带小孔隔板,你认为隔板应装在 A a处 B b处 C c处 D 任意处
6、 NO2、NH3、O2组成的混合气体,一定条件下完全反应生成N2和H2O,则原混合气体中NO2、NH3、O2的体积比可能是(不考虑二氧化氮与四氧化二氮的转化)
A、2∶4∶1 B、2∶1∶2 C、1∶2∶1 D、1∶4∶3
NO2、NH3、O2组成的混合气体,一定条件下完全反应生成N2和H2O,则原混合气体中NO2、NH3、O2的体积比可能是(不考虑二氧化氮与四氧化二氮的转化)
A、2∶4∶1 B、2∶1∶2 C、1∶2∶1 D、1∶4∶3
5、有关下列三个化学反应的叙述,正确的是
①2H2S+SO2=3S+2H2O ②S+2H2SO4(浓)=3SO2↑+2H2O
③3S+6KOH=2K2S+K2SO3+3H2O A.反应①说明SO2能与酸反应,具有碱性氧化物的性质 B.反应②改用稀H2SO4,则能放出H2 C.反应②和③说明S具有两性元素的性质 D.反应③说明S既有氧化性又有还原性
4、有人认为NO2可以称为混合酸酐。下列化学方程式所代表的反应中你认为能正确描述NO2是混合酸酐的化学方程式是 ①2NO2+2NaOH==NaNO3+NaNO2+H2O ②2NO2+H2O==HNO2+HNO3 3HNO2==HNO3+2NO↑+H2O ③NO2+NO+2NaOH==2NaNO2+H2O A.①②③ B.②③ C.①③ D.①②
3、金属铁可分别与卤素单质化合成卤化铁,当把一定量的铁粉与碘粉混合一起研磨,生成一种Fe3I8的化合物,根据元素化合物知识,试推断在此产物中的铁元素化合价是 A 、+2 B、+3 C、+2、+3都有 D、无法判断
2、某碱式盐的化学式为Mg(1+x)(CO3)x(OH)2取1.55 g该固体恰好与10 mL 4mol·L-1硝酸完全反应,所得溶液仅为Mg(NO3)2溶液,则x值为 A.1 B.2 C.3 D.5
1、下列化学用语表示错误的是
A.次氯酸电子式 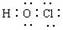 B.羟基电子式
B.羟基电子式 C.镁离子结构示意图
C.镁离子结构示意图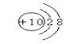 D.氨分子结构
D.氨分子结构
11.在1 L密闭容器中,把1 mol A和1 mol B混合发生如下反应:
3A(g)+B(g) xC(g)+2D(g),当反应达到平衡时,生成0.4
mol D,并测得C的平衡浓度为0.4 mol/L,通过计算完成下列问题:
xC(g)+2D(g),当反应达到平衡时,生成0.4
mol D,并测得C的平衡浓度为0.4 mol/L,通过计算完成下列问题:
(1)在该平衡下,在保持压强不变时,向该容器内充入氦气,则该平衡向 (填写“正向移动”、“逆向移动”、“不移动”)
(2)x的值为 ; (3)平衡时A的转化率为 ;
(4)如果加入0.2mol的C、 0.2molD、0.9molB和0.7molA充入到原来容器内,保持原来的条件不变,则达到平衡时B的物质的量浓度是 。
10. 实验室用下图所示的装置制取溴化亚铁。其中,A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管,e是两只耐高温的瓷夹,其中共盛有56g细铁粉。实验开始时先将铁粉加热至600-700℃,然后将干燥、纯净的CO2气流通入D中,E管中的物质开始反应,不断地将d中的液溴滴入100-120℃的D中,经过几小时的连续反应后在不锈钢管一端沉积有黄绿色鳞片状溴化亚铁80g。
实验室用下图所示的装置制取溴化亚铁。其中,A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管,e是两只耐高温的瓷夹,其中共盛有56g细铁粉。实验开始时先将铁粉加热至600-700℃,然后将干燥、纯净的CO2气流通入D中,E管中的物质开始反应,不断地将d中的液溴滴入100-120℃的D中,经过几小时的连续反应后在不锈钢管一端沉积有黄绿色鳞片状溴化亚铁80g。
(1)若导入的CO2不干燥,会在E中发生副反应,其化学方程式为 。
(2)在A中盛有CaCO3,a中盛有6mol·L-1盐酸。为使A中产生的CO2在进入D之前既干燥又纯净,B、C处采用相同的玻璃仪器,其仪器名称为 ;
B盛有的试剂是: ;C盛有的试剂是: .
(3)实验时,D和E的橡胶塞为什么最好用铝箔包住?
(4)反应过程中要不断地通入CO2,其主要作用是: 。
(5)E中在加热时进行的反应是:2Fe+3Br2=2FeBr3,2FeBr3=2FeBr2+Br2↑。此实验中溴化亚铁的产率为 。(保留到小数点后一位)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com