
题目列表(包括答案和解析)
7. (2000年春)在一定温度下,反应A2(g)+B2(g) 2AB(g) 达到平衡的标志是( )
(2000年春)在一定温度下,反应A2(g)+B2(g) 2AB(g) 达到平衡的标志是( )
A.单位时间内生成n mol 的A2同时生n mol AB B.容器内的总压强不随时间变化
C.单位时间内生成2n mol 的AB同时生n mol 的B2
D.单位时间内生成n mol 的A2同时生n mol 的B2
6.
 将固体NH4I置于密闭容器中,在某温度下发生下列反应:NH4I(s) NH3(g)+HI(g),2HI(g) H2(g)+I2(g)。当反应达到平衡时c(H2)=0.5 mol·L-1,c(HI)=4 mol·L-1,则NH3的浓度为( )
将固体NH4I置于密闭容器中,在某温度下发生下列反应:NH4I(s) NH3(g)+HI(g),2HI(g) H2(g)+I2(g)。当反应达到平衡时c(H2)=0.5 mol·L-1,c(HI)=4 mol·L-1,则NH3的浓度为( )
A.3.5mol·L-1 B.4 mol·L-1 C.4.5 mol·L-1 D.5 mol·L-1
5. 在一个固定容积的密闭容器中,加入m mol A和n mol B,发生下列反应:mA(g)+nB(g) pC(g)平衡时C的浓度为v mol·L-1。若维持容器体积和温度不变,起始时放入a
在一个固定容积的密闭容器中,加入m mol A和n mol B,发生下列反应:mA(g)+nB(g) pC(g)平衡时C的浓度为v mol·L-1。若维持容器体积和温度不变,起始时放入a
mol A,b mol B ,c mol C,要使平衡后C的浓度仍为v mol·L-1,则a、b、c须满足的关系是 A.a : b : c= m : n : p
B.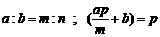
C.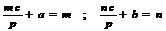 D.
D.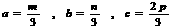
4. 在一定条件下,在容积为2L的密闭容器中,将2mol L气体和3mol M气体相混合,发生如下反应:2L(g)+3M(g) xQ(g)+3R(g),该反应达到平衡时,生成2.4mol
R,并测得Q的浓度为0.4mol·L-1。下列有关叙述正确的是( )
在一定条件下,在容积为2L的密闭容器中,将2mol L气体和3mol M气体相混合,发生如下反应:2L(g)+3M(g) xQ(g)+3R(g),该反应达到平衡时,生成2.4mol
R,并测得Q的浓度为0.4mol·L-1。下列有关叙述正确的是( )
A.x的值为2 B.混合气体的密度增大
C.平衡时M的浓度为0.3mol·L-1 D.L的转化率为80%
3. 在一密闭容器中,用等物质的量的A和B发生如下反应:A(g)+2B(g) 2C(g)反应达到平衡时,若混合气体中的A和B的物质的量之和与C的物质的量相等,则这时A的转化率为
在一密闭容器中,用等物质的量的A和B发生如下反应:A(g)+2B(g) 2C(g)反应达到平衡时,若混合气体中的A和B的物质的量之和与C的物质的量相等,则这时A的转化率为
A.40% B.50% C.60% D.70%
2. 把3mol P和2.5mol Q置于2L密闭容器中,发生如下反应:3P(g)+Q(g) xM(g)+2N(g),5min后达到平衡生成1mol N,经测定M的平均速率是0.1mol·L-1· 0.1mol-1,下列叙述错误的是( )
把3mol P和2.5mol Q置于2L密闭容器中,发生如下反应:3P(g)+Q(g) xM(g)+2N(g),5min后达到平衡生成1mol N,经测定M的平均速率是0.1mol·L-1· 0.1mol-1,下列叙述错误的是( )
A.P的平均反应速率为0.15mol·L-1·0.1mol-1 B.Q的转化率为25%
C.Q的平衡浓度为1mol·L-1 D.x是2
1.在容器中充入SO2和只由18O原子组成的氧气(18O2) ,在一定条件下达到平衡时,18O存在于( )
A.只存在于中O2 中 B.只存在于O2和SO3中
C.只存在于SO2和SO3中 D.SO2、SO3和O2中都有可能存在
11、 (10分) 物质的转化关系如下图所示(有的
反应可能在水溶液中进行)。其中A为化合
物,甲可由两种单质直接化合得到,乙为金
属单质,G为酸,乙在G的浓溶液中发生钝 化。 (1)若A为黄色固体,C能使品红试液褪色,D的
水溶液中加入HNO3酸化的AgNO3溶液有白色沉淀生成。则 ①工业上反应I在 中进行,反应Ⅲ在 (均填设备名称)中进行。 ②由两种单质直接化合得到甲的反应条件是 或 。 ③反应I的化学方程式是 。 (2)若甲为淡黄色固体,D、F的溶液均呈碱性,用两根玻璃棒分别蘸取A、G的浓溶液并使它
们接近,有大量白烟生成。则①D的溶液与乙反应的离子方程式是 。 ②若1.7gA与O2反应生成气态的B和C时放出22.67 kJ热量,写出该反应的热化学方程式
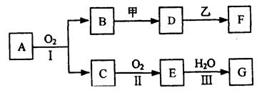
10、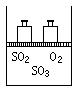 I(6分)如图,将4molSO2和2 mol O2混合置于体积可变的等压密闭容器中,
I(6分)如图,将4molSO2和2 mol O2混合置于体积可变的等压密闭容器中,
在一定温度下发生如下反应2SO2(g)+O2(g)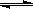 2SO3(g);ΔH<0。该反应达
2SO3(g);ΔH<0。该反应达
到平衡状态时,测得气体的总物质的量为4.2 mol。试回答: (1)在该平衡状态时n(SO3)=______________________; (2)若起始时加入1.2 mol SO2、0.6 mol O2和x mol SO3,达到平衡状态后,各
气体的体积分数与上述平衡状态相同,x的取值为____________________________; (3)若反应开始时的V(逆)>V(正),达到上述平衡状态时,气体的总物质的量仍为4.2 mol。
则起始时n(SO3)的取值范围是________________________________。
II(7分)在一定温度下,有1mol N2气体和3mol H2气体发生下列反应:
N2(g)+3H2(g) 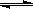 2NH3(g);ΔH<0
(1)若在相同温度下,分别在1L定压密闭容器中和1L定容容器中反应(密闭):
哪个容器中的反应先达到平衡? 答: 哪个容器中的N2的转化率高? 答:
2NH3(g);ΔH<0
(1)若在相同温度下,分别在1L定压密闭容器中和1L定容容器中反应(密闭):
哪个容器中的反应先达到平衡? 答: 哪个容器中的N2的转化率高? 答:
(2)若在上述定压密闭容器中,反应已达到平衡时,再加入0.5mol氩气,则N2的转化率会起
什么变化?正反应速度与原平衡相比,有无变化,简答理由。
9、(10分)(1)第二周期非金属元素的氢化物分子中去掉一个氢原子,将剩余的基团相互连接(相同或不同的基团均可以)能形成一系列新的物质。例如,二个相同的-CH3连接成CH3-CH3,相个相同的-OH连接成H2O2。将二个相同的___________连接成分子A,已知1摩尔A能与2摩尔HCl发生中和反应生成正盐,则A分子式是______________,A与过量盐酸形成盐的水溶液呈_________(酸、碱、中)性。在氧化还原反应中与H2O2相似,既可以作氧化剂,又可作还原剂。试从化合价态分析产生这种情况的原因是
___________ _____________。
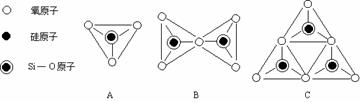
⑵原硅酸根离子SiO44- 中的Si 原子被4个O 原子所包围,可以用图A来表示其空间构型。你认为SiO44-的空间构型为 。图B 表示 (写化学式)的空间构型,图C表示 (写化学式)的空间构型。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com