
题目列表(包括答案和解析)
2.右表为元素周期表短周期的一部分,下列有关A、B、C、D四种元素的叙述正确的是
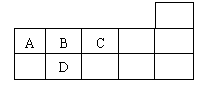 A.原子半径大小比较为A>B>C>D
A.原子半径大小比较为A>B>C>D
B.生成的氢化物稳定性为A>B>C>D
C.A与C形成的阴离子可能有AC32-、A2C42-
D.A、B、C、D的单质常温下均不导电
1.最近日本科学家确认世界上还存在的另一种“分子足球”N60,它与C60的结构相似。下列说法正确的是
A.N60是一种新型化合物 B.N60和14N都是氮的同位素
C.N60和N2是同素异形体 D.N60和N2是同系物
13.(8分) 能源是人类社会发展进步的物质基础。在当代,能源同信息、材料一起构成了现代文明的三大支柱。
(1)为了降低汽车尾气对大气的污染,江苏有关部门拟用甲醇替代液化石油气作为公交车的燃料。已知:在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热akJ。请写出表示甲醇燃烧热的热化学方程式。
(2)测定工业甲醇中CH3OH的质量分数可按下法:取0.1000g工业甲醇样品,以适量H2SO4酸化后,加入20.00mL 0.2000mol/L的K2Cr2O7溶液,再用0.3000mol/L (NH4)2Fe(SO4)2标准溶液滴定,耗去此标准液20.00mL时,刚好到达滴定终点。
已知:CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O
①写出H2SO4酸化的K2Cr2O7溶液与(NH4)2Fe(SO4)2溶液反应的离子方程式。
②求此工业甲醇中CH3OH的质量分数。
12.(14分)A、B、C、D、E、F、G是由短周期元素组成的七种物质,其中B、C、F是单质;常温下B、C、E为气体;A物质的焰色反应呈黄色。(下图中反应②的部分产物未表示出来。)
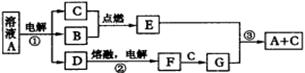
根据上图所示转化关系回答: (1)经测定G属于离子化合物,其电子式为___________。 (2)写反应②的电极反应式: 阳极______ ; 阴极 。 (3)反应③的化学方程式为 ___________ 。
(4)反应①的离子方程式为___________ 。
(5)这七种物质中含有共价键的有___________ (用化学式回答)
11.(10分) 配制500 mL0.2 mol.L-1的FeSO4 溶液,实验操作步骤有:
①在天平上称取a克绿矾(FeSO4 ·7H2O),将它放在烧杯中,用适量蒸馏水使
其完全溶解 ②将所得溶液沿玻璃棒注入500 mL容量瓶中
③继续向容量瓶中加水至液面距刻度线1-2cm处,改用胶头滴管加蒸馏水
至液面底部与刻度线相切
④用少量水洗涤烧杯和玻璃棒2-3次,每次洗液都转入容量瓶 ⑤将容量瓶塞紧,充分摇匀
填写下列空白: (1)a克绿矾的实际质量为 克
(2)上述操作步骤的正确顺序为 。
(3)若配制时遗漏步骤④,会使所配溶液的浓度 (填“偏高”、“偏低”或“无影响”)。(4)若加蒸馏水时不慎超过刻度线,处理方法是
若操作步骤②时有溶液溅在窖量瓶外,处理方法是
10.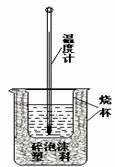 (10分)实验室利用如右图装置进行中和热的测定。回答下列问题:
(10分)实验室利用如右图装置进行中和热的测定。回答下列问题:
①该图中有两处未画出,它们是 、 ;
②在操作正确的前提下提高中和热测定的准确性的关键是 ;
③如果用0.5 mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将 (填“偏大”、“偏小”、“不变”);原因是 。
9.科学家预言,C3N4晶体很可能具有比金刚石还大的硬度,且每个原子最外层均满足8电子稳定结构。则下列关于C3N4晶体的说法正确的是:
A.C3N4 晶体可能是分子晶体,晶体微粒间通过共价键结合
B.C3N4 晶体可能是原子晶体,具有较高的硬度
C.C3N4 晶体中每个C原子连接4个N原子,而每个N原子连接3个C原子
D.C3N4 晶体中N的最外层电子均参与成键
8.FeS2在空气中充分燃烧的化学方程式为4FeS2 + 11O2 2Fe2O3 + 8SO2,若agFeS2在空气中充分燃烧,并转移N个电子,则阿伏加德罗常数(NA)可表示为
A.120N/a B.120a/11N C.11a/120N D.120N/11a
7.下列离子反应方程式正确的是
A.KHCO3的水解:HCO3-+H2O H3O++CO32-
H3O++CO32-
B.NaHSO4溶液与Ba(OH)2溶液混合呈中性:2HSO4-+Ba2++2OH-=BaSO4↓+SO42-+2H2O
C.将少量铁粉加入到过量的稀硝酸中:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O
D.碳酸氢钙溶液中加入足量石灰水:Ca2++HCO3-+OH-= CaCO3↓+H2O
6.某无色溶液与NH4HCO3作用能产生气体,此溶液中可能大量共存的离子组是:
A.Cl-、Mg2+、H+、Cu2+、SO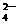 B.Na+、Ba2+、NO3-、OH
B.Na+、Ba2+、NO3-、OH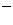 、SO
、SO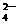
C.MnO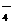 、K+、Cl-、H+、SO
、K+、Cl-、H+、SO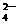 D.K+、NO
D.K+、NO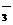 、SO
、SO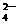 、OH-、Na+
、OH-、Na+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com