
题目列表(包括答案和解析)
11.在一定温度下,容器内某一反应中M、N的物质的量随
时间变化的曲线如图所示,下列表述中正确的是( )
A.反应的化学方程式为:2M N
N
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
10.2004年9月莫斯科时间3日下午1时左右,俄军特种部队成功解救人质,被武装分子占
据的俄罗斯南部学校中的全部人质都已被疏散出学校体育馆。一桩震惊世界的大规模绑
架案就此告一段落。其中在解救的过程中所使用的气体芬太奴,是医疗中使用的一种速
效强力镇痛药。它可以通过抑制呼吸和血液循环进行止痛,使人感觉麻木,大量使用能
使人昏迷乃至死亡。芬太奴的结构简式如下图所示,下列关于芬太奴的说法正确的是
 ①芬太奴在一定条件下可发生水解反应
①芬太奴在一定条件下可发生水解反应
②该分子中所有原子可以共平面
③芬太奴属于苯的同系物
④芬太奴的分子式为C20H24N2O
 A.①④ B.①② C.②③ D.③④
A.①④ B.①② C.②③ D.③④
9.将 mL NO、
mL NO、 mL NO2、
mL NO2、 mL O2混合于同一试管里,将试管口倒置于水中,充分反应
mL O2混合于同一试管里,将试管口倒置于水中,充分反应
后试管内气体全部消失,则 对
对 、
、 的函数关系式是
的函数关系式是
A. B.
B.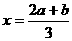 C.
C. D.
D.
8.苯氯乙酮中毒后,能够使人失去行动能力,所以常作为警用控暴剂。已知其分子中苯环
上含有乙酮基(-COCH3),则符合上述条件的苯氯乙酮共有
A.3种 B.2种 C.4种 D.5种
(HOOCCH2)2NCH2CH2N(CH2COOH)2,下列说法正确的是
A.EDTAFeNa铁为+3价 B.EDTAFeNa中铁为+2价
C.EDTAFeNa溶液显强碱性 D.人体血液中血红蛋白中铁显+3价
7.已知在25℃,101 kPa下,1 g C8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40 kJ
热量。表示上述反应的热化学方程式正确的是
A. ;
; kJ·mol
kJ·mol
B. ;
; kJ·mol
kJ·mol
C. ;
; kJ·mol
kJ·mol
D. ;
; kJ·mol
kJ·mol
13.时钟反应或振荡反应提供了迷人课堂演示实验,也是一个活跃的研究领域。测定含I-浓度很小的碘化物溶液时,利用振荡反应进行化学放大,以求出原溶液中碘离子的浓度。主要步骤是
①在中性溶液中,用溴将试样中I-氧化成IO3-,将过量的溴除去
②再加入过量的碘化钾,在酸性条件下,使IO3-完全转化成I2
③将②中生成的碘完全萃取后,用肼将其还原成I-,方程式为
H2N-NH2+2I2→4I-+N2↑+4H+
④将生成的I-萃取到水层后用①法处理。
⑤将④得到的溶液加入适量的KI溶液,并用硫酸酸化。
⑥将⑤反应后的溶液以淀粉作指示剂,用Na2S2O3标准溶液滴定,方程式为:
2 Na2S2O3+I2→Na2S4O6+2NaI。
经过上述放大后,则溶液中I-浓度放大为原溶液中I-浓度的(设放大前后溶液体积相等):
A.2倍 B.4倍
C.6倍 D.36倍
10.已知常温常压下,N2(g)和H2(g)反应生成2 mol NH3(g),放出92.4 kJ热量,在同温同压下向密闭容器中通入1 mol N2和3 mol H2,达平衡时放出热量为Q1 kJ;向另一体积相同的容器中通入0.5 mol N2和1.5 mol H2、1 mol NH3,相同温度下达到平衡时放出热量为Q2 kJ,则下列叙述正确的是
A.Q2<Q1<92.4 B.2Q2=Q1=92.4
C.Q1<Q2<92.4 D.Q1=Q2<92.4
 11.如图是元素周期表前六周期的一部分,关于元素X、Y、Z的叙述正确的是
11.如图是元素周期表前六周期的一部分,关于元素X、Y、Z的叙述正确的是
①X的气态氢化物与Y最高价氧化物对应的水化物能发生反应生成盐
②X、Y、Z的气态氢化物的水溶液的酸性X<Y<Z
③Z的单质常温下的是液体,可与铁粉反应
④Z的原子序数比Y大19
⑤Z所在的周期中含有32种元素
A.只有③ B.只有①④
C.只有①②③④ D.①②③④⑤
 12.有机物甲在一定条件下能发生水解反应生成两种有机物,乙中①~⑥是标出该有机物分子中不同的化学键,在水解时,断裂的键是
12.有机物甲在一定条件下能发生水解反应生成两种有机物,乙中①~⑥是标出该有机物分子中不同的化学键,在水解时,断裂的键是
A.①、④ B.③、⑤
C.②、⑥ D.②、⑤
9.下列反应的离子方程式正确的是
A.二氧化硫气体通入到漂白粉溶液中:
Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
B.碳酸氢镁溶液中加入过量的澄清石灰水:
Mg2++2HCO3-+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O
C.H218O中投入Na2O2固体:
2H218O+2O22-=4OH-+18O2↑
D.向硫酸氢钠溶液中滴入氢氧化钡溶液至pH=7:
Ba2++OH-+H++SO42-=BaSO4↓+H2O
8.NA代表阿伏加德罗常数,下列说法正确的是
A.在标准状况下,22.4 L辛烷完全燃烧,生成二氧化碳分子数为8 NA
B.46 g二氧化氮和46 g四氧化二氮含有的原子数均为3 NA
C.1 mol氦气和氢气的混合气体含有的原子个数为2 NA
D.0.1 mol/L的100 mL H2SO3溶液中,含有的离子数约为0.03 NA
A.铝质轻,便于运输、贮存,且安全
B.在地球上,铝矿资源比较丰富
C.铝燃烧时放出的热量大,且燃烧后新产物对环境的污染容易得到有效的控制
D.现代电冶铝的工业技术已为铝作为新能源奠定了重要基础
7.四支试管分别充满O2、NO2、Cl2、NH3四种气体,把它们分别倒立于盛有下列各种液体的水槽中,发生的现象如下图所示,其中充满Cl2的试管是

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com