
题目列表(包括答案和解析)
8.在氧化还原反应中,下列叙述正确的是 ( )
A.氧化剂本身被还原,生成氧化产物
B.物质在变化中失去电子,此物质是氧化剂
C.发生电子转移的反应即是氧化还原反应
D.还原剂在反应时所含元素的化合价降低
7.按金属活动性顺序由前到后考虑,下列说法中正确的是 ( )
A.单质的还原性逐渐减弱 B.原子的失电子能力逐渐增强
C.对应离子的氧化性逐渐减弱 D.金属原子失电子越多,还原性越强
5.下列含有非极性键的共价化合物是 ( )
A.HCl B.Na2O2 C.C2H2 D.CH4
|
C.2Na+2H2O==2NaOH+H2↑ D.Cl2+H2O==HCl+HClO
4.实现下列各组物质的变化时,需克服的作用力完全相同的是 ( )
A.硫磺和氢氧化钠的熔化 B.二氧化硅和生石灰的熔化
C.碘和萘的升华 D.氯化钠和铁的熔化
3.下列物质属于弱电解质的是 ( ) A.氯化铝 B.铜 C.酒精 D.水
2.下列化学式既能表示物质的组成,又能表示物质的一个分子的是 ( )
A.NaOH B.C C.SiO2 D.CO2
1.闪电时空气中有臭氧生成,下列说法正确的是 ( )
A.O2和O3互为同位素 B.O2比O3稳定
C.等体积的O2和O3具有相同的质子数D.O2与O3的相互转变是物理变化
28.(14分)有X、Y、Z和W四种元素。已知:①X、Y、Z属同一短周期,其离子以X2+、
Y3+、Z-的形式存在。②W和Z组成化合物WZ3溶液遇苯酚呈紫色。请回答:
(1)Z的最高价氧化物对应水化物的名称为 。
(2)X的单质在M氧化碳中燃烧的化学方程式为 。
(3)Y的单质可用于冶炼金属锰,写出Y与二氧化锰反应的化学方程式 ,
Y的最高价氧化物对应的水化物既可溶于强酸又可溶于强碱,请用电离平衡理论解释其原因 。
(4)当有28.0 g W组成的单质,在加热条件下与足量水完全反应,则生成气体标准状况下
的体积为 L。
(5)我国陆地上冶炼X的主要流程如图14所示

已知当有 lmolX的氧化物参加反应时,有2 mol电子转移且生成三种产物,则步骤②反
应的化学方程式为 。
(6)在新生代的海水中有一种细菌,它们提取海水中W2+,利用酶为催化剂把W2+转化为它们的皮鞘(可用W2O3表示其中W);该反应中的另一种反应物二氧化碳转化为甲醛,请用离子方程式表示上述转化过程(W用具体元素符号表示) 。

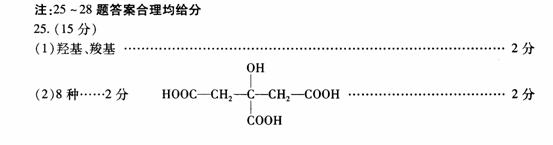
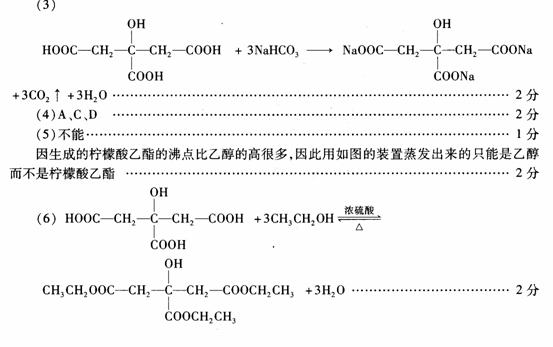


27.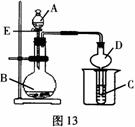 (l6分)某课外小组利用如图13装置进行相关实验,请回答下列问题。
(l6分)某课外小组利用如图13装置进行相关实验,请回答下列问题。
(1)仪器D在实验中的作用是 ,
实验前检查整套装置气密性的方法是
。
(2)若将A容器中的液体逐滴加人到B容器的固体中,产生气体,该气体可以是(填化学式,写出4种即可) 。
(3)若 A中装有浓盐酸,B中装有高锰酸钾固体,C容器中装有淀粉碘化钾溶液,旋开 E
后,一段时间C中溶液变蓝色,写出B中发生反应的化学方程式
;
(4)工业上用电解饱和氯化钠溶液的方法制取氯气,写出该反应的化学方程式
;电解过程中在阴极附近可得到(填名称),生成的原因是 ;
若电解池中装有 26.0%的氯化钠溶液 2.0 L(密度为1.2g/mL),当在标准状况下生成112.0L的氯气时(假设产生氯气全部放出),电解池溶液中氯化钠溶质的质量分数为 。
26.(15分)二氧化硫是污染大气形成酸雨的主要有害物质之一,如果了解二氧化硫的性质,它在我们的生活中也有广泛的用途。
(1)下列可产生二氧化硫污染大气的是 。(填序号)。
A.含硫矿石的冶炼 B.大量化石燃料的燃烧
C.大量烟花爆竹的燃放 D.硫酸厂排放的工业尾气
(2)某课外小组采集了一份雨水样品,每隔一段时间测定该雨水样品的pH变化数据如下
|
测试时间段 |
0 |
1 |
2 |
3 |
4 |
|
雨水的pH |
4.73 |
4.62 |
4.56 |
4.55 |
4.55 |
分析雨水样品PH变化的原因(用文字和化学方程式说明)
。
(3)某实验小组欲探究二氧化硫的化学性质,设计如下实验,请完成实验报告。
|
序号 |
二氧化硫的性质 |
主要操作和现象 |
化学方程式 |
|
① |
|
 将二氧化硫通入装有品红溶液的试管中,品红由红色变为无色 将二氧化硫通入装有品红溶液的试管中,品红由红色变为无色 |
|
|
② |
氧化性 |
|
|
|
③ |
|
将二氧化硫通入装有新制氯水的试管中,氯水由浅黄绿色变为无色 |
|
(4)目前,我国大都使用以亚硫酸类化合物为主的漂白剂,通过产生的二氧化硫而使食品漂白。我国《食品添加使用卫生标准》规定:“亚硫酸用于蜜饯、葡萄糖中的残留量(以二氧化硫计)不超过0.05 g/kg”。目前通常采用滴定法测定食品中残留二氧化硫的含量。具体实验方法主要是:样品经处理后,加入氢氧化钾使残留的二氧化硫以亚硫酸盐的形式固定,再加入硫酸使二氧化硫游离,用碘标准溶液滴定二氧化硫。在滴定时用 (填名称)作指示剂,滴定终点的现象是 。
(5)现有100 g二氧化硫含量超标的蜜饯样品经过处理后,配制成1000mL溶液,取出50 mL溶液,分别与氢氧化钾、硫酸反应,再用碘标准溶液 5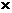 103mol/L滴定,消耗碘标准溶液5 mL,则样品中二氧化硫的含量(g/kg)为
(保留二位小数)。
103mol/L滴定,消耗碘标准溶液5 mL,则样品中二氧化硫的含量(g/kg)为
(保留二位小数)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com