
题目列表(包括答案和解析)
24、已知物质A显酸性,请根据以下框图回答问题:
 F为七原子组成的环状结构。
F为七原子组成的环状结构。
(1)A的结构简式为
(2)①②③的反应类型分别为 、 、
(3)化合物B中含有官能团的名称是
(4)D和E生成F的化学方程式
(5)G生成H的化学方程式
(6)写出C的同分异构体中属于酯类物质的结构简式:(任写2种)
________________________、_________________________
23、已知:A是FeSO4,G是硫酸铁,且C和D,F和H元素组成相同。反应过程中产生的水在图示中已略去。
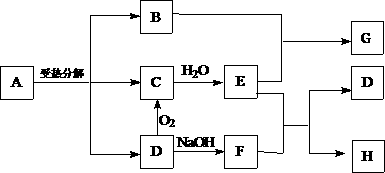
回答下列问题:
(1)A受热分解的化学方程式为:____________________________________
(2)检验F中所含阴离子的方法是:_____________________________________
(3)B跟E的稀溶液反应的离子方程式是:_______________________________
22、已知X、Y、Z、L、M、N是元素周期中前20号的五种元素,它们的原子序数依次增大。X和Y可形成常见化合物YX4,一个YX4分子电子总数为10。L原子的最外层电子数是核外电子总数的3/4。NY2加水生成Y2X2和化合物D。试回答:
(1)、X单质和Z单质在一定条件下可生成化合物E。
①、E的电子式为 ,化学键类型为 ,晶体类型为
②、工业上制取E的化学方程式为(注明反应条件)
______________________________________________________________________
③、实验室制取E的化学方程式为
(2)、由M、Y、L三种元素组成的物质焰色反应显浅紫色,向其溶液中滴入酚酞溶液,溶液显红色,原因是(用离子方程式表示)___________________________
若再向溶液中滴入过量的氯化钙溶液,观察到的实验现象是___________________
原因是(用离子方程式表示)______________________________________
(3)、NY2与水反应生成Y2X2和化合物D的化学方程式为:
______________________________________________________________________
21、已知过量氨气跟氯气可迅速反应生成氯化铵和氮气。当转移的电子总数为a个时,生成的氮气的物质的量b mol。
①写出该反应配平的化学方程式:
②该反应中参加氧化还原反应的氧化剂和还原剂的物质的量之比为
③阿伏加德罗数常数为(用含a、b的代数式表示)
20、为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球。
(1)实验时,为在E烧瓶中收集到NO,以便观察颜色,必须事先出去其中的空气。其中第一步实验操作为:__________________________________________
如何确定E中空气已被赶尽:______________________________________
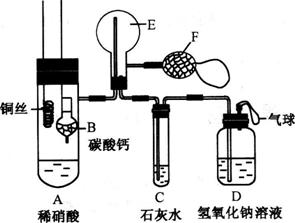
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的离子方程式为
(3)如何证明E中收集到的是NO而不是H2?
______________________________________________________________________
一段时间后,C中白色沉淀溶解,其原因是_________________________________
______________________________________________________________________
(4)装置D的作用是___________________________________________________
19、(1)、指出在使用下列仪器(已经洗涤干净)或用品时的第一步操作:
①石蕊试纸(检验气体):
②容量瓶:
(2)、某学生用已知质量y g的表面皿,准确称取w g NaOH固体。他在托盘天平的右盘上放(w+y)g砝码,在左盘的表面皿中加入NaOH固体,这时指针偏向右边,下面他的正确操作应该是:
使 。
若称取的w g NaOH刚好可配制0.5 mol· L-1NaOH溶液500 mL。在下列配制0.5 mol·L-1 NaOH溶液过程示意图中有错误的是(填操作序号) 。
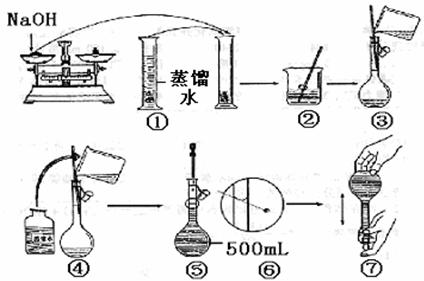
18、在容积不变的密闭容器中存在如下反应:
2SO2(g)+O2(g) 2SO3(g);△H<0
2SO3(g);△H<0
某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是:



I II III
A、图I研究的是t0时刻增大O2的浓度对反应速率的影响
B、图II研究的是t0时刻加入催化剂后对反应速率的影响
C、图III研究的是催化剂对平衡的影响,且甲的催化效率比乙高
D、图III研究的是温度对化学平衡的影响,且乙的温度较高
第Ⅱ卷(非选择题,共76分)
17、右图是2004年批量生产的笔记本电脑所用甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:
2CH3OH+3O2 2CO2+4H2O
下列说法正确的是:
A、右电极为电池的正极,b处通入的物质是空气
B、左电极为电池的负极,a处通入的物质是空气
C、负极反应式为:CH3OH+H2O-6e- CO2+6H+
D、正极反应式为:O2+4e- 2O2-
16、已知KHSO3溶液呈弱酸性。在0.1mol·L-1KHSO3溶液中,下列关系正确的是
A、c(K+)+c(H+)=c(HSO3-)+c(OH-)+c(SO32-)
B、c(HSO3-)+c(SO32-)=0.1 mol·L-1
C、c(SO32-)>c(H2SO3)
D、c(K+)=c(H2SO3)+c(HSO3-)+c(SO32-)

15、下列说法正确的是
A、离子半径:Ca+<S2-,原子半径:Na>Cl
B、从上到下,卤素的非金属性逐渐减弱,故氢卤酸的酸性依次减弱
C、因为氧化性:HClO>稀H2SO4,所以非金属性:Cl>S
D、钠在反应中失去的电子比铝少,故钠的金属性小于铝的金属性
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com