
题目列表(包括答案和解析)
9.已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图所示,下列说法正确的是
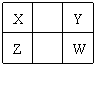 A.Z元素的原子半径可能比Y元素的小
A.Z元素的原子半径可能比Y元素的小
B.Z元素的最高化合价可能比Y元素的高
C.W的气态氢化物的稳定性一定比Y的强
D.Z的最高价氧化物的水化物的酸性一定比W的强
8.下列叙述中,结论(事实)和对应的解释(事实)均不正确的是
A、金刚石的熔沸点高于晶体硅,因为C一C键能大于Si一Si键能
B、稀有气体的晶体属于原子晶体,因为其组成微粒是原子,不存在分子间作用力
C、二氧化硅晶体中不存在简单的SiO2分子,因其晶体是含有硅氧四面体的空间网状结构
D、分子空间构型为正四面体结构的分子中化学键的键角不一定是109028’,因为键角还有可能为60°
7.下列有关热化学方程式的叙述中,正确的是
A、含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出 28.7 kJ的热量,则表示该反应中和热的热化学方程式为NaOH(aq)+HCl(aq)=NaC1(aq)+H2O(l);△H=十57.4 kl/mol
B、已知C(石墨,s)=C(金刚石,s);△H> 0,则金刚石比石墨稳定
C、已知2H2(g)十O2(g)=2H2O(g);△H=-483 6 kJ/mol,则H2的燃烧热为 241.8kl/mol
 D、已知
则△H1<△H2
D、已知
则△H1<△H2
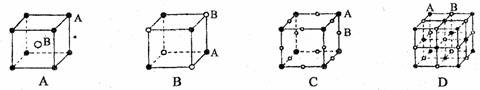
6.有四种晶体,其离子排列方式下图所示,其中化学式不属AB型的是
5.下列说法不正确的是(NA表示阿伏加德罗常数) A.标准状况下,11.2LCO和CO2的混合气体含有碳原子的数目为0.5NA
B.3mol氖气所含的原子数为3NA
C.0.5mol/L的Ca(NO3)2溶液中NO3-的浓度是1mol/L
D.1mol甲基(-CH3)所含的电子数为10NA
4.下列反应中,H2O作为还原剂的是 A.2Na2O2 + 2H2O = 4NaOH + O2↑ B.2F2+2H2O = 4HF+O2
C.NaH + H2O = NaOH + H2↑ D.Cl2+ H2O = HCl + HClO
3.下列说法正确的是 A.SiO2、NaCl、CO2三种化合物的晶体中都存在分子
B.等质量的O22-和O2-具有相同的离子数
C.铝单质既属于金属,又属于非金属
D.聚乙烯、明矾[KAl(SO4)2·12H2O]、盐酸都是化合物
2.关于物质的分类正确的是 A.SO2、CO2、NO2都是酸性氧化物
B.Na2O、Fe2O3、Mn2O7都是金属氧化物
C.HClO、HClO3、HClO4都是强酸
D.KOH、Ba(OH)2、Fe(OH)3都是强碱
1.2007年3月22日是第十五届“世界水日”。我国纪念“世界水日”和开展“中国水周”活动的宣传主题为“水利发展与和谐社会”。下列有关活动不符合这一主题的是
A、加强工业用水系统的环保改造,提高水的重复利用率
B、加强城市生活污水处理,坚持达标排放
C、加快产业结构调整,建立水资源节约型、环保型的国民经济体系
D、推广使用纯净水代替自来水作生活用水,以保障用水安全
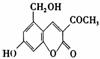 28、(10分)2006年5月,齐齐哈尔第二制药厂生产的假药“亮菌甲素注射液”导致多名患者
28、(10分)2006年5月,齐齐哈尔第二制药厂生产的假药“亮菌甲素注射液”导致多名患者
肾功能衰竭。“亮菌甲素”的结构简式为 ,它配以辅料丙二
|
成针剂用于临床。假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强
的毒性。请回答下列问题:
(1)“亮菌甲素”的分子式为 。
(2)丙二醇的分子式是C3H8O2,已知两个羟基连在同一个碳原子上的物质不存在。写出其属于醇类的同分异构体的结构简式 。
(3)下列有关“亮菌甲素”的叙述正确的是 (填序号)。
A.“亮菌甲素”能与H2发生加成反应
B.不能使酸性KMnO4退色
C.“亮菌甲素”分子中含氧官能团只有2种
D.1mol“亮菌甲素”最多与2molNaOH反应
(4)核磁共振仪可以测定有机物分子中处于不同化学环境的氢原子及相对数量。氢原子在分子中的化学环境不同,在核磁谱图中就处于不同的位置,化学环境相同的氢原子越多,波谱峰积分面积越大(或高度越高)。核磁共振氢谱分析,发现二甘醇分子中有3个吸收峰,其峰面积之比为2:2:1。又知二甘醇中C、O元素的质量分数相同,且H的质量分数为9.4%,1mol二甘醇与足量的金属钠反应生成1molH2。写出二甘醇与乙酸(按物质的量之比1:1)反应的化学方程式 。
29、(10分)下表为周期表的一部分,其中的字母代表对应的元素
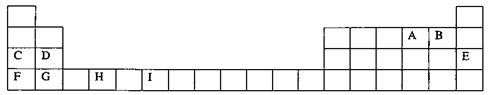
请回答下列问题:
(1)写出元素I的基态原子的价电子排布式 ;已知M2+离子3d轨道中有6个电子,试推出M元素位于周期表的 周期 族。
(2)请列举F的金属性比C强的实验事实: ,并用原子结构理论解释其原因:
。
(3)在标准状况下,根据M=m/n测定B的气态氢化物的相对分子质量,结果发现,测定结果总比理论值高,其原因是 。
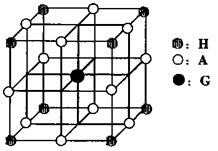
(4)H、A、G三种元素形成的晶体是一种矿物的主要成分,其晶胞结构如下图,则该晶体的化学式为 ;在该晶体中,G离子的配位数为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com