
题目列表(包括答案和解析)
18.pH相同的四种一元 酸A、B、C、D的溶液各20 mL,与过量Mg充分反应后,产生氢气的质量是D>C>A=B。下列说法正确的是:
①D的酸性最强 ②A与B的酸性最强且彼此相当 ③反应后原D溶液的pH最大 ④反应后原A和B溶液的pH最大 ⑤反应前D溶液的物质的量浓度最大 ⑥反应前四种溶液的物质的量浓度一样大
A.②③⑤ B.①④⑥ C.②④⑤ D.①③⑤
第II卷(共56分)
17.下列实验操作中错误的是
A.用分液漏斗分液时,下层液体从下口放出,上层液体从上口倒出
B.蒸发结晶时,应将溶液蒸干,并放在干燥器中冷却
C.无锈的细铁丝可以代替铂丝,做焰色反应的工具
D.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
16.根据相应的图象(图象编号与答案一一对应),判断下列相关说法正确的是
A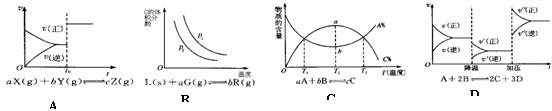 .密闭容器中反应达到平衡,t0时改变某一条件有如图所示,则改变的条件一定是加入催化剂
.密闭容器中反应达到平衡,t0时改变某一条件有如图所示,则改变的条件一定是加入催化剂
B.反应达平衡时,外界条件对平衡影响关系如图所示,则正反应为放热反应,且a>b
C.物质的百分含量和温度关系如图所示,则该反应的正反应为吸热反应
D.反应速率和反应条件变化关系如图所示,则该反应的正反应为放热反应,A、B、C是气体、D为固体或液体
15.下列反应的离子方程式正确的是
A. 次氯酸钙溶液中通入过量二氧化碳 Ca2++2ClO-+H2O+CO2
== CaCO3¯+2HClO
B. 硫酸亚铁溶液中加过氧化氢溶液 Fe2++2H2O2+4H+
== Fe3++4H2O
C. 用氨水吸收少量二氧化硫 NH3.H2O+SO2
== NH +HSO
+HSO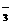 D. 硝酸铁溶液中加过量氨水Fe3++3NH3.H2O ==
Fe(OH)3¯+3NH
D. 硝酸铁溶液中加过量氨水Fe3++3NH3.H2O ==
Fe(OH)3¯+3NH
14. 将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是
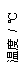
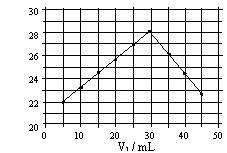 A. 做该实验时环境温度为22℃
A. 做该实验时环境温度为22℃
B. 该实验表明化学能可能转化为热能
C. NaOH溶液的浓度约为1.0mol/L
D. 该实验表明有水生成的反应都是放热反应
13.依照阿佛加德罗定律,下列叙述正确的是 A . 同温同压下两种气体的体积之比等于摩尔质量之比
B. 同温同压下两种气体的物质的量之比等于密度之比 C. 同温同压下两种气体的质量之比等于密度之比 D. 同温同体积下两种气体的物质的量之比等于压强之比
12.几种短周期元素的原子半径及主要化合价见下表:
|
元素代号 |
L |
M |
Q |
R |
T |
|
原子半径/nm |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
|
主要化合价 |
+2 |
+3 |
+6、-2 |
+2 |
-2 |
下列叙述正确的是
A.在相同条件下,单质与同浓度稀盐酸反应的速率:L>R
B.只有T形成的化合物具有两性
C.Q、T两元素的氢化物分子间都存在氢键
D.L、Q形成的简单离子核外电子数相等
11.在标准状况下,将V L气体A(摩尔质量为M g·mol-1)溶于0.1L水中,所得溶液密度为d g·cm-3,则该溶液的物质的量浓度为
A.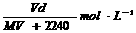
 B.
B.
C.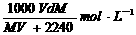 D.
D.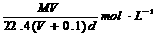
10.下表为元素周期表短周期的一部分。下列有关A、B、C、D、E五种元素的叙述中,错误的是
A.A与B形成的阴离子可能有AB32-、A2B42-
B.E的氢化物的稳定性小于C 的氢化物的稳定性
C.D在适量的B中燃烧的产物为DB3
D.A与E形成的分子是非极性分子
9.下列各组离子,在指定的环境中一定能大量共存的是
A.滴加石蕊试液显红色的溶液:Fe3+、NH4+、C1-、SCN-
B.含有大量HCO3-的溶液:NH4+、Ca2+、Mg2+、I-
C.在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、NO3-
D.含有大量ClO-的溶液:H+、Mg2+、I-、SO42-
|
|
|
|
|
|
|
A |
|
B |
C |
|
|
|
|
D |
E |
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com