
题目列表(包括答案和解析)
14. 常温下,0.1 mol·L-1某一元酸(HA)溶液中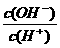 =1×10-8,下列正确的是
=1×10-8,下列正确的是
A.该溶液中由水电离出的c(H+)=1×10-11 mol·L-1
B.0.1mol/L的NaA溶液中的离子浓度大小关系为:
c(Na+)>c(A-) >c(H+)>c(OH-)
C.该溶液中水的离子积常数为1×10-22
D.用0.1 mol·L-1NaOH溶液V1 L 与0.1 mol·L-1该一元酸(HA)V2 L溶液混合,若混合溶液的pH = 7,则V1<V2
13. 能正确表示下列反应的离子方程式是
A.饱和碳酸氢钙溶液中加入饱和氢氧化钙溶液
Ca2+ + HCO3- + OH- = CaCO3↓+ H2O
B.氯化亚铁溶液中加入硝酸
Fe2+ + 4H+ + NO3- = Fe3+ + 2H2O + NO↑
C.氯气通入冷的氢氧化钠溶液中
2Cl2 + 2OH- = 3Cl- + ClO-+ H2O
D.氨水中通入过量CO2
2NH3·H2O + CO2 = 2NH4+ + CO32- + H2O
12. 硝苯地平缓释片(简称NSRT)是一种用于治疗各种类型的高血压及心绞痛的新药,其结构式如右图所示。下列关于硝苯地平缓释片的说法正确的是
硝苯地平缓释片(简称NSRT)是一种用于治疗各种类型的高血压及心绞痛的新药,其结构式如右图所示。下列关于硝苯地平缓释片的说法正确的是
A.NSRT的分子式为C18H17N2O6
B.1molNSRT在水溶液中最多能消耗2molNaOH
C.NSRT不能使酸性高锰酸钾溶液褪色
D.1mol NSRT在一定条件下能和7molH2发生加成反应
11.向硝酸钠溶液中加入铜粉不发生反应,若再加入某种盐,则铜粉可以逐渐溶解,符合此条件的盐是
A. ZnSO4 B. NaHCO3
C. NaHSO4 D. Fe(NO3)3
10. 下列各过程的解释正确的是
A. 氧气与氢气的混合气体点燃时发生爆炸符合列夏特勒原理
B. 珠江啤酒打开瓶盖时产生大量气泡符合列夏特勒原理
C. 合成氨工业中使用适当的高温是为了提高氨的产率
D. 碳酸氢铵的分解若用熵增加原理来判断:这是一个自发过程
10. 已知:在100℃时,水的离子积为1×10-12,此时将pH=12的NaOH溶液V1 L与
pH=l的H2SO4溶液V2 L混合,若所得混合溶液的pH=10,则V1∶V2为
A.1 : 9 B.10: 1 C.9 : 1 D.1: 10
9.一定温度下,向a L密闭容器中加入2mol NO2(g),发生如下反应:
2NO2 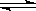 2NO + O2 ,此反应达到平衡状态的标志是
2NO + O2 ,此反应达到平衡状态的标志是
A. 混合气体的密度不再变化
B. 单位时间内生成 n mol O2同时生成2n mol NO2
C. 混合气体中NO2、NO、O2的物质的量之比为2︰2︰1
D. 混合气体的颜色变浅
8. 已知铅蓄电池放电时发生如下反应:
负极:Pb+SO42-=PbSO4+2e-
正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
实验室用铅蓄电池作电源,用惰性电极电解CuSO4溶液,当阴极析出2.4g铜时,铅蓄电池内消耗H2SO4物质的量至少是
A. 0.050mol B. 0.075mol C. 0.20mol D. 0.40mol
7. 用NA表示阿伏加德罗常数,下列说法正确的是
A.71g氯气与过量的FeCl2溶液完全反应转移的电子数为2NA
B.1 mol甲基(-14CH3)所含中子数为9 NA
C.在标准状况下,2.24L二氯甲烷所含的分子数为0.1NA
D.2L 0.1mol/L 的醋酸钠溶液中,所含离子总数是0.2NA
6. 现有等体积的Ba(OH)2、KOH和NH3·H2O三种溶液,将它们分别与V1 L、V2 L、
V3 L等浓度的盐酸混合,下列说法中正确的是
A.若混合前三种溶液pH相等,将它们同等倍数稀释后,则KOH溶液pH最大
B.若混合前三种溶液物质的量浓度相等,混合后溶液呈中性,则V1>V2>V3
C.若混合前三种溶液物质的量浓度相等,酸碱恰好完全中和反应,则V1>V2>V3
D.若混合前三种溶液pH相等,酸碱恰好完全中和反应,则V1>V2>V3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com