
题目列表(包括答案和解析)
18.(10分)配制一定物质的量浓度的溶液是实验室进行科学研究的重要环节。
(1)若配制大约1 mol·L-1叫的溶液100 mL,所给仪器只有托盘天平、量筒、带刻度的烧杯、玻璃棒,下列可选用的试剂是 (填字母序号)。
A.氢氧化钠固体B.浓硫酸(98%) C.浓盐酸(37%) D.浓硝酸(63%)
(2)下图是某学生在配制0.100 mol·L-1的碳酸钠溶液100 mL时,将第一次洗涤液转移到容量瓶内的操作。
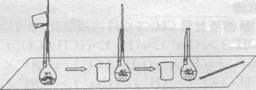
该步操作对所得溶液浓度的影响是 (填“偏高”、“偏低”或“无影响”),原因是
.
(3)若配制(2)中溶液时,该生使用托盘天平称取碳酸钠,则与计算量一致吗?为什么?
.
(4)现用移液管准确量取20.0 mI。0.100 mol·L-1盼碳酸钠溶液,注入锥形瓶中滴加甲基橙试剂2-3滴,此时溶液呈 色。然后将待测稀盐酸注入洁净、干燥的滴定管内,记下滴定管内稀盐酸的初始刻度读数,接着开始向锥形瓶内滴加盐酸。当锥形瓶内溶液颜色突变成 色时即达到滴定终点,此时消耗盐酸体积为21.36 mI。,则待测盐酸的浓度为 mol·L-1。
17(A).(12分)“物质结构与性质”课程模块
下表为长式周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中属于ds区的元素是 (填编号)。
(2)表中元素①的2个原子与元素③的2个原子形成的分子中元素③的杂化类型是 ;
③和⑦形成的常见化合物的化学键类型是 。
(3)元素⑧的外围电子排布式为 ,该元素原子中未成对电子数为 。
(4)在周期表中位于对角线的元素的性质也有一定的相似性。试写出元素②的氢氧化物与NaOH溶液反应的化学方程式: .
(5)在1183 K以下,元素⑨形成如图1所示基本结构单元的晶体;1183 K以上,转变 为图2所示基本结构单元的晶体。
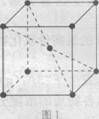

在1183 K以下的晶体中,与元素⑨的原子等距离且最近的原子数为 ;
在1183 K以上的晶体中,与元素⑨原子等距离且最近的原子数为 。
17(B).(12分)“实验化学’课程模块
已知亚甲基蓝其氧化型呈蓝色,还原型呈无色,其转化关系式为: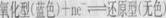
奇妙的“蓝瓶子”实验就是利用上述原理,其装置如图1。


某校化学兴趣小组用图1装置进行下述实验:
①在250 mL锥形瓶中,依次加入2g NaOH、100mlH2O和2g葡萄糖,搅拌溶解后,再加入3-5滴0.2%的亚甲基蓝溶液,振荡混合液呈蓝色;
②塞紧橡皮塞,关闭活塞a、b,静置,溶液变为无色;
③打开活塞、振荡,溶液又变为蓝色;
④关闭活塞、静置,溶液又变为无色;
⑤以上步骤③、④可重复多次。
请回答下列问题:
(1)若塞紧图1中锥形瓶塞,并打开导管活塞a、b,从导管口(填“左”或“右”)通入足量氦气后,再关闭活塞a、b并振荡,溶液 (填“能”或“不能”)由无色变为蓝色。
(2)如图2所示:某学生将起初配得的蓝色溶液分装在A、B两支试管中,A试管充满溶液,B中有少量溶液,塞上橡皮塞静置片刻,两溶液均显无色。若再同时振荡A、B试管,溶液显蓝色的是 试管。
(3)上述转化过程中葡萄糖的作用是 ,亚甲基蓝的作用是
(4)上述实验中葡萄糖也可用鲜橙汁(其中含丰富维生素C)代替,这是因为 。
(5)该实验中③、④操作 (填“能”或“不能”)无限次重复进行,理由是 。
16.(10分)图中字母所代表的物质均为中学化学常见物质。其中A是日常生活中不可缺少的物质,也是化工生产上的重要原料;常温下C、D、H为气体单质。单质E、M、N为金属,N是地壳中含量最大的金属元素。Y是红褐色沉淀。这些物质在一定条件下存在如下转化 关系,其中有些反应物或生成物已经略去。试回答下列问题:

(1)工业上,在电解A溶液的设备中将阴极区和阳极区用隔开,目的是 。
(2)Z→L反应的名称是 ,K的电子式为 。
(3)写出B→F的离子方程式 。
(4)写出K与C02反应的化学方程式 。
(5)Y与NaCl0和B混合溶液作用,是制备绿色水处理剂(Na2M04)的一种方法,请写出有关反应的离子方程式 。
15.(10分)现有五种短周期元素A、B、C、D、E,其原子序数依次增大。A、E同主族,A元素原子半径最小。B元素原子的最外层电子数是内层电子数的2倍。C元素最高价氧化物的水化物X与其氢化物Y反应生成一种盐。A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物。试回答下列问题:
(1)写出X与Y反应生成这种盐的化学方程式 。
(2)A、B、D、E四种元素组成的某无机盐受热易分解。写出少量该化合物与足量的 Ba(OH)2溶液反应的离子方程式 。
(3)将B的某种单质用作电极,电解E元素的最高价氧化物水化物的溶液时,阳极的电极反应式为 。
(4)在一密闭容器中注入A2、C2两种气体,发生了“ ”的化学反应。在某温度下达到平衡时,各物质的浓度分别是:c(A2)=9.00 mol·L-1,c(C2)
=3.00 mol·L-1,c(CA3) =4.00 mol·L-1。则此时该反应的平衡常数K=
;C2的初始浓度为mol·L-1;A2的转化率是
%。
”的化学反应。在某温度下达到平衡时,各物质的浓度分别是:c(A2)=9.00 mol·L-1,c(C2)
=3.00 mol·L-1,c(CA3) =4.00 mol·L-1。则此时该反应的平衡常数K=
;C2的初始浓度为mol·L-1;A2的转化率是
%。
14.在大试管内依次加入20 mL蒸馏水、10 mL无水酒精、7 g硫酸铵晶体,充分振荡后静置片刻,形成液体分层、部分固体沉淀的现象;再用激光笔测试,仅上层液体出现右图所示现象。依据上述描述,判断下列说法错误
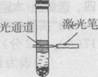 的是 ( )
的是 ( )
A.硫酸铵的溶解过程属于熵减小的过程
B.上层可能是硫酸铵在乙醇溶液中形成的胶体
C.该温度下,硫酸铵在水中的溶解度大于其在乙醇中的溶解度
D.再向该试管内滴入甲基橙试剂振荡后静置,上层液体显无色,下层液体出现红色
第Ⅱ卷(非选择题共72分)
13.已知 。下列关于不溶物之间转化的说法中正确的是 ( )
。下列关于不溶物之间转化的说法中正确的是 ( )
A.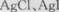 两者都不溶于水,因此AgCl与AgI不能相互转化
两者都不溶于水,因此AgCl与AgI不能相互转化
B.常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于

C.一定条件下AgCl可以转化为更难溶的AgI
D.只能由Ksp较大的不溶物转化为Ksp较小的不溶物
12.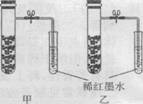 右图为模拟铁生锈的实验。铁粉中均匀混有少量碳粉,撒入在内壁已分别用氯化钠溶液和稀醋酸润湿过的甲、乙两支具支试管。打开止水 夹片刻后,以下有关该实验的说法合理的是 ( )
右图为模拟铁生锈的实验。铁粉中均匀混有少量碳粉,撒入在内壁已分别用氯化钠溶液和稀醋酸润湿过的甲、乙两支具支试管。打开止水 夹片刻后,以下有关该实验的说法合理的是 ( )
A.甲装置中红墨水倒吸量比乙装置多
B.甲装置中发生的电化学腐蚀主要是吸氧腐蚀
C.乙装置中发生的电化学腐蚀主要是析氢腐蚀
D.乙装置开始导管口有气泡冒出,接着红墨水又较快倒流
11.下述反应①、②分别是从海藻灰和智利硝石中提取碘的主要反应:
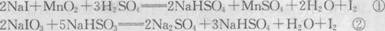
根据上述信息,手球断下列说法正确的是 ( )
A.两个反应中NaHS04均为氧化产物
B.在反应①中NaI是氧化剂,在反应②中NaI03中的碘元素被氧化
C.氧化性:Mn02>SO42一>IO3->I2
D.反应①、②中生成等量的I2时转移电子数之比为1:5
10.常温下,将稀NaOH溶液与稀CH。COOH溶液混合,不可能出现的结果是 ( )
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com