
题目列表(包括答案和解析)
17.(10分)各地电视台的天气预报中都要报城市的空气质量。根据国家环保局的统一规定,目前进行常规大气监测的项目是:氮氧化合物、二氧化硫、悬浮颗粒物等三种大气污染物。
(1)德国科学家曾经利用卫星数据和一种先进的仪器,绘制了一幅地球上空二氧化氮的分布图,从科学家绘制的二氧化氮分布图看,欧洲和北美洲的一些大城市上空二氧化氮密度很高,其原因是什么? 。
(2)与氮氧化合物有关的全球或区域性大气环境问题涉及到的有 。
A.酸雨 B.臭氧层空洞 C.光化学烟雾
(3)为了降低汽车尾气对大气的污染,目前最有效的方法是给汽车安装尾气净化装置。它能将一氧化碳和氮氧化物(NOx)通过催化剂发生反应转化为无害气体,其反应的化学方程式为 。
(4)用KIO3一淀粉溶液可定性检验空气中的SO2,写出反应的化学方程式。
。
(5)高锰酸钾法可定量测定空气中的SO2含量:反应器中有25.00mL 0.0200mol·L-1的酸性KMnO4溶液,往其中持续缓缓通入VL的空气,结束后,溶液仍呈淡红色,此时应用标准还原性溶液反滴定剩余的KMnO4溶液。下列溶液中可作为标准还原性溶液的是
(填选项字母)
A.FeSO4溶液 B.H2O2溶液 C.KNO3溶液 D.H2C2O4溶液
16.(12分)我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:NH3+CO2+H2O NH4HCO3 ; NH4HCO3+NaCl NaHCO3↓+NH4Cl ;
 2NaHCO3 Na2CO3+CO2↑+H2O
2NaHCO3 Na2CO3+CO2↑+H2O
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是 (填字母标号)。
a. 碳酸氢钠难溶于水
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验。
① 一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。
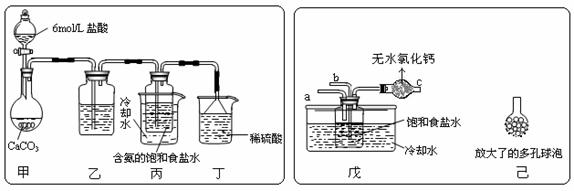
试回答下列有关问题:
 (Ⅰ)乙装置中的试剂是 ;
(Ⅰ)乙装置中的试剂是 ;
(Ⅱ)丁装置中稀硫酸的作用是 ;
(Ⅲ)实验结束后,分离出NaHCO3 晶体的操作是 (填分离操作的名称)。
② 另一位同学用图中戊装置(其它装置未画出)进行实验。
(Ⅰ)实验时,须先从 管通入 气体,再从 管中通入 气体;
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是 ;
(3)请你再写出一种实验室制取少量碳酸氢钠的方法: 。
15、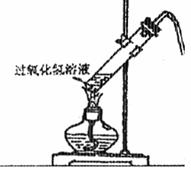 (6分)I、某小组用市售过氧化氢溶液配成15%左右过氧化氢溶液,采用下列装置(装置气密性良好)以过氧化氢代替氯酸钾制取氧气。进行实验。在有不少气泡产生数分钟后,用排空气法收集一试管气体,用带火星的木条检验。
(6分)I、某小组用市售过氧化氢溶液配成15%左右过氧化氢溶液,采用下列装置(装置气密性良好)以过氧化氢代替氯酸钾制取氧气。进行实验。在有不少气泡产生数分钟后,用排空气法收集一试管气体,用带火星的木条检验。
[实验问题]带火星的木条并不复燃。
[原因分析]
a.加热的时间还不够长,试管内氧气的蓄积量不够多(观察与猜想)。
b.产生气泡的速度太慢,应提高温度加快产生气泡的速度(观察与假设)。
c.过氧化氢溶液浓度过小。
[实验论证]
增大过氧化氢溶液的浓度,延长加热时间,在反应速率明显加快的情况下,用带火星木条检验,仍不复燃。
在经过重新讨论后,该小组同学将收集气体的方法改为排水法收集后,并用带火星木条检验,木条复燃。则原先带火星木条并不复燃的原因可能是:
a. 。
b. 。
II、已知下列化学反应:2H2O2 + 2KMnO4 + 3H2SO4 = K2SO4 + 5O2↑+ MnSO4 + 8H2O。某化学研究性学习小组在做此实验时发现:在敞口容器中, 当H2O2与酸化的KMnO4 溶液混合时,开始放出氧气的速率很慢,一段时间后产生氧气的速率很迅速,经过测定发现溶液中温度变化不大,学生百思不得其解,经向老师询问,老师说:影响化学反应速率的外界因素有浓度、温度、压强和催化剂,现随着反应的进行,反应物的浓度在逐渐降低,敞口容器的压强不受影响,反应的温度变化不大,则可能的因素是催化剂的影响。在老师的提示下学生又做了三个对比实验如下:
(1)空白实验
(2)起始时加入少量K2SO4固体
(3)起始时加入少量MnSO4固体
(4)起始时加入少量水
结果发现(1)、(2)起始反应速率差不多,(4)的起始反应速率比(1)、(2)慢,(3)的起始反应速率很快。请解释(1)实验中反应速率的变化现象的原因是: ________ __。
14.接触法制硫酸通常在400-500℃、常压和催化剂的作用下,用SO2与过量的O2反应生成SO3。 2SO2(g) + O2(g)  2SO3(g) ;△H < O。 在上述条件下,SO2的转化率约为90%。但是部分发达国家采用高压条件SO3,采取加压措施的目的是
2SO3(g) ;△H < O。 在上述条件下,SO2的转化率约为90%。但是部分发达国家采用高压条件SO3,采取加压措施的目的是
A.发达国家电能过量,以此消耗大量能源
B.高压将使平衡向正反应方向移动,有利于进一步提高SO2的转化率
C.加压可使SO2全部转化为SO3,消除SO2对空气的污染
D.高压有利于加快反应速率,可以提高生产效
第二卷(72分)
13.镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越来越成为人们研制绿色原电池的关注焦点。其中一种镁原电池的反应为:
 x Mg + Mo3S4
x Mg + Mo3S4  MgxMo3S4
MgxMo3S4
在镁原电池放电时,下列说法错误的是
A.Mo3S4发生氧化反应
B.正极反应为:Mo3S4 + 2xe- = Mo3S42x-
C.Mg2+向正极迁移
D.负极反应为:xMg - 2xe- = xMg2+
12、为确定某溶液的离子组成,进行如下实验:
①测定溶液的pH,溶液显强碱性。
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体。
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀。
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀。
根据实验以下推测正确的是
A. 一定有SO32-离子
B.一定有CO32-离子
C.不能确定C1-离子是否存在
D.不能确定HCO3-离子是否存在
11、某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等)
|
|
50mL盐酸 |
50mL盐酸 |
50mL盐酸 |
|
m(混合物) |
9.2 g |
15.7 g |
27.6 g |
|
V(CO2)(标况) |
2.24 L |
3.36 L |
3.36 L |
则下列分析推理中不正确的是
A.盐酸的物质的量浓度为3.0 mol/L
B.根据表中数据不能计算出混合物中NaHCO3的质量分数
C.加入混合物9.2 g时盐酸过量
D.15.7 g混合物恰好与盐酸完全反应
10、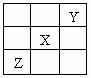 已知X、Y、Z三种主族元素在周期表中的相对位置如图所示,且X的原子序数为a,下列说法不正确的是
已知X、Y、Z三种主族元素在周期表中的相对位置如图所示,且X的原子序数为a,下列说法不正确的是
A.Y、Z的原子序数之和可能为2a
B.Y的原子序数可能是a-17
C.Z的原子序数可能是a+31
D.X、Y、Z一定都是短周期元素
9.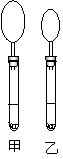 右图是10mLpH均为2的盐酸和醋酸分别与足量的碳酸钙反应一段时间后,所观察到的实验现象(反应过程中产生的气体收集在试管上部的气球中)。
右图是10mLpH均为2的盐酸和醋酸分别与足量的碳酸钙反应一段时间后,所观察到的实验现象(反应过程中产生的气体收集在试管上部的气球中)。
下列说法正确的是
A.甲试管中盛放的是盐酸溶液
B.甲试管中盛放的是醋酸溶液
C.图中所示的反应瞬间,甲试管中溶液的pH小于乙试管中溶液的pH
D.图中所示的反应瞬间,甲试管中溶液的pH大于乙试管中溶液的pH
8、2008年北京奥运会“祥云”火炬用的是环保型燃料--丙烷(C3H8),悉尼奥运会火炬所用燃料为65%丁烷(C4H10)和35%丙烷,已知丙烷的燃烧热为:2221.5 kJ/mol,下列有关说法正确的是
A.奥运火炬燃烧主要是将化学能转变为热能和光能
B.丙烷的沸点比正丁烷高
C.丙烷、空气及铂片可组成燃料电池,在丙烷附近的铂极为电池的正极
D.丙烷燃烧的热化学方程式为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(g);△H=-2221.5kJ/mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com