
题目列表(包括答案和解析)
16.(10分)氟化钠是一种重要的氟盐,主要用作农业杀菌剂、杀虫剂、木材防腐剂。实验室可通过下图所示的流程以氟硅酸(H2SiF6)等物质为原料制取氟化钠,并得到副产品氯化铵:

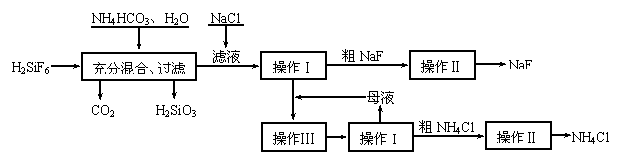
有关物质在水中溶解度分别为:
氯化铵:10℃时33.3 g、20℃时37.2 g、30℃时41.4g;氟化钠:20℃时4 g;氟硅酸钠微溶于水。
请回答下列问题:
⑴ 上述流程中发生两步化学反应,第一步反应的化学方程式为: ,第二步反应能进行是因为 。
⑵ 操作Ⅰ需要用到的玻璃仪器除玻璃棒外,还有 。
⑶ 操作II的作用是 。
⑷ 流程中NH4HCO3必须过量,其原因是 。
15.(9分)化学是一门以实验为基础的自然科学,化学实验在化学学习中具有极其重要的作用。(1)下列关于实验的叙述正确的有 (填序号)。
①在气体发生装置上直接点燃一氧化碳气体时,必需要先检验一氧化碳气体的纯度。最简单的方法是用排空气的方法先收集一试管气体,点燃气体,有爆鸣声即可。
②配制浓硫酸时,可先在烧杯中加一定体积的水,再边搅拌边加入浓硫酸
③实验结束后将所有的废液倒入下水道排出实验室, 以免污染实验室
(2) 粗盐经提纯后得到NaCl溶液,再经蒸发、结晶、烘干得精盐。
①蒸发操作中使用到的瓷质仪器的名称为____________________。
②该同学将所得精盐配成溶液。实验中需要用80mL,1mol/L的NaCl溶液,实际配制过程中用托盘天平称取的精盐质量为_________g,用于定容的玻璃仪器的规格和名称_______________。
(3)在进行研究性学习的过程中,某同学把AgNO3溶液滴入K2HPO4溶液,即得黄色沉淀。经过查阅资料得知:K2HPO4溶液呈碱性;Ag2HPO4和Ag3PO4均为黄色沉淀,只是Ag2HPO4的颜色略浅。该同学认为不能简单地根据颜色的深浅,来确定沉淀是何物。为此,他设计了一个分析实验的方案:先测K2HPO4溶液的pH值;在K2HPO4溶液中滴加硝酸银溶液的同时,不断测定溶液的pH值,直到沉淀量达到最大为止。实际实验中,随着AgNO3溶液的滴入,溶液的pH最终为3-4之间。
①请你判断沉淀量达到最大值时的黄色沉淀是__________________。(填“Ag3PO4”或“Ag2HPO4”)
②根据上述实验结果,请写出K2HPO4 与AgNO3的化学方程式: ;
③请你写出该实验的分析方案中是怎样得出实验结果的:
__________________________________________________________________________。
14.将a g CuO和Fe2O3的混合物分成两等份,向其中一份中加入b mL c mol/L的稀硫酸正好完全反应;另一份在加热的条件下用H2还原,反应完全时用去H2 d L(折算成标准状况)。则d等于
A.22.4bc×10-3 B.44.8bc×10-3
C.22.4(3a-4bc×10-3) D.22.4(3a-4bc)×10-3
第Ⅱ卷 非选择题(共70分)
13.如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是
 A.蓝色石蕊试纸先变红后褪色
A.蓝色石蕊试纸先变红后褪色
B.品红试纸、沾有KMnO4溶液滤纸均褪色都能证明SO2的漂白性
C.湿润淀粉KI试纸未变蓝说明SO2的氧化性弱于I2
D.NaOH溶液可用于除去实验中多余的SO2
12.Na2FeO4是一种高效多功能水处理剂,应用前景广阔。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应下列说法中不正确的是
A.Na2O2在反应中只作氧化剂
B.O2是氧化产物
C.Na2FeO4既是氧化产物又是还原产物
D.有2mol FeSO4参加发生反应时,反应中共有8mol电子转移
11.下列说法中,正确的是
A.NO2、BF3、NC13分子中没有一个分子中各原子的最外层电子都满足8电子稳定结构
B.P4和CH4都是正四面体分子,两种分子中化学键之间的夹角相等且均为109°28′
C.(NH4)2SO4晶体中只有离子键
D.由原子间通过共价键而形成的晶体具有高的熔点、沸点及硬度
10.钡在氧气中燃烧时得到一种钡的氧化物晶体, 结构如下图所示, 有关说法正确的是
 A.该晶体属于离子晶体
A.该晶体属于离子晶体
B.晶体的化学式为Ba2O2
C.该晶体晶胞结构与CsCl相似
D.与每个Ba2+距离相等且最近的Ba2+共有12个
9.下列各组中的X和Y两种原子,化学性质一定相似的是
A.X原子和Y原子最外层都只有一个电子
B.X原子的核外电子排布为1s2,Y原子的核外电子排布为1s22s2
C.X原子2p能级上有三个电子,Y原子的3p能级上有三个电子
D.X原子核外M层上仅有两个电子,Y原子核外N层上仅有两个电
8.在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62-+6M。关于该反应的说法中正确的组合是
① 氧化剂是H3AsO3; ② 还原性:Cl->As; ③ 每生成7.5gAs,还原剂失去的电子为0.3mol;④ M为OH-;⑤ SnCl62-是氧化产物。
A.①③⑤ B.①②④⑤ C.①②③④ D.只有①③
7.下列离子方程式正确的是
A.碳酸氢钠溶液与足量氢氧化钡溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O
B.亚硫酸氢铵和少量氢氧化钠溶液的反应:NH4++OH-=NH3↑+H2O
C.足量的溴化亚铁和少量的氯气反应:2Fe2++4Br-+3Cl2=3Fe3++2Br2+6Cl-
D.碳酸氢钙溶液中加入足量的氢氧化钠溶液:
2HCO3-+Ca2++2OH-=CO32-+CaCO3↓+2H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com