
题目列表(包括答案和解析)
14.已知:CH3CH2CH2CH3(g)+6.5O2(g) 4CO2(g)+5H2O(l);DH =-2878 kJ/moL
4CO2(g)+5H2O(l);DH =-2878 kJ/moL
(CH3)2CHCH3(g)+6.5O2(g) 4CO2(g)+5H2O(l);DH=-2869 kJ/moL
4CO2(g)+5H2O(l);DH=-2869 kJ/moL
下列说法正确的是
A.正丁烷分子储存的能量大于异丁烷分子
B.正丁烷的稳定性大于异丁烷
C.异丁烷转化为正丁烷的过程是一个放热过程
D.异丁烷分子中的碳氢键比正丁烷的多
13.某二价金属碳酸盐和碳酸氢盐的混合物跟足量盐酸反应,消耗H+和产生CO2的物质的量之比为6:5,该混合物中碳酸盐和碳酸氢盐的物质的量之比为
A.1:1 B.1:2 C.1:3 D.1:4
12.常温下,测得0.100mol/L。的某一元酸(HA)的pH不等于1,0.100mol/L的某一元碱(BOH)溶液中 将该两种溶液等体积混合,所得溶液中离子浓度关系正确的是
将该两种溶液等体积混合,所得溶液中离子浓度关系正确的是
A.C(A- )>C(B+)>C(H+)>C(OH- ) B.C(B+) > C(A- ) > C(OH- ) > C(H+)
C.C(B+)>C(A-)> C(H+) > C(OH- ) D.C(A- ) > C(B+)> C(H+)=C(OH- )
11.由一种阳离子与两种酸根离子组成的盐称为混盐。混盐CaOCl2在酸性条件下可以产生Cl2。下列关于混盐CaOCl2的有关判断正确的是
A.该混盐与硫酸反应产生1 molCl2时转移2NA个电子
B.该混盐的水溶液呈碱性
C.该盐也是一种复盐
D.该混盐中的氯元素的化合价为+1和-1
10.下列离子方程式正确的是
A.氢氧化钡溶液中加入过量小苏打 Ba2+ +2OH- +2HCO-3 = BaCO3↓+ CO32- +2H2O
 B.用碳棒作电极电解氯化钠饱和溶液2Cl- + 2H2O Cl2↑+
H2↑+2OH-
B.用碳棒作电极电解氯化钠饱和溶液2Cl- + 2H2O Cl2↑+
H2↑+2OH-
C.氯气通入水中 Cl2 + H2O = 2H+ + Cl- + ClO-
D.向漂白粉溶液中通人SO2气体:Ca2++2C1O-+SO2 =CaSO3↓+2H C1O
9.为了探索月球上是否有生命存在的痕迹,就要分析月球岩石中是否包藏有碳氢化合物(当然这仅仅是探索的第一步)。科学家用氘盐酸(DCl)和重水(D2O)溶液处理月球岩石样品,对收集的气体加以分析,结果只发现有一些气体状态的碳氘化合物。这个实验不能用普通盐酸,其理由是
A.普通盐酸的酸性太强
B.普通盐酸具有挥发性
C.普通盐酸和月球岩石中的碳化物无法反应
D.无法区别岩石中原来含有的是碳化物,还是碳氢化合物
8.有下列四组物质,如果把某组物质中的后者逐滴加入到前者中至过量,将出现“先产生白色沉淀,后白色沉淀溶解”的现象,这组物质是
A. 稀硫酸、氯化钡溶液 B. 硫酸亚铁溶液、氢氧化钠溶液
C. 氯化钠溶液、硝酸银溶液 D. 氯化铝溶液、氢氧化钠溶液
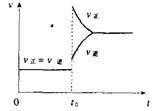
7.往一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g) 2HI(g);△H>O,当达到平衡后,t0时改变反应的某一条件(混合气体物质的量不变),且造成容器内压强增大,下列说法正确的是
2HI(g);△H>O,当达到平衡后,t0时改变反应的某一条件(混合气体物质的量不变),且造成容器内压强增大,下列说法正确的是
 A.容器内气体颜色变深,平均分子量不变
A.容器内气体颜色变深,平均分子量不变
B.平衡不移动,混合气体密度增大
C.H2转化率增大,HI平衡浓度变小
D.改变条件前后,速度图象为(如右图)
6.下列各组离子中,在溶液中能够大量共存的一组是
A.A1O2-、SO42-、Cl-、K+ B.Al3+、Ca2+、HCO3-、Na+
C.Fe3+、NH4+、SO42-、SCN- D. H+、C1-、Na+、H PO42-
5.设NA代表阿伏加德罗常数,下列说法中正确的是
①常温常压下,17g甲基(一CH3)所含的中子数为9NA
②常温常压下,22.4LNO气体的分子数小于NA
③64g铜发生氧化还原反应,一定失去2NA个电子
④常温常压下,100mL0.5mol/L的乙酸溶液中,乙酸的分子数目小于0.05NA
⑤标准状况下,22.4L二氯甲烷所含有的分子数为4NA
⑥常温常压下,lmol氦气含有的核外电子数为4NA
A.①② B.③④ C.②④ D.⑤⑥
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com