
题目列表(包括答案和解析)
19.(10分)大城市机动车带来的污染问题不容忽视。汽车排出尾气中含有CO、NOx和其他大气污染物,其成分与车速有关。下面是不同车速时排放的污染物质量(以平均行驶1km算);
|
车速(km/h) |
CO/g |
NOx/g |
碳氢化合物/g |
|
50 |
8.7 |
0.6 |
0.6 |
|
80 |
5.4 |
1.5 |
0.7 |
|
120 |
9.6 |
3.8 |
0.8 |
(1)随着汽车速度增加,污染气体排放量随之增加最多的是 。
(2)在汽车尾气系统中装置催化转化器,可使尾气中的CO和NOx在催化剂作用下相互发生氧化还原反应转化成两种无毒的气体,从而有效减少尾气中大气污染物。
该反应的化学方程式为 。
(3)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ·mol-1
若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移的电子总数
(4)随着我国家用汽车数量的迅猛增加,不但中速了城市空气污染,而且加剧了能源危机,导致石油和石油产品的价格不断攀升。往汽油中混入比例达到20%至35%的酒精,不仅可以节约汽油,而且可以减少70%以上的污染。已知酒精的燃烧热为1367kJ,请写出酒精燃烧的热化学方程式:
。
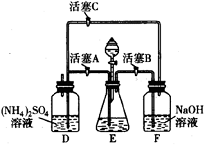
18.(10分)莫尔盐[(NH4)2SO4·FeSO4·6H2O]在
空气中比一般亚铁盐稳定,是化学分析中常用
的还原剂。某研究性学习小组用右图所示的实
验装置来制取莫尔盐,实验步骤如下:
①用30%的NaOH溶液和废铁屑混合、煮沸、
冷却、分离,将分离出的NaOH溶液装入F中;
②在E中用①处理过的铁屑和稀H2SO4反应制取FeSO4;
③将②制得的FeSO4溶液与(NH4)2SO4溶液混合,结晶得到莫尔盐。
试回答下列问题:
(1)利用铁屑和稀硫酸反应产生的氢气赶走装置中的氧气及硫酸铵溶液中溶解的氧,其目的是_________________________________;铁屑和稀硫酸反应产生的氢气的另外一个作用是_______________________________________________。
(2)如何设计一个简单的实验证明得到的产品中有Fe2+?
______________________________________________________________________
____________________________________________________________________。
(3)为了确定产品中亚铁离子的含量,研究小组用滴定法来测定。若取产品24.50g配成100mL溶液,取出10mL用0.10mol·L-1KMnO4酸性溶液滴定,消耗KMnO4溶液10.00mL。
①试配平反应的离子方程式:
______MnO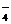 +_____Fe2++_____H+=_____Fe3++______Mn2++______H2O
+_____Fe2++_____H+=_____Fe3++______Mn2++______H2O
②试求产品中莫尔盐的质量分数_______________ (NH4)2SO4·FeSO4·6H2O的相对分子质量为392)。
17.(10分)工业上制备氯化铜时,是将浓盐酸用水蒸汽加热至80℃左右,慢慢加入粗制氧化铜粉(含杂质氧化亚铁),充分搅拌,使之溶解,反应如下:
CuO + 2HCl = CuCl2 + H2O ,FeO + 2HCl = FeCl2 + H2O。
已知:
|
物质 |
开始沉淀时的pH |
|
||
|
Fe(OH)3 |
1.9 |
3.2 |
||
|
Fe(OH)2 |
7.0 |
9.0 |
||
|
Cu(OH)2 |
4.7 |
6.7 |
(1)若提供的药品有:Cl2、浓H2SO4、NaOH溶液、CuO、Cu,试结合题给表格请参照,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤:
_____________________________________________________________________。
(2)将除去Fe2+后所得溶液小心加热浓缩,再冷却结晶,即可得CuCl2·xH2O。
①过滤操作中需要的玻璃仪器有________________________________________。
②经检测,CuCl2·xH2O中含水28.6%,则CuCl2·xH2O中x的值为 。
③如果要将CuCl2·xH2O处理为无水氯化铜,如何操作:
 。
。
16.下述实验能达到预期目的的是 ( )
|
编号 |
实验内容 |
实验目的 |
|
A |
将SO2通入酸性KMnO4溶液中 |
证明SO2具有漂白性 |
|
B |
将Cl2通入NaBr溶液中 |
比较氯与溴的氧化性强弱 |
|
C |
将铜与浓硝酸反应生成的气体收集后用冰水混合物冷却降温 |
研究温度对化学平衡的影响 |
|
D |
向某无色溶液中滴加酚酞试液 |
确定该溶液为碱溶液 |
|
15.已知酸性条件下有如下反应:2Cu+=Cu2++Cu。由于反应温度不同,用氢气还原氧化铜时,可能产生Cu或Cu2O,两者都是红色固体。一同学对某次用氢气还原氧化铜实验所得的红色固体产物作了验证,实验操作和实验现象记录如下 ( )
|
加入试剂 |
稀硫酸 |
浓硫酸、加热 |
稀硝酸 |
浓硝酸 |
|
实验现象 |
红色固体 和蓝色溶液 |
无色气体 |
无色气体 和蓝色溶液 |
红棕色气体 和绿色溶液 |
由此推出本次氢气还原氧化铜实验的产物是
A.Cu B.Cu2O
C.一定有Cu,可能有Cu2O D.一定有Cu2O,可能有Cu
14.在给定条件下,下列加点的物质在化学反应中能被完全消耗的是 ( )
A.用50 mL 8 mol·L-1浓盐酸与10 g二氧化锰共热制氧气
B.标准状况下,1 g铝片投入20 mL 18.4 mol·L-1的浓硫酸中
C.向100 mL 3 mol·L-1的硝酸中加入5.6 g铁
D.在5×107 Pa、500℃和铁触煤催化的条件下,用氮气和氢气合成氨
13.有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是 ( )
A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
D.若X的最高正价为+m,则Y的最高正价一定为+m
12.过氧化氢(H2O2)熟称双氧水,它是一种液体,易分解为水和氧气,常用作氧化剂、漂白剂和消毒剂。为了贮存、运输、使用的方便,工业上采用“醇析法”:将H2O2转化为固态的过碳酸钠晶体(其化学式为2Na2CO3·3H2O2),该晶体具有Na2CO3和H2O2的双重性质。下列物质不会使过碳酸钠失效的是 ( )
A.MnO2 B.Na2SO3溶液 C.稀盐酸 D.CH3COONa溶液
11.粗盐中含有可溶性杂质CaCl2、MgCl2和Na2SO4,若要得到纯净的NaCl固体,有如下实验操作:①加入过量Ba(OH)2溶液 ②加入过量NaOH溶液 ③加入过量BaCl2溶液 ④加入过量Na2CO3溶液 ⑤加入过量盐酸 ⑥过滤 ⑦蒸发结晶。正确的实验操作顺序是
( )
A.③②④⑥⑤⑦ B.③④②⑤⑦ C.②③④⑤⑥⑦ D.①④⑥⑤⑦
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com