
题目列表(包括答案和解析)
7.工业生产中物质的循环利用有多种模式。例如:

下列表述正确的是
A、图I可用于合成氨中的N2、H2的循环
B、图I可用于氨碱法制纯碱中CO2的循环
C、图Ⅱ可用于电解饱和食盐水中NaCl的循环
D、图Ⅲ可用于氨氧化法制硝酸中NO的循环
6.固体A的化学式为NH5,它的所有原子的最外层都符合相应的稀有气体原子的最外层电子结构。该物质适当加热就分解成两种气体。下列关于A的说法正确的是:
A.固体A属于分子晶体 B.A加热分解产生的两种气体是氨气和氢气
C.A与水发生的反应是氧化还原反应 D.A属于铵盐,溶于水后,水解呈酸性
5.三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有: HF、 NO 和 HNO3 。则下列说法错误的是:
A.反应过程中,被氧化与被还原的元素的物质的量之比为1:2
B.NF3是一种无色、无臭的气体,因此NF3在空气中泄漏时不易被察觉
C.一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染
D.若反应中生成1.0mol NO,转移的电子数目为6.02×1023
4.甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH+H2O(l)=CO2(g)+3H2(g);△H=+93.0kJ/mol
②CH3OH+1/2O2(g)=CO2(g)+2H2(g);△H=-192.9kJ/mol
下列说法正确的是
A、CH3OH的燃烧热为192.9 kJ/mol B、CH3OH的燃烧热为764.7 kJ/mol
C、CH3OH的燃烧热为392.7 kJ/mol D、不能算出其燃烧热
3.下列实验操作正确的是
A.粗盐提纯时,为了加快过滤速率,可用玻璃棒搅拌过滤器中的液体
B.容量瓶检漏:在容量瓶中注入适量的水,塞上玻璃瓶塞,左手五指托住瓶底,右手食指顶住瓶塞,反复倒置数次,观察是否漏水
C.不慎将浓苛性钠溶液沾到皮肤上,立即用H2SO4 中和并洗涤
D.测定溶液pH的操作:将pH试纸置于表面皿上,用玻璃棒蘸取溶液,点在pH试纸的中部,与对应的标准比色卡比较
2.下列实验中金属或氧化物可以完全溶解的是
A、1 mol铜片与含2 mol H2SO4的浓硫酸共热
B、1 mol MnO2粉末与含2 mol H2O2的溶液共热
C、常温下1 mol铝片投入足量的浓硫酸中
D、常温下1 mol铜片投人含4 mol HNO3的浓硝酸中
1.2007年据世界卫生组织统计,最常用避孕环是含金属铜的。金属铜的避孕机理之一是:铜与人体分泌物中的盐酸以及子宫内的空气反应:Cu+HCl+O2=CuCl+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是
A.氧化产物是HO2 B.HO2在碱中能稳定存在
C.氧化剂是O2 D.1 mol Cu参加反应有2 mol电子发生转移
23.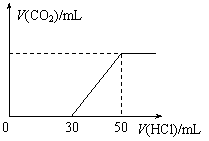 (10分) 标况下,在100 mL0.1mol·L-1某NaOH溶液中通入一定量CO2后,再向所得溶液中滴加某浓度的稀盐酸,滴加盐酸的体积与生成气体的情况如图所示。(假设生成的CO2全部逸出)。
(10分) 标况下,在100 mL0.1mol·L-1某NaOH溶液中通入一定量CO2后,再向所得溶液中滴加某浓度的稀盐酸,滴加盐酸的体积与生成气体的情况如图所示。(假设生成的CO2全部逸出)。
求:
(1)该稀盐酸物质的量浓度c(HCl)。
(2)滴加稀盐酸至50mL时共产生气体体积。
(3)滴加盐酸前溶液中所含溶质的成分及各自的物质的量浓度。
22.(8分)目前一种新型抗酸剂能迅速改善和缓解胃酸过多的症状,它主要由碳酸镁、氢氧化镁和氢氧化铝组成(说明:Mg(OH)2在高温下分解为MgO)。现按如下步骤测定药剂中三种主要成分的配比:
①取药剂样品,研磨后,加入50mL3.6 mol·L-1盐酸,正好完全反应并收集得到标准状况下224mL气体
②过滤,弃去其中不溶性物质(其余成分不参与反应)
③取②中滤液,加入足量的NaOH溶液后,过滤、洗涤、灼烧,所得固体2.4g。
试求该药剂中三种主要成分的物质的量之比。
21.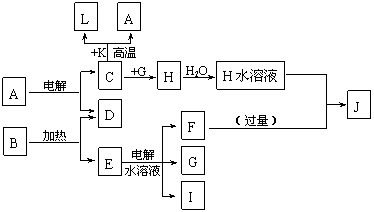 (10分) A-J分别代表中学化学中常见的一种单质或化合物,其转化关系如图。
(10分) A-J分别代表中学化学中常见的一种单质或化合物,其转化关系如图。
已知A在工业上常用作耐火材料,C、D、G、I为短周期元素形成的单质,D、G、I常温下为气态;形成D的元素的原子最外层电子数是次外层的3倍;B在焰色反应中呈紫色(透过蓝色钴玻璃),L是目前应用最广泛的金属。请回答下列问题:
(1)若K为红棕色粉末,写出C与K反应的化学方程式____________________________,引发该反应的操作为_____________________________________________________
__________________________________________________________。
(2)写出电解E水溶液的化学方程式__________________________________________。
(3)J与H反应的离子方程式为_________________________________。若在上述转化关系中每一步反应均为恰好反应,且不考虑C+K→A+L的变化时,为了最终得到J,则A、B的物质的量之比为_____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com