
题目列表(包括答案和解析)
28.(10分)
A. (1)今有化合物
(1)今有化合物
①请写出丙中含氧官能团的名称
②请判别上述哪些化合物互为同分异构体:
③请按酸性由强至弱排列甲、乙、丙的顺序:
(2)由丙烯经下列反应可制得F、G两种高分子化合物,它们都是常用的塑料。
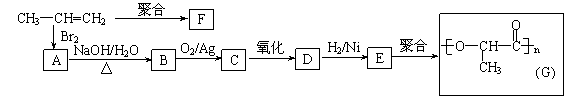
①聚合物F的结构简式是
②B转化为C的化学方程式是
保密★启用前 试卷类型:A
化 学
 选 择 题 答 题 区 选 择 题 答 题 区 ⒈用2B铅笔填涂: ⒉修改时用橡皮擦干净: ⒊填涂的正确方法  是: 是: |
以下为非选择题答题区,必须用黑色字迹的签字笔或钢笔在指定区域内用答,否则无效。
|
21.(10分) ①:____________ ___。② _______。 ③_____ ___。④_ ______。 ⑤________ ______。 22.(10分) (1) g。 (2) 、 (3) 。 (4) 。 (5) 。 23.(10分)(1) __________________________________________________。 (2) ________________________________________。 (3) ________________________. ______________________。 (4)_____________________ 。 四.(本题包括3小题,共30分) 24.(10分) (1) __________________________________________________。 (2) ①_______。②__ 。③_________________ (3) ①___________。②________ __ ③_______ __________ 25. (10分)(1)_____________________ ___. ___________ ___________ (2)________(3)_________________________。(4)_____________________; (5) __________ ____, (6)_________。 26.(10分)(1) 。________ (2) 。(3) (填序号) 。 (4) 五、(本题包括1小题,共10分) 27、(1)________________。 (2)_______________。 (3)___________ ______________ (4)_____________________ 六、28. (1)①____ ②_________ ③_____ (2) ①____ ②_________ |
27.(10分)(10分)聚氯乙烯(PVC)保鲜膜的安全问题引起广泛关注。PVC的安全隐患主要来自于塑料中残留的PVC单体以及不符合国家标准的增塑剂DEHA。工业上用乙烯和氯气为原料经下列各步合成PVC:


 乙烯
甲
乙
PVC
乙烯
甲
乙
PVC
(1)乙是PVC的单体,其结构简式为 ;
(2)反应③的化学方程式为
;
(3)写出以下反应类型:反应① ;反应② 。
(4)邻苯二甲酸辛酯(DOP)是国家标准中允许使用的增塑剂之一,邻苯二甲酸
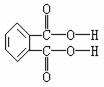
是制造DOP的原料,它跟过量的甲醇反应能得到另一种增塑剂DMP
(分子式为C10H10O4),DMP属于芳香酯,其结构简式
为 。
26.一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
根据题意完成下列各题:
(1) 反应达到平衡时,平衡常数表达式
K= ,升高温度,K值 (填“增大”、“减小”或“不变”)。
(2)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是
a 氢气的浓度减少 b 正反应速率加快,逆反应速率也加快
c 甲醇的物质的量增加 d 重新平衡时n(H2)/n(CH3OH)增大
(4)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是: (用化学方程式表示)
25.(10分)聚合氯化铝晶体的化学式为[Al2(OH)nCl6-n·xH2O]m,它是一种高效无机水处理剂,它的制备原理是调节增大AlCl3溶液的pH,通过促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣--铝灰,它主要含Al2O3、Al,还有SiO2等杂质。聚合氯化铝生产的工艺流程如下:

(1)搅拌加热操作过程中发生反应的离子方程式 ; 。
(2)生产过程中操作B和D的名称均为 (B和D为简单操作)。
(3)反应中副产品a是 (用化学式表示)。
(4)生产过程中可循环使用的物质是 (用化学式表示)。
(5)调节pH至4.0~4.5的目的是 。
(6)实验室要测定水处理剂产品中n和x的值。为使测定结果更准确,需得到的晶体较纯净。
生产过程中C物质可选用 。
A.NaOH B.Al C.氨水 D.Al2O3 E.NaAlO2

0.05 mol·L-1AgNO3溶液中的溶解度分别为S1、S2、S3、S4,则S1、S2、S3、S4由大到小的
顺序为 。
(2)下列曲线分别表示元素的某种性质与核电荷的关系(Z为核电荷数,Y为元素的有关性质)。把与下面元素有关的性质相符的曲线标号填入相应的空格中:
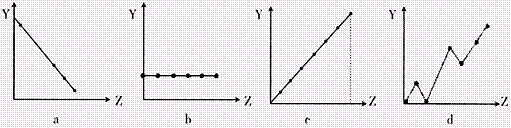
①ⅡA族元素的价电子数 ;
②第3周期元素的最高化合价 ;
③F-、Na+、Mg2+、Al3+的离子半径 。
(3)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3:4;M元素原子的最外层电子数与电子层数之比为4:3;N-、Z+、X+离子的半径逐渐减小;化合物XN常温下为气体。据此回答:
①N的最高价氧化物的水化物的化学式为 。
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1:1:1,A溶液中水的电离程度比B溶液中水的电离程度小。则化合物A中的化学键类型为 ,
B的化学式为 。
③工业上制取单质M的化学方程式为
24.(10分)(1)若AgC1在水中、0.01 mol·L-1 CaCl2溶液中、0.01 mol·L-1 NaCl溶液中及
23.(10分)氧化铜是一种黑色固体,可溶于稀硫酸。某同学想知道是稀硫酸的哪种粒子(H2O,H+,SO42-)能使氧化铜溶解。请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动。
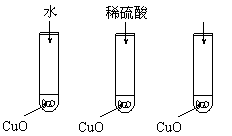 (1)某同学提出的假设是
(1)某同学提出的假设是
;
(2)通过实验Ⅰ可以证明
;
 (3)要证明另外两种粒子能否溶解氧化铜,还需要进行
(3)要证明另外两种粒子能否溶解氧化铜,还需要进行
实验Ⅱ和Ⅲ,在Ⅱ中加入稀硫酸后氧化铜溶解,则
进一步所做的确认为:在Ⅲ中先加入 ,再加入 。
(4)探究结果为 。
你认为除实验Ⅱ和Ⅲ所用的试剂外,还能溶解氧化铜的一种常见物质是 。
22.(10分)(10分) 以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:

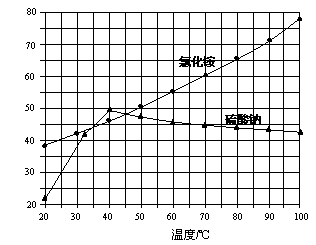
氯化铵和硫酸钠的溶解度随温度变化如上图所示。回答下列问题:
(1)欲制备10.7gNH4Cl,理论上需 NaCl g。
(2)实验室进行蒸发浓缩用到的主要仪器有 、烧杯、玻璃棒、酒精灯等。
(3)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为 。
(4)不用其它试剂,检查NH4Cl产品是否纯净的方法及操作是 。
(5)若NH4Cl产品中含有硫酸钠杂质,进一步提纯产品的方法是 。

21. (10分)⑴指出在使用下列仪器(已经洗涤完毕)或用品时的第一步操作:
①蓝色石蕊试纸(检验某无色气体):____________ ___。
②250mL容量瓶:_______ _ _______。
③25mL酸式滴定管:______________ ___。
④集气瓶(收集氨气):_____________ ______。
⑤托盘天平:_____________ ______。
20.化学实验设计和操作中必须十分重视安全问题和环境保护问题。下列实验问题处理方法不正确的是
A.实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室
B. 在气体发生装置上直接点燃一氧化碳气体时,必需要先检验一氧化碳气体的纯度,最简单的方法是用排空气的方法先收集一试管气体,点燃气体,听爆鸣声
C.制氧气时排水法收集氧气后出现倒吸现象,立即松开试管上的橡皮塞
D. 给试管中的液体加热时不时移动试管或加入碎瓷片,以免暴沸伤人
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com