
题目列表(包括答案和解析)
19.(8分)已知单质铁溶于-定浓度的硝酸溶液中反应的离子方程式为:
aFe+bNO3-+cH+=dFe2++fFe3++gNO↑+hN2O↑+kH2O(化学计量数a-k均为正整数)。
回答下列问题:
(1)根据反应中氮、氢、氧三种元素的原子个数守恒,可得c、g、h的关系式是(用-个代数式表示。下同) 。
(2)根据反应中离子的电荷守恒,可得b、c、d、f的关系式是 。
(3)根据反应中电子转移的总数相等,可得d、f、g、h的关系式是 。
(4)若a=12,且铁和稀硝酸恰好完全反应,则b的取值范围是 ;c的取值范围是 。
18.(12分)我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:NH3+CO2+H2O NH4HCO3 ; NH4HCO3+NaCl NaHCO3↓+NH4Cl ;
 2NaHCO3 Na2CO3+CO2↑+H2O
2NaHCO3 Na2CO3+CO2↑+H2O
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是 (填字母标号)。
a.碳酸氢钠难溶于水 b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验。
① 一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。
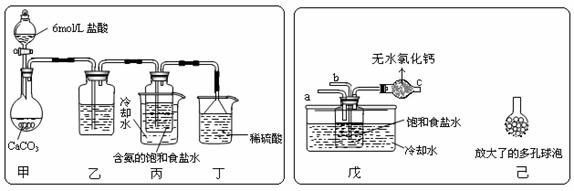
试回答下列有关问题:
 (Ⅰ)乙装置中的试剂是
;
(Ⅰ)乙装置中的试剂是
;
(Ⅱ)丁装置中稀硫酸的作用是 ;
(Ⅲ)实验结束后,分离出NaHCO3 晶体的操作是 (填分离操作的名称)。
② 另一位同学用图中戊装置(其它装置未画出)进行实验。
(Ⅰ)实验时,须先从 管通入 气体,再从 管中通入 气体;
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是 ;
(3)请你再写出一种实验室制取少量碳酸氢钠的方法: 。
17.(9分)化学是一门以实验为基础的自然科学,化学实验在化学学习中具有极其重要的作用。(1)下列关于实验的叙述正确的有 (填序号)。
①在气体发生装置上直接点燃一氧化碳气体时,必需要先检验一氧化碳气体的纯度。最简单的方法是用排空气的方法先收集一试管气体,点燃气体,听爆鸣声。
②配制稀硫酸时,可先在烧杯中加一定体积的水,再边搅拌边加入浓硫酸
③实验结束后将所有的废液倒入下水道排出实验室, 以免污染实验室
(2)下列实验没有错误的是 (填字母代号)。
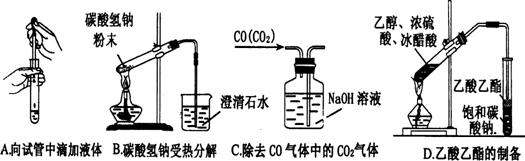
(3)下图为常见仪器的部分结构(有的仪器被放大)
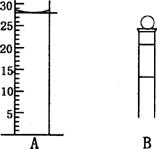
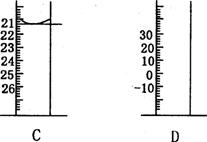
A图中液面所示溶液的体积为 mL,用上述四种仪器中的某种测量一液体的体积,平视时读数为NmL,仰视时读数为MmL,若M>N,则所使用的仪器是 (填字母标号)。
(4) 粗盐经提纯后得到NaCl溶液,再经蒸发、结晶、烘干得精盐。
①蒸发操作中使用到的瓷质仪器的名称为____________________。
②该同学将所得精盐配成溶液,用于另一实验。实验中需要用80mL,1mol/L的NaCl溶液,配制过程中用托盘天平称取的精盐质量为_________g,用于定容的玻璃仪器的规格和名称____________________________ ___。
16.镁铁混合物4.9g,溶解在过量某浓度的稀硝酸中,完全反应得到标况下气体2.24L(假设气体全为NO),则向反应后的溶液中加入足量的烧碱,则可生成沉淀的量是
A.10g B.8g C.6g D.12g
第二卷(非选择题 共72分)
15.世界上60%的镁是从海水中提取的,其主要步骤如下:
①把贝壳制成石灰乳;②在海水中加入石灰乳,过滤,洗涤沉淀物;③将沉淀物与盐酸反应,结晶、过滤;④在氯化氢热气流中干燥晶体;⑤电解上述晶体的熔融物。
下列说法正确的是
A.镁元素在元素周期表中位于第三周期、ⅡA族
B.向洗涤液中滴加碳酸钠溶液可检验沉淀是否洗涤干净
C.在氯化氢热气流中干燥晶体的目的是加快干燥速度
D.步骤⑤也可以采用电解该晶体水溶液的方法
14.某学生在实验室做了5个实验:
(1)在铝盐溶液中逐滴加入稀氨水直至过量,(2)在明矾溶液中加入NaOH溶液直至过量,(3)在强碱性溶液中逐滴加入铝盐溶液直至过量,(4)在偏铝酸钠溶液中通入CO2直至过量,(5)在强酸溶液中逐滴加入偏铝酸钠溶液直至过量。
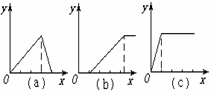
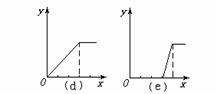
并根据以上实验画出下列5种图象(纵坐标为沉淀物质的量,横坐标为溶液中加入物质的量)实验与图象对立关系正确的是:___________。
A.(1)和(a) B.(2)和(b) C.(3)和(e) D.(4)和(c)
13.如图是a、b两种固体物质的溶解度曲线,下列说法中错误的 是
A.a中含有少量b时可以用结晶法提纯a
B.20℃时a和b饱和溶液的物质的量浓度是a<b
C.30℃时a和b饱和溶液的质量分数是a>b
D.x点表示的a和b溶液都是饱和溶液
12.下列有关化学事实或现象的解释正确的是
A.合金在潮湿的空气中形成原电池,故其耐腐蚀性都较差
B.升高温度反应速率加快,原因是活化分子百分数增加
C.氯化钠溶于水也有化学过程,是因为离子键发生了断裂
 D.铝的金属活动性较强,所以铝制容器在空气中容易被腐蚀
D.铝的金属活动性较强,所以铝制容器在空气中容易被腐蚀
11.下列离子方程式书写正确的是
A.NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3- +Ba2++2OH- = BaCO3↓+2H2O+CO32 -
B.向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全:
Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3·H2O+ H2O
C.硫酸亚铁溶液与稀硫酸、双氧水混合:2Fe2++H2O2 +2H+=2Fe3++2H2O
D.向次氯酸钠溶液中通入足量SO2气体:ClO-+ SO2+ H2O = HClO+ HSO3-
10.下列各组离子可能大量共存的是
A.pH=1的溶液中:Fe2+、Al3+、HCO3-、MnO4-
B.能与金属铝反应放出氢气的溶液:K+、NO3-、Cl-、NH4+
C.含有大量OH-的无色溶液中:Na+、Cu2+、AlO2-、SiO32-
D.常温下水电离出的c(H+)·c(OH-)=10-20的溶液中:Na+、C1-、S2-、SO32-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com