
题目列表(包括答案和解析)
4.通过复习总结,你认为下列对化学知识的概括合理的是
A.氧化物不可能是还原产物,只可能是氧化产物
B.一种元素可能有多种氧化物,但相同化合价只对应一种氧化物
C.原子晶体熔点不一定比金属晶体高,分子晶体熔点不一定比金属晶体低
D.原子晶体、离子晶体、金属晶体、分子晶体的粒子之间都一定存在化学键
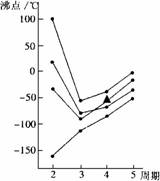
3.右图中每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化(外压为1atm),其中▲代表的是
A.AsH3 B.HBr C.H2Se D.GeH4
2. 不能用勒沙特列原理解释的是
不能用勒沙特列原理解释的是
A.经粉碎的黄铁矿在沸腾炉中燃烧得较快、较完全
B.饱和FeCl3溶液中加入盐酸,丁达尔效应减弱
C.NaOH溶液使酯水解比稀H2SO4使酯水解效果好
D.氨水的保存需要密封、低温保存
1.设NA表示阿佛加德罗常数的值,下列关于NA的下列说法中正确的是
A.铁粉与一定量浓硫酸反应,产生11.2LSO2和1gH2,铁粉失去的电子数为2NA
B.124g白磷中含有P-P键的数目为4NA
C.含2NA个化学键的CnH2n+2分子的物质的量为2/(3n+1)mol
D.7.8gNa2S溶于水中,S2-的数目为0.1NA
23.(6分)自然界存在的某天然碱(纯净物)的组成表示为aNa2CO3·bNaHCO3·cH2O
(a、b、c为正整数)。现称取不同质量的天然碱样品,溶于水后,分别逐滴加入相同浓度的盐酸30.0 mL,产生二氧化碳的体积(标准状况)如图所示。
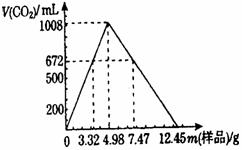
(1)若用2.49 g样品进行同样的实验时,产生二氧化碳 mL
(标准状况)。
(2)另取3.32 g天然碱样品于300℃加热分解至完全(300℃时碳酸钠不分解),产生
112 mL二氧化碳(标准状况)和0.450 g水,试通过计算确定该天然碱的化学式为 。
(3)实验所用盐酸的物质的量浓度为 。
21. (10分) A、B、C、D、E都是短周期元素,原子序数依次增大,A、B属于同一周期,C、D、E同处另一周期。C、B可按原子个数比2:1和1:1分别形成两种离子化合物甲和乙。D、A按原子个数比3:2形成离子化合物丙。E是地壳中含量最高的金属元素。A、B均是有机化合物丁的组成元素,而且在同类化合物中丁的组成最简单。根据以上信息回答下列问题:
(1)B元素在周期表中的位置是 ,
D元素的原子结构示意图是 。
(2)A、B、C、D、E五种元素的原子半径由小到大的顺序是
(用元素符号填写)。
(3)丁能与乙醇发生酯化反应,其化学方程式为
(4)乙投入到水中发生反应的离子方程式是 22.(13分)A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件未标出),其中反应①是置换反应。

[Ⅰ]若在常温下A是常见的金属单质,D、F是气态单质,反应①需在水溶液中进行,则:
(1)试推测A D (填化学式)
(2)写出反应①的化学方程式 。
(3)E的水溶液显酸性,其原因是(用离子方程式来表示)
(4)已知1g D与F反应生成B时放出了92.3 kJ的热量,写出该反应的热化学方程
式 。
(5)在现实生活中A物质主要发生 腐蚀,其反应的正极反应式为 。
[Ⅱ]若在常温下A是非金属单质,D、F是气态的单质,反应①需在高温条件下进行,则:
试推测A E (填化学式)
20.(14分)某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题。

(1)若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制Cl2 ,制得的Cl2体积(标准状况下)总是小于1.12 L的原因是
。
(2)①装置B中盛放的试剂名称为 ,作用是 ,
现象是 。
②装置C和D中出现的不同现象说明的问题是 。
③装置E的作用是 。
④写出装置F中发生反应的离子方程式 。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在 与 之间(填装置字母序号),装置中应放入 (填写试剂或用品名称)。
19.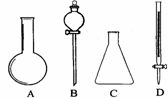 (9分)(1)右下图所示A、B、C、D四种仪器: 请选择下列仪器名称的序号,填人相应的空格内:①烧杯 ②普通漏斗 ③圆底烧瓶 ④锥形瓶 ⑤分液漏斗 ⑥酸式滴定管
(9分)(1)右下图所示A、B、C、D四种仪器: 请选择下列仪器名称的序号,填人相应的空格内:①烧杯 ②普通漏斗 ③圆底烧瓶 ④锥形瓶 ⑤分液漏斗 ⑥酸式滴定管
A______________ B______________ C______________ D______________
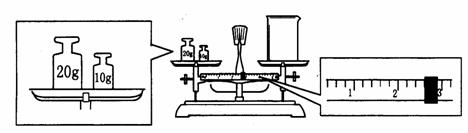 (2)某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图.由图中可以看出,该同学在操作时的一个错误是______________,烧杯的实际质量为______________g
(2)某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图.由图中可以看出,该同学在操作时的一个错误是______________,烧杯的实际质量为______________g
 (3)指出下面3个实验中各存在的一个错误:
(3)指出下面3个实验中各存在的一个错误:
A_________________________
B__________________________
C___________________________
18. 向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入400 mL 0.5 mol·L-1 HCl,恰好使混合物溶解,并放出气体224 mL (标准状况下),所得溶液中加入KSCN溶液无血红色出现,若用足量的CO在高温下还原质量相同的此混合物,得到铁的质量为
A.11.2g B.22.4g C.5.6g D.无法计算
安丘市高三9月份教学质量检测
化学试题
第Ⅱ卷(非选择题 共52分)
17. 如右图所示,集气瓶内充满下列某混合气体,置
如右图所示,集气瓶内充满下列某混合气体,置
于光亮处,若将胶头滴管内的水挤入集气瓶,一段时间后
烧杯中的水就会进入集气瓶,则集气瓶中的气体不可能
是
[① CO、O2 ② Cl2、CH4 ③ NO2、O2 ④N2、H2]
A.①② B.②④ C.①④ D.②③
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com