
题目列表(包括答案和解析)
14.利尿剂是2008北京奥运会违禁药物,顾名思义,此类药物有稀释尿液的功能。利尿剂现有15种,主要用于掩盖或“清洗”体内其它违禁药品的存在,以逃避兴奋剂检查。下图所示有机物是其中之一的结构简式:
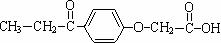
下列叙述正确的是
A.1mol利尿酸最多可与5mol H2发生加成反应
B.利尿酸分子式是C11H12O4
C.利尿酸分子中位于同一平面内的原子有10个
D.利尿酸与新制Cu(OH)2悬浊液反应有红色沉淀生成
13.X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期, W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价代数和为6。下列说法正确的是
A.Y元素最高价氧化物对应的水化物化学式H2YO4
B.X与W可以形成W2X、W2X2两种化合物
C.原子半径由小到大的顺序为:W<X<Z<Y
D.Y、Z两种元素气态氢化物中,Z的气态氢化物最稳定
12.某溶液中加入铝粉产生的气体只有氢气,该溶液中肯定可以大量存在的离子组是
A.Na+、NO3-、Cl-、SO42- B.Na+、K+、Ba2+、HCO3-
C.Na+、K+、Cl-、SO42- D.Fe3+、H+、SO42-、Cl-
11.有关键能数据如表:
晶体硅在氧气中燃烧的热化学方程式为Si(s)+O2(g)=SiO2(s); = -989.2/kJ·mol-1,则X的值为
= -989.2/kJ·mol-1,则X的值为
A.423.3 B.460 C.1165.2 D.920
10.将下列每组内的四种物质同时加入到水中,充分搅拌后,既有氧化还原反应发生,又有沉淀产生的一组是(酸均过量)
A.Na2O2、NH4Cl、NaCl、Na2SO4 B.FeO、AlCl3、Na2SiO3、硝酸
C.KHCO3、Ca(OH)2、MgCl2 、硫酸 D.Na2CO3、BaCl2、K2S、盐酸
|
化学键 |
Si-O |
O=O |
Si-Si |
|
键能/kJ·mol-1 |
X |
498.8 |
176 |
9.一定量的铜与一定量的浓硝酸恰好完全反应,产生NO、NO2两种气体(不考虑2NO2 N2O4),已知反应中被还原的HNO3占HNO3总量的1/3,则还原产物中NO、NO2的物质的量之比为
N2O4),已知反应中被还原的HNO3占HNO3总量的1/3,则还原产物中NO、NO2的物质的量之比为
A.2∶1 B.1∶2 C.2∶3 D.1∶1
8.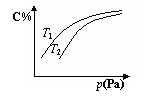 在密闭容器中,对于可逆反应A+3B
在密闭容器中,对于可逆反应A+3B 2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
A.若正反应方向△H <0,则T1> T 2
B.压强增大时,混合气体的平均相对分子质量减小
C.B一定为气体
D.A一定为气体
7.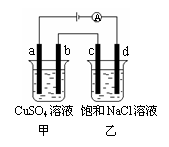 如图所示,a、b、c、d均为石墨电极,通电进行电解。下列说法正确的是
如图所示,a、b、c、d均为石墨电极,通电进行电解。下列说法正确的是
A.乙烧杯中d的电极反应为 2Cl––2e– =Cl2↑
B.a、c两极产生气体的物质的量相等
|
2NaCl + 2H2O  2NaOH + H2↑+ Cl2↑
2NaOH + H2↑+ Cl2↑
D.甲、乙两烧杯中溶液的pH均保持不变
6.K35ClO3晶体与H37Cl的溶液反应后,生成氯气、氯化钾和水。下列说法正确的是
A.生成氯气的相对分子质量为72
B.被还原的K35ClO3和被氧化的H37Cl的物质的量之比为1:6
C.氯化钾既不是氧化产物,也不是还原产物
D.每生成标准状况下的氯气11.2L,转移的电子数约为6.02×1023
5.下列关于接触法制硫酸的叙述中正确的是 A.为防止污染大气,从吸收塔出来的尾气常用NaOH溶液吸收
B.由于高压的条件有利于SO2转化为SO3,所以SO2接触氧化采用高压的反应条件
C.为提高SO3的吸收效率,吸收操作采取逆流形式,SO3从吸收塔的下部通入
D.在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com