
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
23.(1)ЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎ(2)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ (3)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
28Ј® (14·Ц)ЎЎ aЎўbЎўcЎўdЎўeКЗ¶МЦЬЖЪФӘЛШЈ¬ЦЬЖЪұнЦРaУлbЎўbУлcПаБЪЈ»aУлeөДЧоНвІгөзЧУКэЦ®ұИОӘ2:3Ј¬bөДЧоНвІгөзЧУКэұИeөДЧоНвІгөзЧУКэЙЩ1ёцЈ»іЈјы»ҜәПОпd2c2УлЛ®·ҙУҰЙъіЙcөДөҘЦКЈ¬ЗТИЬТәК№·УМӘКФТәұдәмЎЈ
(1) eөДФӘЛШ·ыәЕКЗ__________ЎЈ
(2)aЎўbЎўcөДЗв»ҜОпОИ¶ЁРФЛіРтОӘ(УГ·ЦЧУКҪұнКҫ)______________________Ј»bөДЗв»ҜОпәНbөДЧоёЯјЫСх»ҜОпөДЛ®»ҜОп·ҙУҰЙъіЙZЈ¬ФтZЦРөД»ҜС§јьАаРНОӘ_________________Ј¬ZөДҫ§МеАаРНОӘ_____________Ј»abЈӯАлЧУөДөзЧУКҪОӘ____________ЎЈ
(3)УЙaЎўcЎўdРОіЙ»ҜәПОпөДЛ®ИЬТәПФјоРФЈ¬ЖдФӯТтКЗ(УГАлЧУ·ҪіМКҪұнКҫ)______________________________________________ЎЈ
(4)Т»¶ЁБҝөДd2c2Улac2·ҙУҰәуөД№ММеОпЦКЈ¬ЗЎәГУл0.8 molПЎСОЛбИЬТәНкИ«·ҙУҰЈ¬ІўКХјҜөҪ0.25 molЖшМеЈ¬ФтУГОпЦКөДБҝұнКҫёГ№ММеОпЦКөДЧйіЙОӘ__________________Ўў___________________ЎЈ
РХГыЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЧщәЕЎЎЎЎЎЎЎЎ °аұрЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎ
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
ЎЎ |
21ЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
22(1) ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ(2)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
(3)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
(4) ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
(5) ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
27Ўў(14·Ц)ПЦУРІҝ·Ц¶МЦЬЖЪФӘЛШөДРФЦК»тФӯЧУҪб№№ИзПВұнЈә
|
ФӘЛШұаәЕ |
ФӘЛШРФЦК»тФӯЧУҪб№№ |
|
T |
MІгЙПУР2¶ФіЙ¶ФөзЧУ |
|
X |
ЧоНвІгөзЧУКэКЗҙОНвІгөзЧУКэөД2ұ¶ |
|
Y |
іЈОВПВөҘЦКОӘЛ«ФӯЧУ·ЦЧУЈ¬ЖдЗв»ҜОпЛ®ИЬТәіКјоРФ |
|
Z |
ФӘЛШЧоёЯХэјЫКЗ+7јЫ |
(1)ФӘЛШTөДФӯЧУЧоНвІг№ІУРЎЎЎЎЎЎ ЦЦІ»Н¬ФЛ¶ҜЧҙМ¬өДөзЧУЎЈФӘЛШXөДТ»ЦЦН¬О»ЛШҝЙІв¶ЁОДОпДкҙъЈ¬ХвЦЦН¬О»ЛШөД·ыәЕКЗЎЎЎЎЎЎ ЎЈ
(2)ФӘЛШYУлЗвФӘЛШРОіЙТ»ЦЦАлЧУYH4+ Ј¬РҙіцёГОўБЈөДөзЧУКҪЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ (УГФӘЛШ·ыәЕұнКҫ)
(3)ФӘЛШZУлФӘЛШTПаұИЈ¬·ЗҪрКфРФҪПЗҝөДКЗЎЎЎЎЎЎ (УГФӘЛШ·ыәЕұнКҫ)Ј¬ПВБРұнКцЦРДЬЦӨГчХвТ»КВКөөДКЗ___________ЎЈ
aЈ®іЈОВПВZөДөҘЦКәНTөДөҘЦКЧҙМ¬І»Н¬ЎЎЎЎ bЈ®ZөДЗв»ҜОпұИTөДЗв»ҜОпОИ¶Ё
cЈ®Т»¶ЁМхјюПВZәНTөДөҘЦК¶јДЬУлЗвСх»ҜДЖИЬТә·ҙУҰ
(4)МҪС°ОпЦКөДРФЦКІоТмРФКЗС§П°өДЦШТӘ·Ҫ·ЁЦ®Т»ЎЈTЎўXЎўYЎўZЛДЦЦФӘЛШөДЧоёЯјЫСх»ҜОпөДЛ®»ҜОпЦР»ҜС§РФЦКГчПФІ»Н¬УЪЖдЛыИэЦЦЛбөДКЗЎЎЎЎЎЎЎЎЎЎЎЎ Ј¬АнУЙКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЈ
26. (9·Ц)ўЩФЪ6·Э0Ј®01 moLЈҜL°ұЛ®ЦР·ЦұрјУИлПВБРёчОпЦКЈәAЈ®ЕЁ°ұЛ®Ј¬BЈ®ҙҝЛ®Ј¬CЈ®ЙЩБҝK2SO3№ММеЈ¬DЈ®ЙЩБҝЕЁБтЛбЈ¬EЈ®ЙЩБҝNaOH№ММеЈ¬FЈ®ЙЩБҝAl2(SO4)3Ј¬№ММеЎЈ
(a)ДЬК№C(OH-)јхРЎЈ¬К№C(NH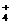 )ФцҙуөДКЗ____________Ј»(b)ДЬК№C(OH-)ФцҙуЈ¬К№C(NH
)ФцҙуөДКЗ____________Ј»(b)ДЬК№C(OH-)ФцҙуЈ¬К№C(NH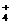 )јхРЎөДКЗ________Ј»(c)ДЬК№C(0H-)әНC(NH
)јхРЎөДКЗ________Ј»(c)ДЬК№C(0H-)әНC(NH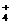 )¶јФцҙуөДКЗ_________Ј»(d)ДЬК№C(OH-)әНC(NH
)¶јФцҙуөДКЗ_________Ј»(d)ДЬК№C(OH-)әНC(NH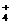 )¶јјхРЎөДКЗ______________ЎЈ(ҫщРҙұаәЕ)
)¶јјхРЎөДКЗ______________ЎЈ(ҫщРҙұаәЕ)
ўЪ25ЎжКұУГPtөзј«өзҪв500mL amolЈҜL CuSO4ИЬТәЈ¬
КФ»ШҙрПВБРУР№ШОКМвЈәЎЎЎЎ
ЎЎЎЎЎЎ (a)РҙіцБҪј«өДөзј«·ҙУҰКҪЈәСфј«____________Ј¬Тхј«__________ЎЈ
(b)өұөзҪвөҪC(Cu2+)ОӘ0.5a mol/LКұЈ¬НЈЦ№өзҪвЈ¬ИфТӘК№ИЬТә»ЦёҙөҪУлөзҪвЗ°ПаН¬өДЧҙМ¬Ј¬ҝЙПтИЬТәЦРјУИлККБҝөД(ЎЎЎЎ )
(A)CuSO4·ЫД©ЎЎ (B)CuSO4ЎӨ5H2OЎЎ (C)CuO·ЫД©ЎЎ (D)Cu(OH)2
25.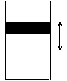 ФЪИзНјЛщКҫөДИэёцИЭ»эПаН¬өДИЭЖчўЩЎўўЪЎўўЫЦРҪшРРИзПВөД·ҙУҰЈә
ФЪИзНјЛщКҫөДИэёцИЭ»эПаН¬өДИЭЖчўЩЎўўЪЎўўЫЦРҪшРРИзПВөД·ҙУҰЈә
ЎЎ
ЎЎ
 3A(g)+B(g)
3A(g)+B(g) 2C(g) ЎчHЈј0.
2C(g) ЎчHЈј0.
(1)ИфЖрКјОВ¶ИПаН¬Ј¬·ЦұрПтИэёцИЭЖчЦР
ідИл3molAәН1molBЈ¬ФтҙпөҪЖҪәвКұЎЎЎЎЎЎ ўЩНвУРёфИИМЧЎЎЎЎЎЎ ўЪЎЎЎЎЎЎ ўЫ»оИыҝЙТЖ¶Ҝ
ёчИЭЖчЦРCОпЦКөД°Щ·Цә¬БҝУЙҙу өҪРЎөДЛіРтОӘ_____________(МоИЭЖчұаәЕ)(І»ҝјВЗ
»оИыЦКБҝәНДҰІБПөКэ)ЎЎЎЎЎЎЎЎЎЎЎЎ
(2)ИфО¬іЦОВ¶ИІ»ұдЈ¬ЖрКјКұўЪЦРН¶Ил3molAЎў1molBЈ»ўЫЦРН¶Ил3 molAЎў1molBәН2molCЈ¬ФтҙпөҪЖҪәвКұЈ¬БҪИЭЖчЦРBөД°Щ·Цә¬БҝўЪ_____________ўЫ(Мо<Ўў>»тЈҪ)
24Ўў(6·Ц)AЎўBЎўCЎўDЎўEЎўFЎўGОӘУЙЖЯЦЦ¶МЦЬЖЪФӘЛШ№№іЙөДБЈЧУЈ¬ЛьГЗ¶ј УР10ёцөзЧУЈ¬ЖдҪб№№МШөгИзПВұнЈә
|
БЈЧУҙъәЕ |
A |
B |
C |
D |
E |
F |
G |
|
ФӯЧУәЛКэ |
өҘәЛ |
өҘәЛ |
Л«әЛ |
¶аәЛ |
өҘәЛ |
¶аәЛ |
¶аәЛ |
|
өзәЙКэ |
0 |
1+ |
1- |
0 |
2+ |
1+ |
0 |
ЖдЦРЈ¬BөДАлЧУ°лҫ¶ҙуУЪEөДАлЧУ°лҫ¶Ј»DКЗУЙј«РФјь№№іЙөД4ФӯЧУј«РФ·ЦЧУЈ»CіЈУГЧчFөДјмСй(јУИИ)ЎЈЗлМоРҙПВБРҝХ°ЧЈә
(1)ЎЎЎЎЎЎ AБЈЧУөДҪб№№КҫТвНјЎЎЎЎЎЎЎЎЎЎ ЎЈ
(2)ЎЎЎЎЎЎ ұИҪПBCәНEC2өДјоРФЗҝИхBCЎЎЎЎЎЎ EC2(Мо<ЎЎ Ўў>ЎЎ Ўў=ЎЎ )ЎЈ
(3)ЎЎЎЎЎЎ FУлC·ҙУҰөДАлЧУ·ҪіМКҪ
23Ј®(14·Ц)ДіТ»·ҙУҰМеПөЦРУР·ҙУҰОпәНЙъіЙОп№І5ЦЦОпЦКЈә
SЎўH2SЎўHNO3ЎўNOЎўH2OЎЈТСЦӘЛ®КЗ·ҙУҰІъОпЦ®Т»ЎЈ
(1)ёГ·ҙУҰЦРөД»№ФӯјБКЗ__________________Ј»(2)ёГ·ҙУҰЦРөД»№ФӯІъОпКЗ_______________Ј»
(3)РҙіцёГ·ҙУҰөД»ҜС§·ҪіМКҪІўұкіцөзЧУЧӘТЖ·ҪПтәНКэДҝ
____________________ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЈ»
(4)Иф·ҙУҰ№эіМЦРЧӘТЖБЛ0.3 molөзЧУЈ¬ФтЙъіЙЛ®өДЦКБҝКЗ______________ЎЈ
22Ўў(10·Ц)өзҪв·ЁЦЖјоөДЦчТӘФӯБПКЗұҘәНКіСОЛ®Ј¬УЙУЪҙЦСОЛ®ЦРә¬УРДаЙіЎўCa2+ЎўMg2+ЎўFe3+ЎўSO42-өИФУЦКЈ¬І»·ыәПөзҪвТӘЗуЈ¬ТтҙЛұШРлҫӯ№эҫ«ЦЖЎЈДіН¬С§ЙијЖБЛТ»ЦЦЦЖұёҫ«СОөДКөСй·Ҫ°ёЈ¬ІҪЦиИзПВ(УГУЪіБөнөДКФјБЙФ№эБҝ)Јә
ІҪҫЫ1ЈәИЎТ»¶ЁБҝөДҙЦСОЈ¬ЦГУЪЙХұӯЦРЈ¬јУИлЧгБҝөДЛ®Ј¬ЕдіЙҙЦСОЛ®Ј»
ІҪҫЫ2ЈәПтҙЦСОЛ®ЦРјУИліэФУКФјБЈ¬И»әуҪшРР№эВЛЈ¬ВЛИҘІ»ИЬОпЈ¬ФЩПтВЛТәЦРјУИлСОЛбөчҪЪСОЛ®өДpHЈ»
ІҪҫЫ3ЈәҪ«өГөҪөДИЬТәХф·ўЕЁЛхЎўАдИҙЎўҪбҫ§Ўў№эВЛЎўәжёЙјҙөГҫ«СОЈ»
Зл»ШҙрТФПВОКМвЈә
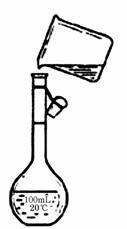 (1)ЙПКцКөСйЦРөД№эВЛІЩЧчРиТӘЙХұӯЎў____________Ўў___________өИІЈБ§ТЗЖчЎЈ
(1)ЙПКцКөСйЦРөД№эВЛІЩЧчРиТӘЙХұӯЎў____________Ўў___________өИІЈБ§ТЗЖчЎЈ
(2)ІҪҫЫ2ЦРіЈУГNa2CO3ЎўNaOHЎўBaCl2ЧчОӘіэФУКФјБЈ¬ФтјУИліэФУКФјБөДЛіРтОӘЈә_____________________________Ј»
(3)ІҪҫЫ2ЦРЈ¬ЕР¶ПјУИлBaCl2ТС№эБҝөД·Ҫ·ЁКЗЈә
________________________________________________Ј»
(4)ІҪҫЫ2ЦРЈ¬ИфПИУГСОЛбөчҪЪpHФЩ№эВЛЈ¬Ҫ«»б¶ФКөСйҪб№ыІъЙъУ°ПмЈ¬ЖдФӯТтКЗЈә
________________________________________________Ј»
(5)ОӘјмСйҫ«СОҙҝ¶ИЈ¬РиЕдЦЖ150 mL 0.2 mol/L NaCl(ҫ«СО)ИЬТәЈ¬ЙПНјКЗёГН¬С§ЧӘТЖИЬТәөДКҫТвНјЈ¬НјЦРУРјёҙҰҙнОуЈ¬Зл»ӯіцХэИ·өДЧӘТЖИЬТәКҫТвНјЎЈ
21. (6·Ц)ПВБРКөСйІЩЧчДЬҙпөҪКөСйДҝөДөДКЗ__________________(МоҙъәЕ)ЎЈ
AЈ®Пт·РЛ®ЦРөОИлЙЩБҝЕЁFeCl3ИЬТәЈ¬Цу·РЦБіКәмәЦЙ«Ј¬ЦЖИЎFe(OH)3ҪәМе
BЈ®ПтКўУРПЎHNO3өДКФ№ЬЦРјУИлНӯЖ¬Ј¬ЙФЙФјУИИЈ¬№ЫІмЙъіЙөДNOЖшМе
CЈ®Ҫ«pHКФЦҪКӘИуәуУГУЪјшұрNH3әНHClБҪЦЦҙМјӨРФЖшМе
DЈ®УГөО№ЬОьИЎNaOHИЬТәөОИлҫГЦГөДFeSO4ИЬТәЦРЈ¬ЦЖИЎFe(OH)2
EЈ®Ҫ«ідУРNO2ЖшМеөДГЬұХІЈБ§Зт·ЕИлИИЛ®ЦРЈ¬СйЦӨОВ¶И¶Ф»ҜС§ЖҪәвөДУ°Пм
20ЎўіЈОВПВЈ¬0.1molЎӨLЈӯ1ДіТ»ФӘЛб(HA)ИЬТәЦРc(OHЈӯ)/c(H+)ЈҪ1ЎБ10Јӯ8Ј¬ПВБРРрКцХэИ·өДКЗ
AЈ®ёГИЬТәЦРУЙЛ®өзАліцөДc(H+)ЈҪ1ЎБ10Јӯ11 molЎӨLЈӯ1
BЈ®УЙpHЈҪ3өДHAУлpHЈҪ11өДNaOHИЬТәөИМе»э»мәПЈ¬ИЬТәЦР
c(Na+)Јҫc(Ac-)Јҫc(OHЁD)Јҫc(H+)
CЈ®ЕЁ¶ИҫщОӘ0.1mol/LөДHAәНNaAИЬТәөИМе»э»мәПәуЈ¬ИфИЬТәіКЛбРФЈ¬Фт
c(AЈӯ)Јҫc(HA)Јҫc(Na+)Јҫc(H+)Јҫc(OHЈӯ)
DЈ®0.1molЎӨLЈӯ1HAИЬТәУл0.05molЎӨLЈӯ1NaOHИЬТәөИМе»э»мәПәуЛщөГИЬТәЦР
2c(H+)+c(HA)ЈҪc(AЈӯ)+2c(OHЈӯ)
·ЗСЎФсМв
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com