
题目列表(包括答案和解析)
44.若pH=3的酸溶液和pH=11的碱溶液等体积混合后 溶液呈酸性,其原因可能是
A 生成了一种强酸弱碱盐 B 弱酸溶液和强碱溶液反应
C 强酸溶液和弱碱溶液反应 D 一元强酸溶液和一元强碱溶液反应
43.将0.1mol·L-1CH3COOH溶液加水稀释或加入少量CH3COONa晶体时,都会引起
A 溶液的pH增加 B CH3COOH电离度变大
C 溶液的导电能力减弱 D 溶液中[OH-]减少
42.用实验确定某酸HA是弱电解质。两同学的方案是:
甲:① 称取一定质量的HA配制0.lmol/L的溶液100mL;
② 用pH试纸测出该溶液的pH值,即可证明HA是弱电解质。
乙: ① 用已知物质的量浓度的HA溶液、盐酸,分别配制pH=l的两种酸溶液各100mL;
② 分别取这两种溶液各10mL,加水稀释为100mL;
③ 各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现 象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH 1(选填>、<、=)
乙方案中,说明HA是弱电解质的现象是 (多选扣分)
(a)装HCl溶液的试管中放出H2的速率快;
(b)装HA溶液的试管中放出H2的速率快;
(c)两个试管中产生气体速率一样快。
(3)请你评价:乙方案中难以实现之处和不妥之处 、
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
[2001广东]
41.为更好地表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG=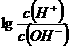 ,则下列叙述正确的是
,则下列叙述正确的是
A 中性溶液的AG=0 C 常温下0.lmol/L氢氧化钠溶液的AG=12
B 酸性溶液的AG<0 D 常温下0.lmol/L盐酸溶液的AG=12
40.将0.1mol/L的醋酸钠溶液20mL与0.1mol/L盐酸10rnL混合后,溶液显酸性,则溶液中有关微粒的浓度关系正确的是
A c (Ac-)>c (Cl-)>c (H+)>c (HAc)
B c (Ac-)>c (Cl-)>c (HAc)>c(H+)
C c (Ac-)=c (Cl+)>c (H+)>c (HAc)
D c (Na+)+c (H+)=c (Ac-)+c (Cl-)+c (OH-)
39.在 0.1 mol/L Na2CO3溶液中,下列关系正确的是
A.c(Na+) = 2c(CO32-) B.c(OH-) = 2c(H+)
C.c(HCO3-) > c(H2CO3) D.c(Na+) <(c(CO32-)+c(HCO3-) )
[2001上海]
38.取pH值均等于2的盐酸和醒酸各100ml分别稀释2倍后,再分别加入0.03g锌粉,在相同条件下充分反应,有关叙述正确的是
A .醋酸与锌反应放出氢气多
B.盐酸和醋酸分别与锌反应放出的氢气一样多
C.醋酸与锌反应速率大
D.盐酸和醋分别与锌反应的速度一样大
[2001春招]
37.等物质的量浓度的下列溶液中,N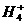 离子的浓度最大的是
离子的浓度最大的是
A.NH4Cl B.NH4HCO3 C.NH4HSO4 D.NH4NO3
36.)25℃时,若体积为Va、pH=a的某一元强酸与体积Vb、pH=b的某一元强碱混合,恰好中和,且已知Va<Vb和a=0.5b,请填写下列空白;
(1)a值可否等于3(填“可”或“否”)_________,其理由是____________________________________________;
(2)a值可否等于5(填“可”或“否”)________,其理由是_____________________________________________;
(3)a的取值范围是_______________________________________。
[2000上海]
35.室温下,在pH=12的某溶液中,由水电离的[OH-]为
A. 1.0×10-7mol·L-1 B.1.0×10-6mol·L-1 C.1.0×10-2mol·L-1 D.1.0×10-12mol·L-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com