
题目列表(包括答案和解析)
6、下列说法中,正确的是( )
A、常温常压下,1mol氖气含有的核外电子数为20NA
B、32g氧气和32g臭氧所含氧原子数都为2NA
C、18g水中所含的电子数是8NA
D、标准状况下,1L戊烷完全燃烧后生成二氧化碳的分子数是5NA/22.4
5、某液体分散系所表现出来的下列性质既可能是胶体所具有,也可能是溶液所具有的是( )
A、光线透过时,从侧面可观察到一条光亮的通路
B、加入适量稀H2SO4,产生沉淀
C、分散质微粒直径小于1nm
D、装入半透膜袋中并将其浸入盛水的烧杯中一段时间,结果袋外部有分散质微粒
4、油炸食品如薯片、虾条等容易挤碎,不宜选用真空袋装,而应采用充气袋装。下列气体中最不应该充入的是( )
A、氮气 B、二氧化碳 C、氧气 D、氩气
3、常用氯气给自来水消毒。某学生用自来水配制下列物质的溶液,不会产生明显药品变质的是( )
A、石蕊 B、硝酸银 C、亚硫酸钠 D、氯化铝
2、下列物质中,前者属于纯净物,后者属于混合物的是( )
A、净化后的空气;氧化镁
B、水和冰的混合物;澄清石灰水
C、生锈的铁钉;高锰酸钾充分加热后的剩余固体
D、氯化钾;液氧
1、下列关于研究物质性质的基本程序:①观察物质的外观性质②实验和观察③解释及结论④预测物质的性质。排列顺序正确的是( )
A、②①③④ B、①②③④ C、①④②③ D、④①②③
22.(7分)将7.5gNa2CO3·10H2O和Na2CO3配制成100ml混合溶液,测得C(Na+)=0.6
mol·L-1。
(1)若将等质量的混合物加热到恒重时,残留物的质量是多少?
(2)Na2CO3·10H2O和Na2CO3物质的量各是多少?
21.(6分)分别取等物质的量浓度的氢氧化钠溶液各100ml,再通入一定量的CO2,随后分别各取20mL溶液,向其中逐滴滴入0.2mol/L的盐酸,在标准状况下产生CO2的体积(y轴)与所加入盐酸的体积(x轴)的关系如图(分A、B两种情况):
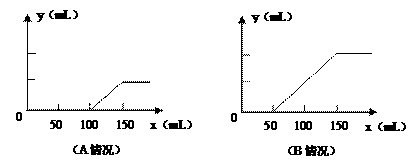
(1)在A情况下,溶质是(填化学式)___________,其物质的量之比为_________。
(2)在B情况下,溶质是(填化学式)_______ ,其物质的量之比为________。
(3)原氢氧化钠溶液的物质的量浓度为______________________。
20.(11分)某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示。
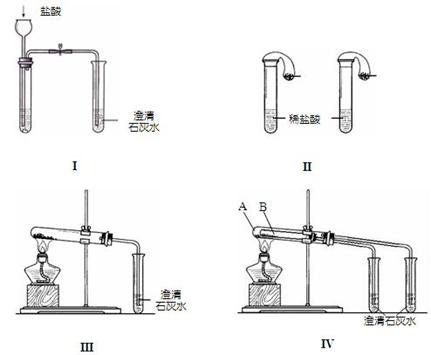
(1)只根据图I、II所示实验,能够达到实验目的是(填装置序号)__________________;
(2)图III、IV所示实验均能鉴别这两种物质,其反应的化学方程式为
______________________________
;与实验III相比,实验IV的优点是(填选项序号)___________________;
A.IV比III复杂
B.IV比III安全
C.IV比III操作简便
D.IV可以做到用一套装置同时进行两个对比实验,而III不行
(3)若用实验IV验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是___________________;
(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应。
①当石灰水过量时,其离子方程式为___________________ ;
②当碳酸氢钠与氢氧化钙物质的量之比为2 : 1时,所得溶液中溶质的化学式为___________________,请设计实验检验所得溶液中溶质的阴离子。
_____________________________________________________________________________________ 。
19.(7分)用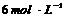 的硫酸配制
的硫酸配制 硫酸,若实验仪器有:
硫酸,若实验仪器有:
A.100mL量筒 B.托盘天平 C.玻璃棒 D.50mL容量瓶 E.20mL量筒
F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
(1)实验时应选用仪器的先后顺序是(填入编号)_________________________。
(2)在容量瓶的使用方法中,下列操作不正确的是(填写编号)___________________。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢
加入蒸馏水到接近标线2cm-3cm处,用滴管滴加蒸馏水到标线
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加
入蒸馏水到接近容量瓶刻度标线1cm-2cm处,用滴管滴加蒸馏水到刻度线
E.盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇
动多次
(3)怎样检查容量瓶是否漏水
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com